Осахаривающая способность характеризует суммарную способность амилолитических ферментов гидролизовать крахмал с образованием восстанавливающих сахаров (мальтозы и частично глюкозы).
За единицу осахаривающей способности принято такое количество фермента, которое в строго определенных условиях за 1 мин при 30° С катализирует расщепление до восстанавливающих сахаров 1 микроэквивалента глико- зидных связей. ОС выражают числом указанных 'единиц в 1 г ферментного препарата.
Сущность определения заключается в гидролизе крахмала раствором ферментов с последующим определением образовавшихся сахаров йодометрическим методом. В коническую колбочку вместимостью 50 мл вносят 20 мл 1 %-ного раствора крахмала и темперируют в ультратермостате при температуре 30° С в течение 10 мин, после чего добавляют 10 мл ферментного раствора и тщательно перемешивают. Рекомендуется одновременно ставить несколько проб с разным количеством ферментного раствора (1—10 мл), учитывая, что общий объем реакционной смеси должен быть 30 мл. Если ферментного раствора берут меньше чем 10 мл, то прежде чем внести его в колбочку, туда добавляют недостающее количество дистиллированной воды.
Реакцию проводят при температуре 30° С точно 10 мин, после чего действие ферментов прекращают добавлением 2 мл 1 н. раствора НСl. Если анализируют кислотоустойчивые амилазы культур Asp. awamori и Asp. niger, то количество НС1 увеличивают до 10 мл.
Для определения образовавшихся редуцирующих сахаров реакционную смесь количественно переносят в колбу вместимостью 300—400 мл, добавляют пипеткой 20 мл 0,1 н. раствора йода и 60 мл 0,1 н. раствора гидроксида натрия или калия. Если кислоты брали 10 мл, то необходимо добавить еще 8 мл 1 н. раствора NaOH. Щелочь приливают по каплям при перемешивании, затем, накрыв часовым стеклом, ставят колбу в темное место на 15 мин. После этого добавляют 2 мл серной кислоты, разбавленной водой в соотношении 1 : 4 и оттитровывают выделившийся йод 0,1 н. раствором тиосульфата йатрия. Контрольный опыт проводят с тем же количеством реактивов, только ферментный раствор вводят после добавления 2 мл 1 н. раствора НСl и не выдерживают в термостате.
Разница между количеством 0,1 н. раствора тиосульфата натрия, пошедшем на титрование опытной и контрольной пробы, должна быть в пределах 0,5—6 мл. Если она выходит за эти пределы, то опыт проводят с другими количествами ферментного раствора.
Осахаривающую способность ОС, ед/г, рассчитывают по формуле
ОС = e/pt,
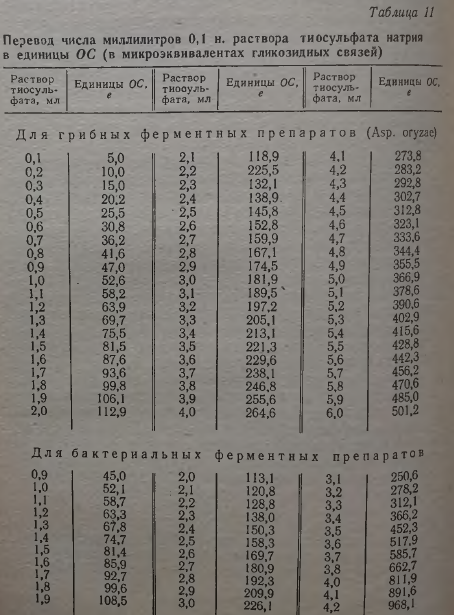
где е — количество единиц активности в микроэквивалентах гликозидных связей, найденное по разности титрований между контрольной и опытной пробой (табл. 11); р — навеска препарата, взятая на анализ, г; I — продолжительность гидролиза, мин.
Если, например, для определения взято 5 мл ферментного раствора после разведения в соотношении 1 : 10 000 (n =0,0005 г), на титрование контроля расходовано 20,4 мл 0,1 н. раствора Na2S203, на опыт — 18,1, то разность (20,4—18,1) = 2,3. По табл. 11 этому соответствует 132,1 ед. активности. Отсюда
ОС = 132,1/(0,0005 • 10) = 26420 ед/г.
Реактивы.
- 1%-ный раствор крахмала (см. с. 68).
- 1 н. ацетатный буфер pH 4,7;
- 0,1 н. раствор йода.
- 0,1 н. раствор тиосульфата натрия.
- Раствор серной кислоты 1 : 4. Один объем крепкой кислоты растворяют в 4 объемах дистиллированной воды (кислоту лить в воду!).
- 0,1 и 1 н. растворы гидроксида натрия.

