Информационный биополимер ДНК (дезоксирибонуклеиновая кислота) содержит всю генетическую информацию клетки. При делении каждая дочерняя клетка наследует по меньшей мере одну полную копию родительской ДНК, что позволяет потомству сохранять все морфологические и функциональные особенности, присущие данному виду. Генетическая информация в ДНК хранится в виде последовательности составляющих ее полимерную цепь остатков нуклеотидов. Механизм передачи информации и место процесса репликации ДНК в жизненном цикле клетки, а также другие аспекты регуляции жизнедеятельности клетки мы обсудим в гл. 6. Здесь же будут рассмотрены химия мономеров нуклеиновых кислот, структура полимерной ДНК и информация, закодированная в ее последовательности.
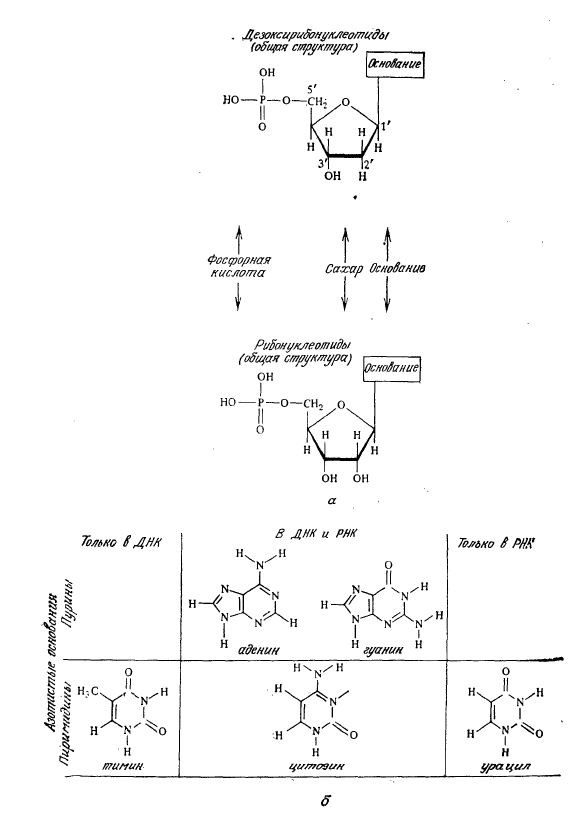
РИС. 2.7. а – общая структура рибонуклеотидов и дезоксирибонуклеотидов;
б – пять азотистых оснований, входящих в состав ДНК и РНК.
2.3.1. Структурные элементы нукленновых кислот;
переносчик энергиии коферменты
Помимо их роли как структурных элементов нуклеиновых кислот нуклеотиды и их производные представляют и самостоятельный биологический интерес. Все нуклеотиды построены из трех компонентов: фосфорной кислоты, альдопентоз рибозы или дезоксирибозы и азотистого основания, обычно производного пурина или пиримидина.
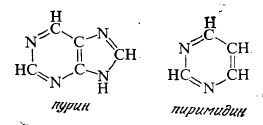
Эти три компонента образуют два типа нуклеотидов, отличающихся природой остатка альдопентозы (рис. 2.7). Рибонуклеиновые кислоты (РНК) представляют собой полинуклеотиды, содержащие остаток рибозы, а полимерные цепи дезоксирибонуклеиновых кислот (ДНК) построены с участием моносахарида дезоксирибозы. На рис. 2.7 изображены также химические формулы пяти азотистых оснований, входящих в состав нуклеотидов ДНК и РНК. Три из этих оснований, аденин (А), гуанин (G) и цитозин (С), типичны как для ДНК, так и для РНК. Напротив, тимин (Т) входит в состав только ДНК, а родственное пиримидиновое основание урацил (U) специфично для РНК. Оба типа нуклеотидов представляют собой сильные кислоты, что обусловлено наличием остатка фосфорной кислоты.
Отщепление фосфатной группы от 5'-углеродноrо атома нуклеотида приводит к соответствующему нуклеозиду. Как показано в табл. 2.4, названия нуклеозидов и нуклеотидов являются производными от названий соответствующих азотистых оснований. Следует отметить, однако, что для нуклеотидов применяется и другая номенклатура. Например, аденилат можно назвать также аденозин-5'-монофосфатом. Номенклатура последнего типа применяется обычно для производных нуклеозидов, у которых гидроксильная группа при С-5' этерифицирована дифосфатной или трифосфатной группировкой, напри.мер аденозин-5'-трифосфат (АТР).
Таблица 2.4. Номенклатура нуклеозидов и нуклеотидов. Как показано в последней строке,
префикс «дезокси-» применяется для обозначения соединений, содержащих остаток дезоксирибозы

С биологической точки зрения особенно важен нуклеозид аденозин, построенный из остатков рибозы и аденина. На рис. 2.8 изображено строение аденозин-5' -монофосфата (АМР) и ряда его важных производных. К. АМР могут быть присоединены еще один или два остатка фосфорной кислоты, в результате чего образуются ADP (аденозин-5'-дифосфат) и АТР соответственно. При гидролизе соединяющих фосфатные группы фосфодиэфирных связей высвобождается большое количество энергии. Например, превращение АТР в ADP и фосфат при 3°С и рН 7 (напомним, что рН = –lg αн, где αн – концентрация ионов Н+ в растворе в моль/л) сопровождается изменением стандартной энергии Гиббса, равным -7,3 ккал/моль.
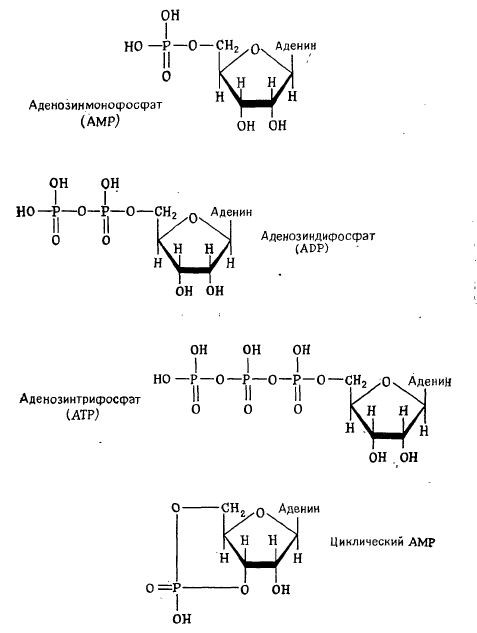
РИС. 2.8. Фосфаты аденозина. АМР, ADP и АТР участвуют в процессах переноса
энергии в клетке, а циклический АМР выполняет регуляторные функции.
Мы привыкли оценивать энергетический эффект реакций прежде всего в единицах тепловой энергии, т. е. теплоты, однако клетка представляет собой, в сущности, изотермическую систему, в которой, как правило, реализуются химические пути трансформации энергии. Позднее, в гл. 6, мы значительно подробнее рассмотрим АТР в качестве основного переносчика химической энергии во всех клетках без исключения. По сути дела, АТР является аккумулятором энергии, получаемой из питательных веществ или солнечного света, которая затем расходуется в биосинтезе полимеров, транспорте веществ через мембраны и движении клеток. Дифосфаты и трифосфаты других нуклеотидов также могут выполнять аналогичные функции в химии клетки, но основными переносчиками энергии служат все же аденозинфосфаты.
Циклическая форма АМР, содержащая внутримолекулярный цикл с участием фосфатной группы (рис. 2.8), выполняет функции регулятора множества клеточных реакций, включая реакции образования полисахаридов и резервных полимеров (жиров).
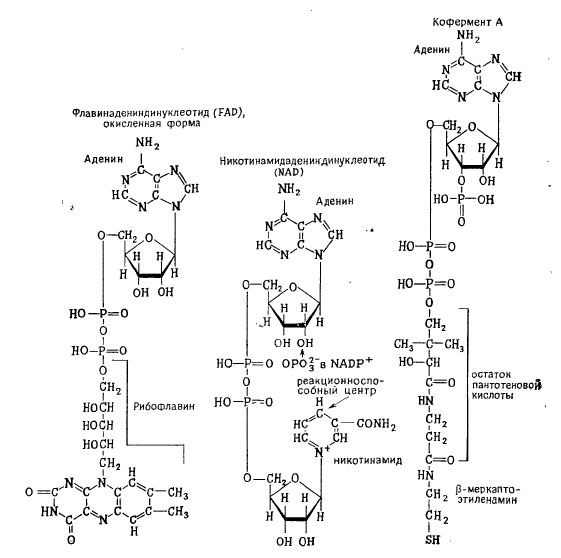
РИС. 2.9. Три важных кофермента, являющиеся производными нуклеотидов.
Недостаток циклического АМР в тканях связывают с одним из видов рака, т. е. состояния относительно неконтролируемого роста клеток.
Аденозинмонофосфат не только является структурным элементом нуклеиновых кислот, но и служит основой для построения ряда коферментов, химические формулы которых изображены на рис. 2.9. Кинетика ферментативных реакций рассматривается в следующей главе; здесь же достаточно отметить, что коферментами мы называем органические соединения, необходимые для активации некоторых ферментов, т. е. для их перевода в ту форму, в которой они способны выполнять каталитические функции. Поскольку практически все реакции в клетке катализируются ферментами, изменение концентрации коферментов представляет собой удобный способ регуляции активности соответствующих ферментов в клетке и таким путем изменения скорости некоторых внутриклеточных процессов.
2.3.2. Хранение биологической информации, ДНК и РНК
Как и полисахариды, полинуклеотиды образуются путем конденсации мономеров. И в РНК, и в ДНК нуклеотиды соединены фосфатными связями, образующимися с участием гидроксильных групп при С-3' и С-5' рибозы или дезоксирибозы. В качестве примера на рис. 2.10 приведена структура одного из тринуклеотидов. Клеточные молекулы ДНК невероятно велики: вся наследственная информация прокариот хранится в одной молекуле ДНК с молекулярной массой порядка 2·109.В эукариотах ядро может содержать несколько больших молекул ДНК. Отрицательные заряды ДНК нейтрализуются двузарядными катионами (в прокариотах) или основными аминокислотами (в эукариотах).
Следует подчеркнуть, что последовательность нуклеотидов, как это показано на рис. 2.10, α, имеет направление или полярность, обусловленную тем обстоятельством, что на одном конце цепи находится свободная гидроксильная группа при С-5', а на другом – гидроксил при С-3'. На рис. 2.10, 6 приведен удобный способ изображения нуклеотидной последовательности в направлении от 5' – к 3'-концу. Часто применяют и еще более короткие обозначения. Предположим, например, что основания 1, 2 и 3 на рис. 2.10, 6 являются цитозином, аденином и тимином соответственно; тогда та же самая нуклеотидная последовательность может быть записана в виде рСрАрТ или даже еще короче: САТ.
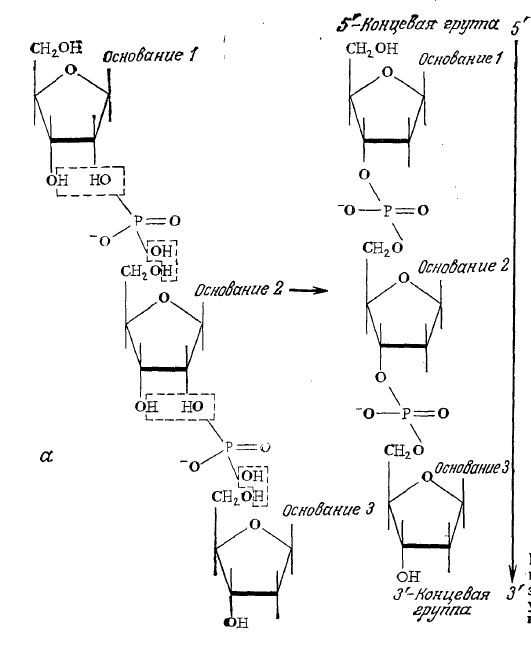
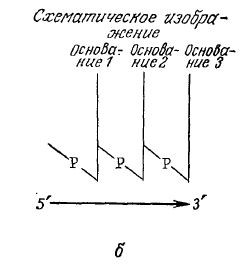
РИС. 2.10. а – конденсация нескольких нуклеотидов с образованием цепи, связанной фосфодиэфириыми связями;
б – упрощенное схематическое изображение нуклеотидной цепи.
Как предположили в 1953 г. Джеймс Уотсон и Фрэнсис Крик, молекула ДНК состоит из двух полинуклеотидных цепей, образующих двойную спираль (рис. 2.11). Имеющий форму правильной спирали каркас молекулы построен из остатков сахаров и фосфатных групп. Внутри двойной спирали расположены пуриновые и пиримидиновые основания. Именно последовательность четырех различных азотистых оснований в полинуклеотидной цепи содержит в себе всю генетическую информацию, в частности данные о структуре синтезируемых рибонуклеиновых кислот и белков. Механизмы, регулирующие и использующие генетическую информацию ДНК, мы рассмотрим в гл. 6.
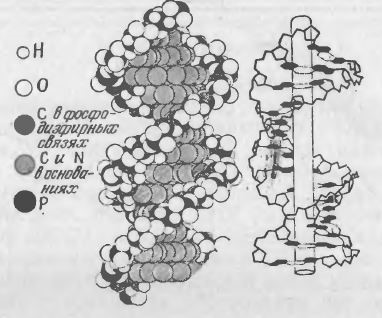
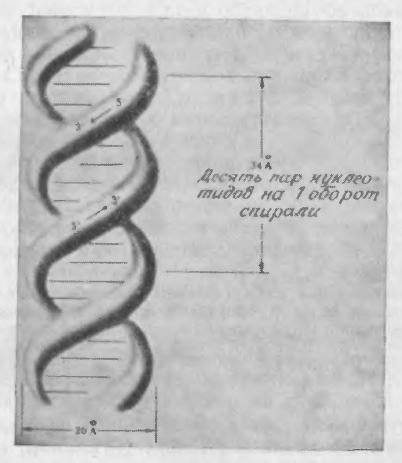
РИС. 2.11. Изображенная несколькими способами структура двойной спирали ДНК. На этом рисунке показана
классическая структура Уотсона – Крика [7], называемая также В-ДНК; она представляет собой правую спираль,
в которой плоскости пар оснований перпендикулярны оси спирали. В нижней части рисунка приведена схема,
иллюстрирующая некоторые геометрические параметры этой структуры.
Азотистое основание одной цепи двойной спирали взаимодействует с пространственно наиболее близко расположенным основанием другой цепи строго определенным образом, так что аденин специфично связывается только с тимином, а гуанин – с цитозином. На рис. 2.12 показано замечательное геометрическое сходство этих пар оснований, а также наличие двух и трех водородных связей в парах оснований А-Т и C-G соответственно.
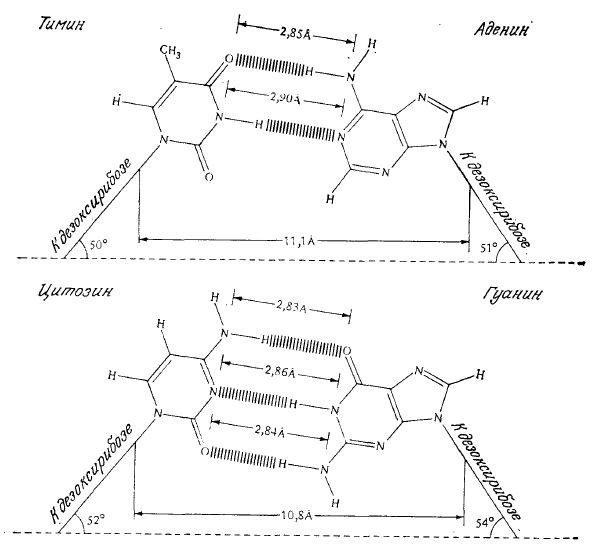
РИС. 2.12. Комплементарные пары оснований аденин – тимин и гуанин – цитозин, образующиеся
за счет водородных связей и обладающие очень близкими пространственными характеристиками,
что способствует формированию пар оснований внутри двойной спирали молекулы ДНК
Две цепи ДНК имеют противоположную направленность (5'→3' и З'→5'). Поэтому, располагая информацией о нуклеотидной последовательности одной дезоксирибонуклеотидной цепи, например, 5'CGAATCGTA3', можно сделать вывод о строении соответствующего фрагмента двуспиральной молекулы ДНК; в нашем случае этот фрагмент будет иметь структуру
5' CGAATCGТАЗ' 3'GCTTAGCAT5'
К той же самой двуспиральной структуре мы пришли бы, если бы нам была задана последовательность 5'ТACGAТТСGЗ'. Таким образом, в информационном смысле последовательность одной цепи определяет последовательность комплементарной цепи, т. е. каждая цепь служит матрицей для другой.
Это характерное свойство ДНК является основой для синтеза дочерних ДНК из исходной родительской молекулы ДНК – процесса, называемого репликацией ДНК. Если две комплементарные цепи ДНК разделяются и затем на каждой из цепей в соответствии с правилами образования пар оснований строятся двойные спирали, то конечным продуктом такого процесса будут две новые молекулы, каждая из которых идентична исходной двухцепочечной· ДНК и содержит одну новую и одну старую цепь (рис. 2.13). Таким образом, образование пар оснований составляет химическую основу считывания биологической информации, закодированной в нуклеотидной последовательности ДНК. Справедливость общих принципов такого механизма, схематично изображенного на рис. 2.13, была убедительно доказана экспериментами по выращиванию клеток Е. coli сначала в среде, содержащей 15N, а затем в среде только с нормальным изотопом азота 14N. Содержащие различные изотопы ДНК могут быть разделены на ультрацентрифуге. Ультрацентрифугирование и применение изотопных меток, в том числе радиоактивных, являются важнейшими инструментами экспериментальных исследований в современной биохимии.
Другая важная деталь структуры ДНК- водородные связи, с помощью которых формируются пары оснований (рис. 2.12). Водородные связи способствуют стабилизации двухцепочечноft структуры ДНК, однако эта стабилизация не является ни постоянной, ни необратимой. Как это показано на схеме репликации (рис. 2.13), биологическая функция ДНК основана на раскручивании спирали и разделении двух цепей. В ходе дальнейшего изучения молекулярной генетики (гл. 6) мы ознако мимся и с другими важными функциями одноцепочечных сегментов ДНК.
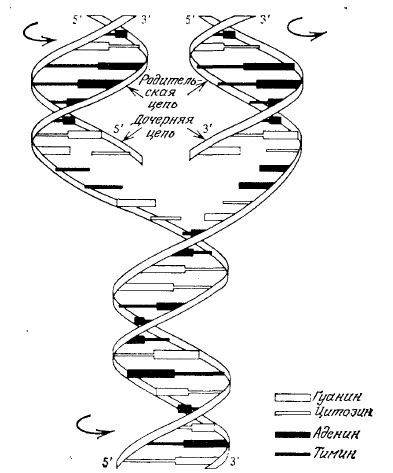
РИС. 2.13. Упрощенная схема репликации ДНК. По мере разделения цепей родительской ДНК
на них синтезируются комплементарные цепи, что приводит к образованию двух дочерних молекул,
идентичных родительской ДНК. Обратите внимание на то, что каждая дочерняя молекула содержит одну цепь родительской ДНК
Разделение двух цепей ДНК при нагревании является основой важного метода идентификации различных ДНК. Поскольку пары оснований АТ связаны двумя водородными связями, а пары GC – тремя, то содержащие большее число пар АТ участки ДНК плавятся (так условно называется процесс разделения двух цепей) раньше, чем участки, обогащенные парами GC. Процесс плавления легко контролируется путем измерения поглощения раствора ДНК при 260 нм; одноцепочечные ДНК поглощают сильнее, и процесс плавления ДНК регистрируется по увеличению общей абсорбции. Температурой плавления, Тпл, называют температуру, при которой изменение абсорбции составляет 50% от разницы в абсорбции между полностью двухцепочечной и полностью расплавленной (одноцепочечной) ДНК. Как и следовало ожидать, величина Тпл коррелирует с содержанием GC. Например, ДНК из Е. coli, содержащая 50% GC, имеет Тпл= 69 °С, а ДНК из Pseudomonas aeruginosa с 68% GC характеризуется Тпл=76°С. Содержание GC в различных организмах меняется в широких пределах (от 23 до 75%). Особенности нуклеотидного состава иногда используются для идентификации организмов.
Если раствор расплавленной ДНК охладить, то разделенные комплементарные цепи вновь образуют структуру типа двойной спирали (эту операцию называют отжигом). Аналогично два различных одноцепочечных сегмента ДНК с частично комплементарными последовательностями могут подвергаться гибридизации с образованием сегмента двойной спирали. Гибридизация является важнейшим экспериментальным приемом в биохимии и технологии рекомбинантных ДНК (гл. 6). В завершение этого краткого введения в физическую химию ДНК следует отметить, что двухцепочечную ДНК можно также расплавить или денатурировать путем добавления щелочи или кислоты, что приводит к ионизации оснований. Можно упомянуть также, что с точки зрения гидродинамики двухцепочечная ДНК в растворе ведет себя подобно жесткому стержню, в то время как одноцепочечная ДНК по своему поведению напоминает неупорядоченный полимерный клубок.
Как уже упоминалось выше, вся информация, необходимая для выполнения клеткой ее важнейших функций, в том числе роста и деления, в бактериях типа Е. coli содержится в одной молекуле ДНК, которая имеет строение гигантского кольца. В нативном состоянии ДНК из Е. coli существует в сверхспирализованной форме, что отчетливо видно на электронных микрофотоrрафиях бактерии в виде несколько размытого нуклеотида (см. рис. 1.2). Эта большая основная ДНК клетки называется хромосомой бактерии; кольцевая хромосома Е. coli построена из 4,7 миллиона пар оснований*.
В заключенном в мембрану ядре эукариот ДНК обычно поделена между несколькими хромосомами; последние могут быть намного больше хромосом прокариот. В состав хромосом эукариот входят также небольшие основные белки, называемые гистонами, которые составляют около половины массы хромосомы. Этот комплекс нуклеиновых кислот и белков хромосом эукариот называется хроматином. В хлоропластах и митохондриях эукариотических клеток также имеются отдельные, более мелкие молекулы ДНК.
Очень существен тот факт, что клетки могут содержать и другие молекулы ДНК. Относительно небольшие ДНК, существующие во многих бактериях и эукариотах, называют плазмидами. Бактериальные плазмиды, например, представляют собой кольцевые молекулы ДНК, содержащие от 4 до 50 тысяч пар оснований. Биологические функции плазмид состоят в обеспечении клетки-хозяина полезными, но не самыми необходимыми качествами, например, устойчивостью к антибиотикам. В биохимических исследованиях и в технологических процессах плазмиды занимают одно из самых центральных мест, являясь важным инструментом методов рекомбинантных ДНК. Как мы увидим в гл. 6, модификация плазмид в лабораторных условиях и последующее введение рекомбинантных плазмид в живые клетки позволяют изменить их генетическую программу, с тем чтобы заставить продуцировать новые соединения или более эффективно расти.
____________________________
* Выраженную в тысячах оснований длину ДНК можно перевести в единицы длины, приняв, что 1 тысяче оснований соответствует длина 0,34 мкм. Кроме того, молекулярная масса двухцепочечной ДНК с 1 тысячью оснований равна приблизительно 660 ООО атомных единиц массы.
Другие небольшие молекулы ДНК могут быть введены в живые клетки вирусами. Небольшие вирусы, способные заражать бактерии, называют бактериофагами или, короче, фагами. Последние могут вызывать ряд трудностей в крупномасштабных технологических процессах с использованием чистых бактериальных культур. В то же время изучение фагов позволило внести большой вклад в развитие молекулярной генетики. Кроме того, фаги используются для создания стабильных рабочих коллекций или библиотек сегментов ДНК. Фаг λ Е. coli содержит одну циклическую двухцепочечную молекулу ДНК, построенную из 48,6 тысяч пар оснований. ДНК фага Т2 Е. coli состоит из 166 тысяч пар оснований.
Основная функция ДНК заключается в хранении инструкций для синтеза молекул РНК определенной нуклеотидной последовательности и длины; некоторые из этих РНК затем направляют синтез различных специфических белков. Кодирующий последовательность молекулы РНК сегмент ДНК называется геном. Ниже мы вкратце расмотрим различные типы РНК, а затем перейдем к обсуждению белков и тех структурных элементов, из которых они построены.
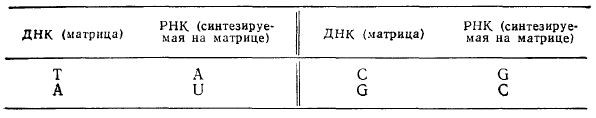
Во всех клетках имеются рибонуклеиновые кислоты трех типов, четвертый тип характерен для некоторых вирусов. Молекулы РНК построены из остатков рибонуклеотидов, углеводным компонентом которых является рибоза (а не дезоксирибоза, как в ДНК). Подобно ДНК, в РНК нуклеотиды расположены в определенной последовательности. В сущности, нуклеотидная последовательность РНК строится на основе той информации, которая содержится в соответствующих сегментах ДНК. В передаче информации от ДНК к РНК основную роль опять-таки играет образование пар оснований. Правила образования пар оснований в этом случае аналогичны тем, которым подчиняется процесс образования пар оснований двухцепочечных ДНК, за исключением пары аденин-тимидин; при синтезе РНК вместо нее формируется пара аденин-урацил:
В нормальном цикле жизнедеятельности клетки участвуют различные РНК, выполняющие важную функцию прочтения и реализации генетической информации, заложенной в ДНК. Матричная, или информационная, РНК (мРНК или иРНК) комплементарна последовательности оснований гена в ДНК. Каждая молекула мРНК переносит определенную информацию от ДНК (к другому механизму биохимического аппарата клетки. Поскольку объем этой информации меняется в довольно широких пределах, то и величина молекул мРНК тоже может быть различной; обычно цепь мРНК содержит 103-104 нуклеотидов. РНК почти всегда имеют одноцепочечную структуру, тогда как образование меж- и внутримолекулярных пар оснований часто играет важную роль в структуре или функции РНК.
Содержащаяся в мРНК информация считывается в рибосоме (рис. 1.2 и 1.3). До 65% рибосомы составляет рибосомальная РНК (рРНК), которая в свою очередь может быть разделена (например, центрифугированием) на РНК нескольких типов. В частности, рибосома Е. coli содержит три различные РНК, обозначаемые 23S, 16S и 5S, которые содержат около 3•103, 1,5•103 и 102 нуклеотидных остатков соответственно. В рибосомах из цитоплазмы клеток-эукариот, с другой стороны, имеются 28S, 18S, 7S и 5S рРНК, а в рибосомах митохондрий и хлоропластов обнаружены РНК, специфичные только для этих органоидов.
Транспортные РНК (тРНК) отличаются наименьшей молекулярной массой и содержат всего лишь от 70 до 95 нуклеотидных остатков; они находятся в цитоплазме клетки и участвуют в процессе реализации генетического кода в рибосоме. В табл. 2.5 приведены основные свойства различных РНК бактерии Е. coli. Нуклеотидные последовательности и, следовательно, структуры и функции различных клеточных рРНК и тРНК, как и мРНК, определяются последовательностями нуклеотидных остатков соответствующих генов клеточной ДНК.
Таблица 2.5. Свойства РНК Е colia

Конечный результат этого сложного процесса передачи и трансляции информации состоит в синтезе молекулы белка. Белки представляют собой материальное биохимическое выражение генетической информации и инструкций, носителем которых является ДНК. Используя терминологию, принятую в теории управления процессами, можно сказать, что белки – это конечные элементы управления, которые передают командные сигналы ДНК клеточным процессам. Ниже и в некоторых последующих главах мы рассмотрим динамику и свойства этих элементов управления.

