B гл. 3 и 4 мы рассматривали кинетику реакций в системах с изолированными ферментами, а также практическое применение свободных ферментов и ферментных препаратов. Большинство упоминавшихся в гл. 3 работ по изучению кинетики ферментативного катализа и большая часть приведенных в гл. 4 примеров практического применения ферментов относятся к гидролазам, которые по определению расщепляют или разлагают большие молекулы на более мелкие с участием воды в качестве второго субстрата. Такие процессы деградации сопровождаются снижением свободной энергии системы и поэтому в закрытой системе происходят спонтанно. B настоящем разделе мы рассмотрим механизмы, которые позволяют открытой системе, а именно живой клетке, сочетать реакции, протекающие с выделением энергии (экзэргонические), с реакциями и другими функциями, осуществляющимися только с затратой определенного количества энергии (эндэргонические процессы).
5.2.1. ATP и другие фосфаты
Ранее мы уже упоминали о строении и некоторых свойствах аденозинтрифосфата (ATP; см. разд. 2.3.1 и рис. 2.8), где, в частности, отмечали, что ферментативный гидролиз ATP до ADP и неорганического фосфата сопровождается большим отрицательным изменением свободной энергии:
АТР + Н2О → ADP + Pi ΔG°' = — 7,3 ккал/моль (5.11)
Здесь Pi — неорганический фосфат. Таким образом, в ходе гидролиза ATP выделяется большое количество энергии, а в обратной реакции присоединения фосфата к ADP энергия может запасаться и храниться в видеАТРдляпоследующего использования. Давайте рассмотрим, как реализуется последний процесс в условиях сопряженных химических реакций.
Понятие об общем промежуточном соединении можно проиллюстрировать на примере другой последовательности реакций, являющейся частью пути метаболизма Эмбдена — Мейергофа — Парнаса. Превращение альдегида в карбоновую кислоту (в водном растворе) сопровождается понижением свободной энергии примерно на 7000 кал/моль. Как показано на рис. 5.3, в изолированной системе эта свободная химическая энергия полностью рассеялась бы в растворе. B живой клетке, однако, этого не происходит. При биохимическом окислении глюкозы превращение глицеральдегид-З-фосфата в соответствующую карбоновую кислоту (З-фосфоглицерат) сапровожда- ется регенерацией ATP из ADP (см. реакцию 2 на рис. 5.3). Таким образом, обусловленное окислением альдегида уменьшение свободной энергии благодаря участию фермйнтативной системы клетки сочетается с одновременной регенерацией ATP.
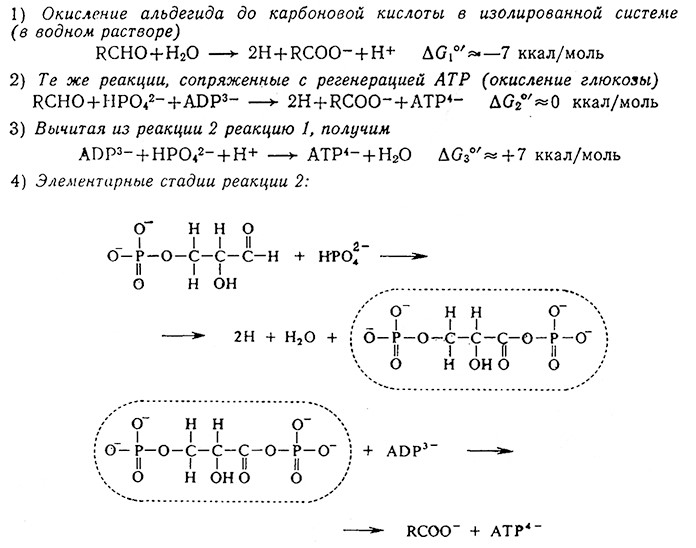
РИС. 5.3. Примеры реакций с общим промежуточным соединением.
Поскольку в результате реакции 2 свободная энергия практически не изменяется, то высвобождающаяся при окислении глицеральдегид-З-фосфата свободная энергия, очевидно, трансформируется в так называемую высокоэнергетическую (макроэргическую) фосфатную связь аденозинтрифосфата.
Последовательность элементарных реакций, в действительности происходящих в клетке, изображена в нижней части рис. 5.3. K наиболее существенным характеристикам этих двух последних реакций относятся, во-псрвых, наличие общего промежуточного соединения, являющегося продуктом первой реакции и реагентом во второй, и, во-вторых, большая свободная энергия реакции гидролиза (отщепления фосфатной группы) промежуточного фосфорилнрованного соединения по сравнению с гидролизом ATP. Равновесие последней стадии смещено вправо, т. е. в сторону образования продукта реакции; таким образом, этот этап метаболизма глюкозы одновременно представляет собой и один из нескольких центров регенерации ATP, необходимого для эндергонических реакций. Регенерация ATP осуществляется путем превращения частично метаболизи- рованного питательного вещества в высокоэнергетическое фос- форилированное промежуточное соединение, которое затем в результате катализируемой ферментом реакции передает фосфатную группу ADP.
Фосфорилирование различных соединений, в том числе и ADP, используется клеткой для нескольких целей. Во-первых, фосфорилированные соединения представляют собой удобное хранилище значительной части свободной энергии, выделяющейся в процессе окисления клеточного топлива. Свободная энергия гидролиза некоторых соединений, называемых фосфатными донорами, превышает ΔG0°' гидролиза ATP (например, величины ΔG0°' для гидролиза фосфоенолпирувата и 1,3-дифосфоглицерата равны —14,8 и —11,8 ккал/моль соответственно). Следовательно, гидролиз этих соединений может использоваться для фосфорилирования ADP. Аналогично гидролиз ATP может быть связан с фосфорилированием некоторых соединений, в результате которого образуются «низкоэнергетические» фосфаты; величины ΔG0' расщепления последних ниже соответствующей величины для реакции гидролиза ATP (например, AG0' гидролиза глюкозо-6-фосфата и глицеро-1-фосфата составляют —3,3 и —2,20 ккал/моль соответственно).
Вторая важная функция фосфорилирования в жизни клеток связана с неспособностью сильноионизированных органических веществ проникать через клеточные мембраны. Благодаря этому обстоятельству заряженные фосфорилированные соединения, являющиеся промежуточными соединениями во многих путях метаболизма, остаются внутри клетки, что в свою очередь позволяет получить максимум энергии и химического сырья из питательных веществ. Обычно дефосфорилирование является последней стадией метаболического пути; неионизи- рованные отходы жизнедеятельности клетки могут выводиться в среду.
5.2.2. Окисление и восстановление;
сочетание с превращением NAD
Мы только что рассмотрели роль ATP как переносчика фосфатных групп, связывание и отщепление которых сопровождается поглощением или выделением довольно значительного ко-личества энергии. B этом разделе мы вкратце проанализируем, как в живой клетке происходят процессы окисления-и восстановления и как они связаны с метаболизмом ATP.
Прежде всего вспомним, что окисление какога-либо соединения означает, что его молекулы теряют электроны, а присоединение электронов есть не что иное, как восстановление. При биохимическом окислении органическое вещество обычно теряет электроны в виде атомов водорода; следовательно, термины окисление и дегидрирование здесь являются синонимами. Точно так же восстановление или присоединение электронов обычно осуществляется путем гидрирования. Примером могут служить реакции восстановления пировиноградной кислоты и окисления молочной кислоты:

(Пировиноградная кислота представляет собой по сути дела то же, что пируват на рис. 5.1. Пируватом называют ионизированную форму кислоты СН3СОСОО–, преобладающую при биологических pH.)
Роль переносчиков пар атомов водорода, высвобождающихся в процессах окисления и расходующихся в реакциях восстановления, выполняют производные нуклеотидов, в первую очередь никотинамидадениндипуклеотид (NAD) (см. рис. 2.9) и его фосфорилированное производное NADP. Ранее эти соединения относили к коферментам, поскольку их присутствие обычно обязательно в процессах ферментативного окисления или восстановления. Если, например, необходимы атомы водорода, то никотинамидная группировка восстановленной формы NAD может отдать их в процессе окисления:
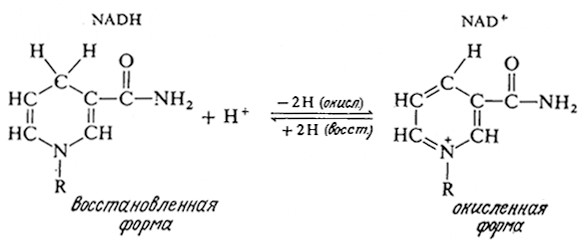
Процесс окисления легкообратим, поэтому NAD может и присоединять электроны (атомы H), если последние высвобождаются в процессах окисления других соединений. Окисленную и восстановленную формы NAD мы будем обозначать далее так, как и на приведенной выше схеме, символами NAD+ и и NADH соответственно.
Как переносчик электронов NAD выполняет две основные функции, первая из которых аналогична функции ATP и заключается в переносе восстанавливающих эквивалентов (электронов или атомов H), высвобождающихся в ходе распада питательных веществ, к биосинтетическим реакциям. Необходимость в восстановлении часто обусловливается тем обстоятельством, что степень окисления непосредственных продуктов биосинтеза не всегда соответствует степени окисления веществ, необходимых для построения структурных элементов клетки. Как мы уже отмечали, степень окисления углерода в клетке приблизительно соответствует углеводам (СН2О)n, поэтому аутотрофным организмам, использующим в качестве источника углерода CO2, для успешной ассимиляции углерода необходимо обладать большой восстанавливающей способностью:
CO2+4H → (CH2O)+H2O
Хотя восстанавливающие эквиваленты в наибольшей степени используются в процессах ассимиляции углерода, усвоение серы и азота также часто требует участия восстановительных реакций. Чтобы оценить эти потребности, можно принять, что клетка содержит азот в основном в степени окисления аммиака (NH3), а серу — главным образом в форме, аналогичной сульфидному иону (S2–). Тогда для утилизации, например, сульфата, в качестве источника серы клетке потребуется значительная восстанавливающая способность, о чем свидетельствует соответствующее уравнение реакции:
SO42–+8H → S2–+4H2O
NAD и родственные пиридиновые нуклеотиды, также выполняющие функцию переносчика атомов водорода, участвуют и в образовании ATP в аэробном метаболизме. B разд. 5.3 мы подробнее изучим процесс соединения атомов водорода из NADH с кислородом в последовательности реакций, известной под названием дыхательной цепи. Выделяющейся в этой последовательности реакций окисления энергии достаточно для превращения трех молекул ADP в ATP.
Интересно, что во всех известных биологических системах, включая анаэробные, аэробные и фотосинтезирующие организмы, ATP является основным инструментом аккумулирования и хранения энергии окисления или света, необходимой дляосуществления эндэргонических процессов в клетке. B последующих разделах этой главы мы проследим за ходом процео сов утилизации ATP и переноса электронов во все более и более сложных путях метаболизма в анаэробных, аэробных и фотосинтсзирующих системах. Анализ уравнений окислительно- восстановительных реакций позволит нам найти стехиометриче- ские ограничения, налагаемые составом питательной среды и клеток, путями метаболизма и природой конечных метаболитов. Поскольку свободная энергия окисления клеточного топлива в конечном счете хранится в ATP, то эффективность утилизации ATP в различных клеточных процессах может служить удобной мерой относительного количества энергии, потребляемой клеткой в этих процессах. Более того, изучение ATP позволяет логически увязать процессы построения углеродных скелетов и связанные с ними изменения свободной энергии. Наконец, сравнение энергетики различных биологических систем дает возможность понять основу высокой термодинамической эффективности их биосинтетического аппарата.

