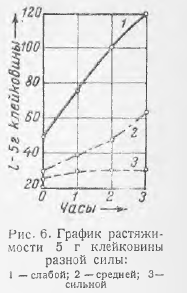
Соединительная ткань входит в состав хрящей, сухожилий, подкожной клетчатки, кости, межклеточного вещества мышц, паренхиматозных органов, стенок сосудов. Все разновидности соединительной ткани составляют около 50% массы тела животного. Несмотря на некоторые морфологические различия, для всех видов соединительной ткани характерно наличие внеклеточных волокнистых структур — коллагеновых и эластино- вых волокон, окруженных межклеточным основным веществом, на долю которого приходится до 30% сухой массы соединительной ткани (рис. 6).
Коллагеновые волокна содержат коллаген, на долю которого приходится около '/з общего количества белков. Кроме того, в их состав входят и другие компоненты.
С помощью электронной микроскопии установлено, что коллагеновые волокна построены из фибрилл различного диаметра, имеющих поперечную исчерченность Фибриллы построены из макромолекул коллагена — тропоколлагена. Тропоколлаген (молекулярная масса 360 000) состоит из трех полипептидных цепей, образующих тройную спираль диаметром около 1,5 нм и длиной 300 нм. Каждая цепь состоит из 1000 аминокислот и имеет молекулярную массу 1200. Структура макромолекулы стабилизируется водородными связями между пептидными группами соседних цепей.
Особенности взаиморасположения молекул тропоколлагена,соединенных конец к концу и бок о бок, определяют характер строения фибрилл (рис. 7). В параллельных нитях, образованных соединением тропоколлагена конец к концу, начало молекул смещено, что обусловливает наблюдаемую периодичность в строении фибрилл. Период поперечной исчерченности коллагеновых волокон 64—70 нм.
Специфика структуры тропоколлагена определяется особенностями его аминокислотного состава. Примерно 33% аминокислотных остатков макромолекул коллагена составляет глицин, 21% — пролин и оксипролин, 11% — аланин. В коллагене отсутствуют триптофан, цистин, цистеин, мало метионина и тирозина. Наличие оксипролина, который присутствует в очень немногих белках, позволяет по содержанию этой аминокислоты судить о количестве коллагена в мясе.
Особенности строения коллагеновых волокон определяют их высокую способность к набуханию и большую механическую прочность, что, в свою очередь, влияет на консистенцию мяса. Нативный коллаген не растворим в воде, но способен к набуханию. Он устойчив к действию пепсина и трипсина, подвергается гидролизу в присутствии коллагеназы поджелудочной железы. Коллаген может быть превращен в легкоусвояемые полипептиды в результате гидролиза некоторыми растительными ферментами. Под действием альдегидов происходит дубление коллагена — образование между пептидными цепями метиленовых мостиков, что повышает его механическую прочность, устойчивость к нагреванию в присутствии воды и воздействию протеолитических ферментов.
Тепловая обработка приводит к процессам дезагрегации макромолекул коллагена, характер которых зависит от температуры и продолжительности нагрева.
При умеренном тепловом воздействии происходит «сваривание» коллагена в результате нарушения части водородных связей внутри пептидных цепей. Изменение их взаиморасположения в трехспиральной структуре тропоколлагена сопровождается ее разрыхлением, повышением гидратации системы и увеличением доступности пептидных связей действию протеаз.
Повышение температуры (до 90 °С) и увеличение продолжительности нагревания приводит к гидротермическому распаду тропоколлагена на составляющие его макромолекулу пептиды в результате разрушения водородных связей между ними. Этот продукт дезагрегации коллагена — глютин — интенсивно набухает в воде и при 40 °С переходит в раствор, понижение температуры которого сопровождается образованием студней. Глютин легко переваривается протеолитическими ферментами. Дальнейшее нагревание при повышенных температурах приводит к гидролизу пептидных связей, к образованию низкомолекулярных продуктов — глютоз (желатоз). При этом не исключена возможность их взаимодействия с образованием новых соединений. Наличие глютоз понижает гидратацию системы и негативно сказывается на студнеобразовании (уменьшается прочность студней). Таким образом, характер изменения коллагена при тепловой обработке мясного сырья может существенно влиять на качество готовых изделий — их консистенцию, водосвязывающую способность, переваримость коллагена ферментами желудочно-кишечного тракта.
В состав эластиновых волокон входит фибриллярный белок эластин. Полипептидные цепи эластина сформированы из молекул проэластина, имеющего молекулярную массу 72 000 и содержащего 800 аминокислотных остатков. Эластиновые волокна построены из сферических молекул. Аминокислотный состав этого белка отличается высоким содержанием глицина, аланина, лизина, отсутствием триптофана и цистина, малым количеством метионина. Содержащиеся только в эластине специфические аминокислоты — десмозин и изодесмозин — участвуют в образовании поперечных связей.
Эластин характеризуется высокой устойчивостью к действию кислот и щелочей. В отличие от коллагена он не изменяется при нагревании. Эластин не переваривается трипсином и химотрипсином, но медленно гидролизуется пепсином при pH 2,0. Продуцируемая поджелудочной железой эластаза и также растительные ферменты — фицин, папаин и бромеллин— вызывают протеолиз эластина.
На долю межклеточного основного вещества приходится до 30% сухой массы соединительной ткани. В его состав входят протеогликаны — полисахариды, ковалентно связанные с белками. Содержание в них углеводов может достигать 95%. Полисахаридная группа протеогликанов — глюкозоаминоглика- ны — содержит глюкозамин или галактозамин. Наиболее распространенным полисахаридом является гиалуроновая кислота, молекулярная масса которой 105—107. В зависимости от структуры полипептидной цепи протеогликаны могут связываться с коллагеном. Протеогликаны являются поливалентными анионами, которые прочно связывают катионы. Наличие катионов Са2+ способствует их агрегации. Вследствие особенностей расположения углеводно-белковые цепи занимают большое пространство, заполненное молекулами воды. Состав про- теогликанов изменяется в зависимости от возраста животных, что отражается на структурно-механических свойствах соединительной ткани, и их изменении под воздействием внешних факторов.

