Вся информация о строении и функционировании любого живого организма содержится в закодированном виде в его генетическом материале, основу которого составляет дезоксирибонуклеиновая кислота (ДНК). ДНК большинства организмов – это длинная двухцепочечная полимерная молекула. Последовательность мономерных единиц (дезоксирибонуклеотидов) в одной ее цепи соответствует (комплементарна) последовательности дезоксирибонуклеотидов в другой. Принцип комплементарности обеспечивает идентичность новосинтезированных молекул ДНК, образующихся при их удвоении (репликации), исходным молекулам. Индивидуальными генетическими элементами со строго специфичной нуклеотидной последовательностью, кодирующими определенные продукты, являются гены. Одни из них кодируют белки, другие – только молекулы РНК. Информация, содержащаяся в генах, которые кодируют белки (структурных генах), расшифровывается в ходе двух последовательных процессов: синтеза РНК (транскрипции) и синтеза белка (трансляции). Сначала на определенном участке ДНК как на матрице синтезируется матричная РНК (мРНК). Затем в ходе согласованной работы многокомпонентной системы при участии транспортных РНК (тРНК), мРНК, ферментов и различных белковых факторов осуществляется синтез белковой молекулы. Все эти процессы обеспечивают правильный перевод зашифрованной в ДНК генетической информации с языка нуклеотидов на язык аминокислот. Аминокислотная последовательность белковой молекулы однозначно задает ее структуру и функции.
Для получения ценных биотехнологических продуктов используют гены самых разнообразных организмов. Чтобы лучше понять, как работают биотехнологические системы, рассмотрим строение молекулы ДНК и процессы репликации, транскрипции и трансляции.
СТРУКТУРА ДНК
Первые данные о химических свойствах ДНК появились в 1868 г. К началу 40-х годов XX в. было установлено, что молекула ДНК – это линейный полимер. Его мономерными единицами являются нуклеотиды, состоящие из азотистого основания, пятиуглеродного сахара (пентозы) и фосфатной группы (рис. 3.1, А). Фосфатная группа присоединена к 5'-атому углерода моносахаридного остатка, а органическое основание – к 1'-атому. Основания в ДНК бывают двух типов: пуриновые [аденин (А) и гуанин (G)] и пиримидиновые] цитозин (С) и тимин (Т)] (рис. 3.1, Б). В ДНК моносахарид представлен 2'-дезоксирибозой, содержащей только одну гидроксильную группу (ОН), а в РНК – рибозой, имеющей две гидроксильные группы. Нуклеотиды соединены друг с другом фосфодиэфирными связями, при этом фосфатная группа 5'-углеродного атома одного нуклеотида связана с З'-ОН-группой дезоксирибозы соседнего нуклеотида (рис. 3.2). На одном конце полинуклеотидной цепи находится З'-ОН-группа (З'-конец), а на другом – 5'-фосфатная группа (5'-конец).
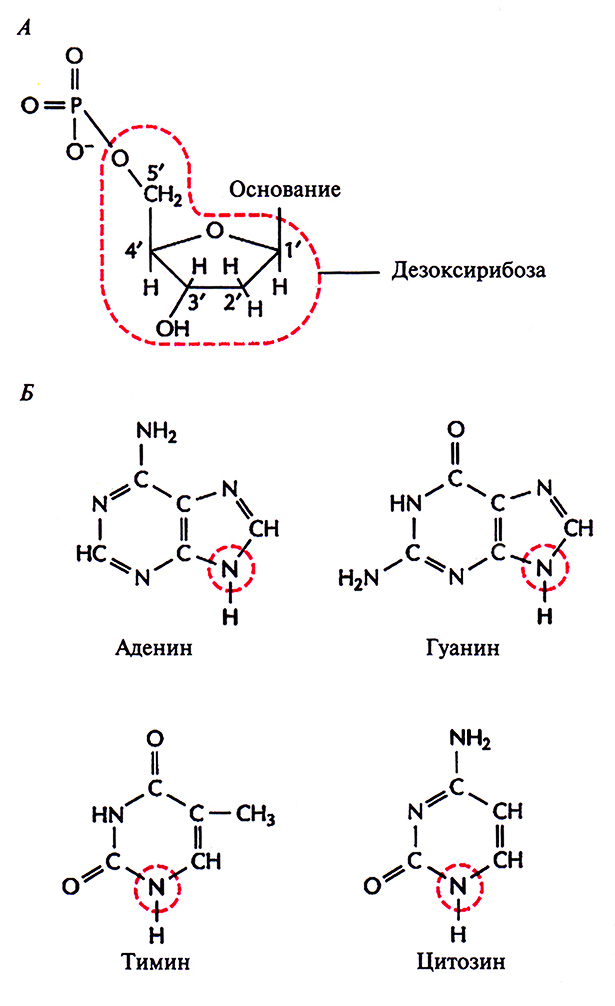
Рис. 3.1. Структурные формулы компонентов ДНК. А. Нуклеотид. Основанием может быть аденин, гуанин, цитозин или тимин. Цветной штриховой линией обведен сахарный остаток (дезоксирибоза): цифрами указаны его углеродные атомы. Б. Основания Цветной штриховой линией обведен атом азота, по которому к основанию присоединяется дезоксириооза.
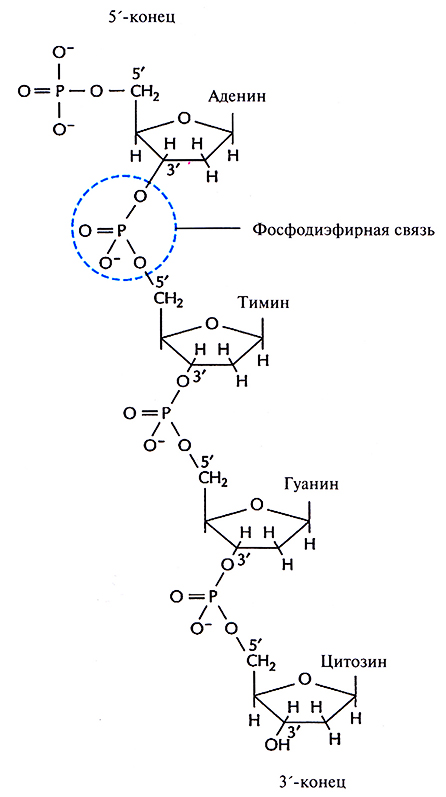
Рис. 3.2. Одна из цепей молекулы ДНК.
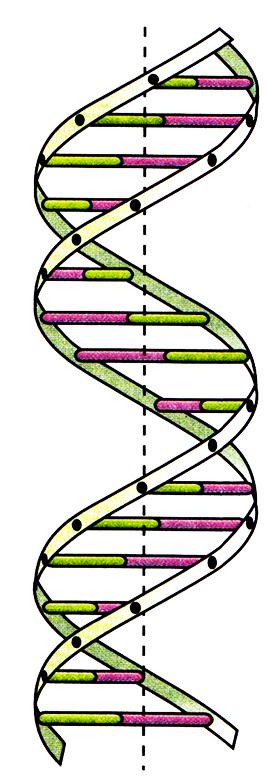
Рис. 3.3. Модель двойной спирали ДНК. Поперечные перекладины – комплементарные пары оснований, «боковины» – сахарофосфатный остов.
В 1953 г. Джеймс Уотсон и Фрэнсис Крик, основываясь на данных рентгеноструктурного анализа кристаллов ДНК, пришли к выводу, что нативная ДНК состоит из двух полимерных цепей, образующих двойную спираль (рис. 3.3). Навитые одна на другую полинуклеотидные цепи удерживаются вместе водородными связями, образующимися между комплементарными основаниями противоположных цепей (рис. 3.4). При этом аденин образует пару только с тимином, а гуанин – с цитозином. Пара оснований А–Т стабилизируется двумя водородными связями, а пара G–С – тремя. Длина двухцепочечной ДНК обычно измеряется числом пар комплементарных нуклеотидов (п.н.). Для молекул ДНК, состоящих из тысяч или миллионов пар нуклеотидов, приняты единицы т.п.н. и м.п.н. соответственно. Например, ДНК хромосомы 1 человека представляет собой одну двойную спираль длиной 263 м.п.н.
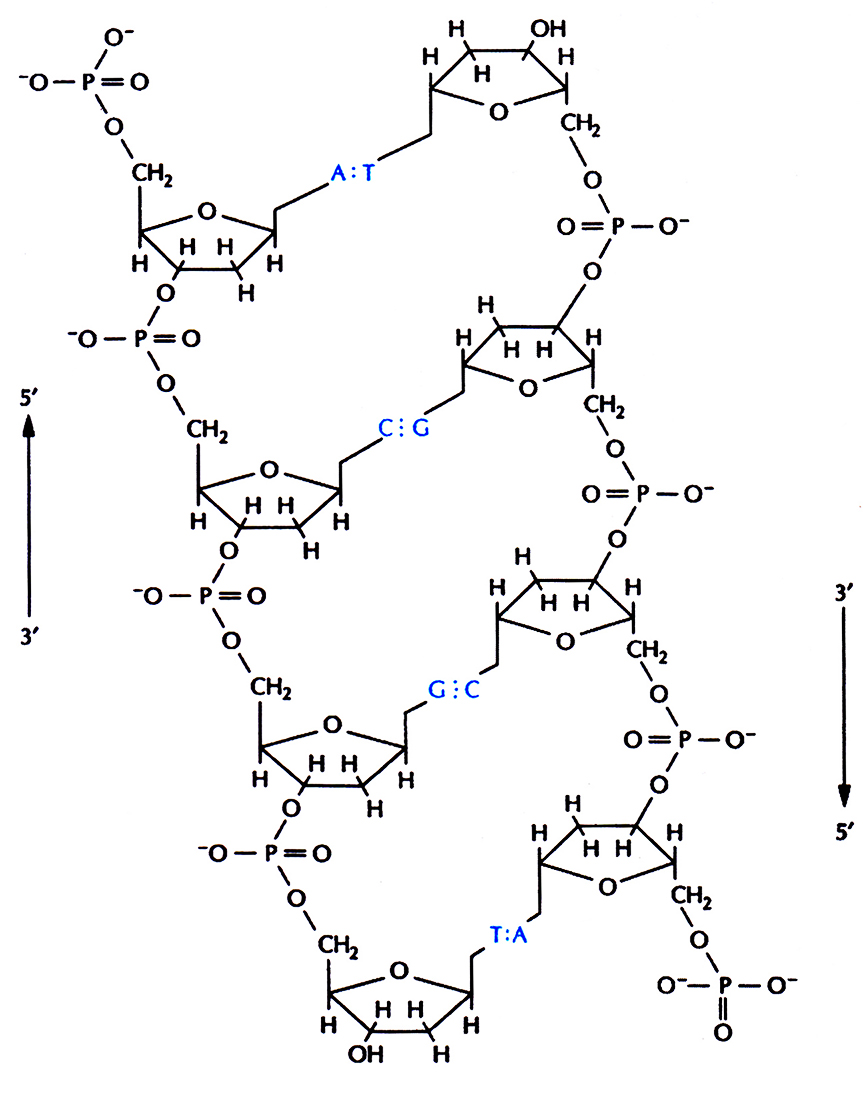
Рис. 3.4. Фрагмент двухцепочечной ДНК.
Сахарофосфатный остов молекулы, который состоит из фосфатных групп и дезоксирибозных остатков, соединенных 5'–З'-фосфодиэфирными связями, образует как бы боковины винтовой лестницы, а пары оснований А–Т и G–С – ее ступеньки (рис. 3.4). Цепи молекулы ДНК антипараллельны: одна из них имеет направление 3'→5', другая 5'→3'. В соответствии с принципом комплементарное™, если в одной из цепей имеется нуклеотидная последовательность 5'-TAGGCAT-3', то в комплементарной цепи в этом месте должна находиться последовательность 3'-ATCCGTA-5'. В этом случае двухцепочечная форма будет выглядеть следующим образом:
5'-TAGGCAT-3'
3 '-ATCCGTA-5'.
В такой записи 5'-конец верхней цепи всегда располагают слева, а 3'-конец – справа.
Носитель генетической информации должен удовлетворять двум основным требованиям: воспроизводиться (реплицироваться) с высокой точностью и детерминировать (кодировать) синтезбелковых молекул. Модель ДНК Уотсона–Крика полностью отвечает этим требованиям. Во-первых, согласно принципу комплементарности, каждая цепь ДНК может служить матрицей для образования новой комплементарной цепи. Следовательно, после одного раунда репликации образуются две дочерние молекулы, каждая из которых имеет такую же нуклеотидную последовательность, как исходная молекула ДНК. Во-вторых, нуклеотидная последовательность структурного гена однозначно задает аминокислотную последовательность кодируемого ею белка.
РЕПЛИКАЦИЯ
Согласно модели Уотсона–Крика, каждая цепь ДНК служит матрицей при синтезе новой комплементарной цепи, а последовательность оснований в синтезируемой (растущей) цепи задается последовательностью комплементарных оснований цепи-матрицы. Каждая мономерная единица, присоединяющаяся к растущей цепи, находится в форме дезоксирибонуклеозид-5'-трифосфата (рис. 3.5); фосфатная группа, связанная с 5'-углеродным атомом дезоксирибозы, обозначается буквой α, к ней присоединены β-фосфат и далее – ץ-фосфат. В ходе репликации β- и ץ-фосфатные группы отщепляются в виде пирофосфата, а α-фосфатная группа связывается с 3'-ОН-группой последнего нуклеотида растущей цепи (рис. 3.6). Синтез ДНК как у про-, так и у эукариот осуществляется при участии множества разных ферментов. Основную роль играет ДНК-полимераза, которая последовательно присоединяет новые звенья к растущей полинуклеотидной цепи в соответствии с принципом комплиментарное и катализирует образование фосфодиэфирных связей.
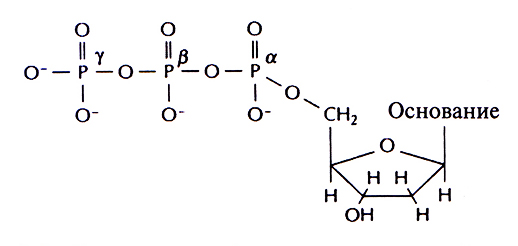
Рис. 3.5. Структурная формула дезоксирибонуклеозидтрифосфата. Фосфатные группы обозначаются буквами, β, и ץ. а-Фосфат связан с 5'-атомом углерода дезоксирибозы и при репликации участвует в образовании фосфодиэфирной связи; β- и ץ-фосфатные группы отщепляются в виде пирофосфата.
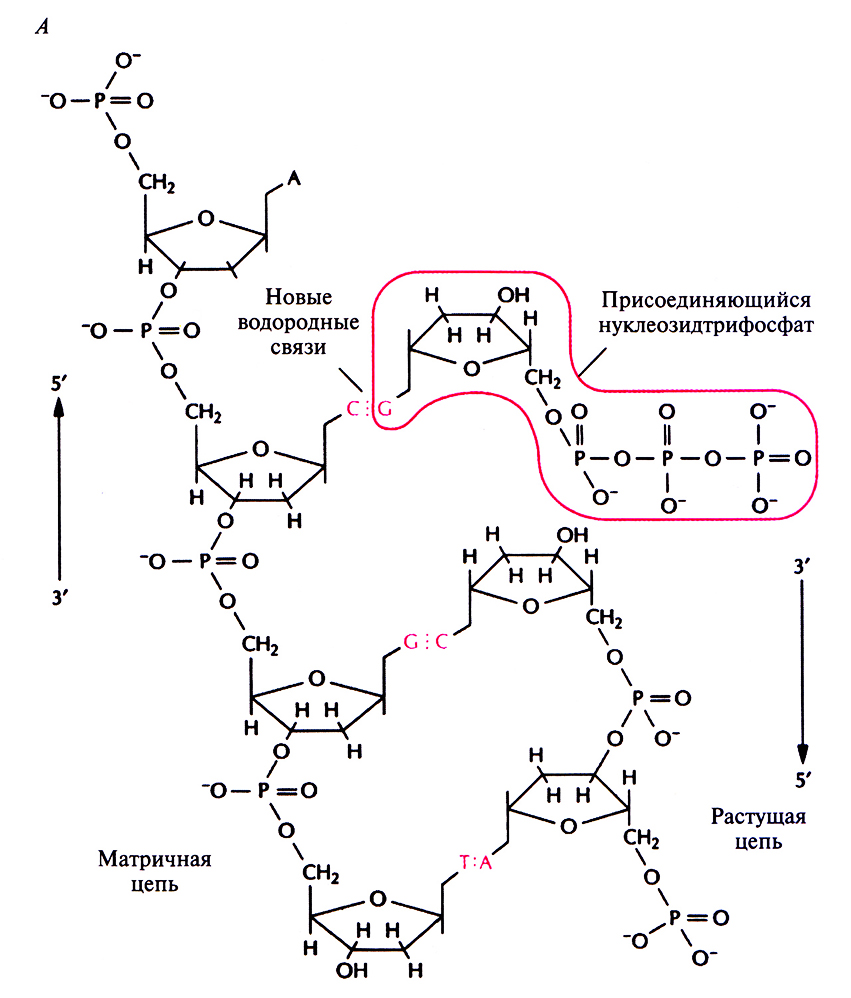
Рис. 3.6. Репликация ДНК. А. Спаривание очередного дезоксирибонуклеозидтрифосфата с комплементарным основанием ДНК-матрицы.
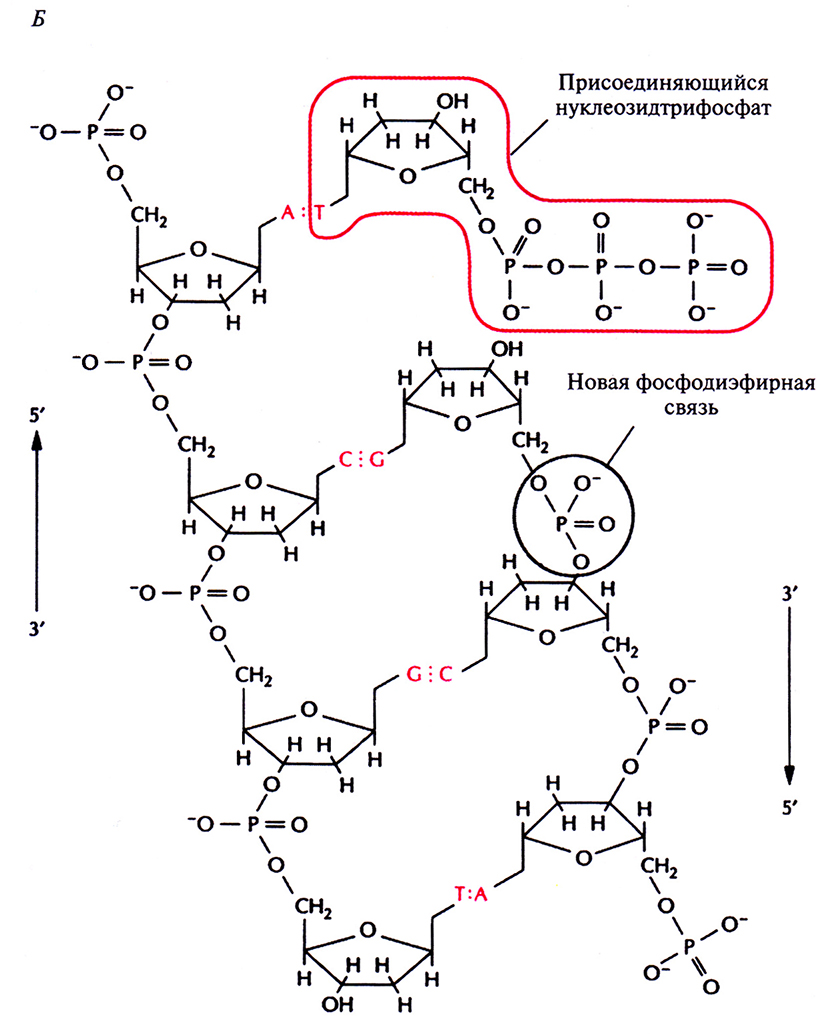
Рис. 3.6. Б. Между α-фосфатной группой присоединяемого нуклеотида и З'-гидроксильной группой растущей цепи образуется фосфодиэфирная связь. К комплементарному спариванию готов следующий дезоксирибонуклеозидтрифосфгт
У бактерий репликация ДНК начинается в особой точке молекулы, которая называется точкой начала (или сайтом иниципции) репликации (ori, от англ. origin). В ДНК эукариот имеется несколько таких сайтов, и репликация может начинаться в каждом из них. Образующиеся при этом сегменты эукариотической ДНК сшиваются друг с другом с помощью особых ферментов. Кроме того, у эукариот есть специальный фермент теломераза, который достраивает концы (теломеры) хромосом.
РАСШИФРОВКА ГЕНЕТИЧЕСКОЙ ИНФОРМАЦИИ: РНК И БЕЛОК
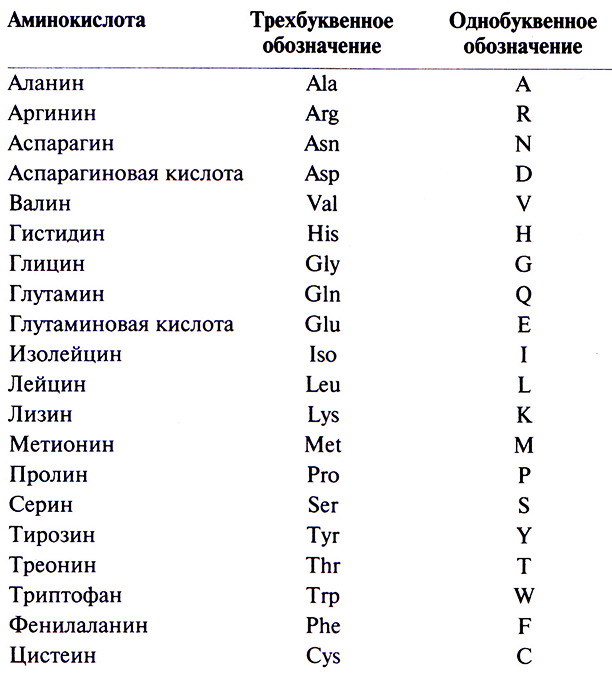
Подавляющее большинство генов содержит в закодированном виде информацию о синтезе белков. Белки – это биологические молекулы, участвующие практически во всех процессах, протекающих в живых системах. Они служат катализаторами разнообразных биохимических реакций, осуществляют транспорт веществ внутри клеток и между клетками, регулируют проницаемость клеточных мембран, из них строятся различные структурные элементы. Белки участвуют в осуществлении двигательных функций, обеспечивают защиту от инфекций и токсинов, регулируют синтез остальных генных продуктов. Основной структурной единицей белков являются аминокислоты. Все аминокислоты имеют сходное химическое строение. К центральному атому углерода (а-углерод) присоединены атом водорода (Н), аминогруппа (NH3+), карбоксильная группа (СОО–) и R-грyппа (боковая цепь) (рис. 3.7, А). Существует 20 разных боковых групп и соответственно 20 аминокислот. Например, в аминокислоте аланине R-группой является метальная группа (СН3). В табл. 3.1 даны одно- и трехбуквенные обозначения аминокислот. Соединяясь друг с другом пептидными связями, аминокислоты образуют полипептидную цепь. Пептидная связь образуется между карбоксильной группой одной аминокислоты и аминогруппой другой (рис. 3.7, Б). Первая аминокислота белковой молекулы имеет свободную аминогруппу (N-конец), а последняя – свободную карбоксильную группу (С-конец).
Длина белковых молекул варьирует от 40 до более 1000 аминокислотных остатков, при этом в зависимости от их последовательности и от аминокислотного состава молекулы белков принимают разную форму (конфигурацию, конформацию). Многие функционально активные белки состоят из двух и более полипептидных цепей (субъединиц), как идентичных, так и несколько различающихся. Кроме того, многие белки, выполняющие ключевые функции, представляют собой сложные белковые комплексы, состоящие из множества разных субъединиц.
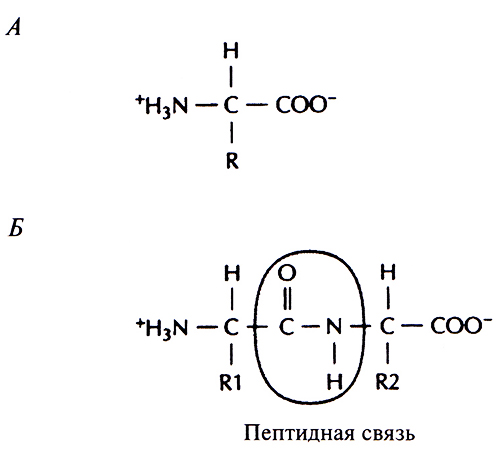
Рис. 3.7. Обобщенная структурная формула аминокислоты и образование пептидной связи. А. Аминокислота. R – боковая группа. Б. Образование пептидной связи между двумя аминокислотными остатками с боковыми группами R1 и R2.
Таблица 3.1. Аминокислоты и их обозначения
Важным «передаточным звеном» при переводе генетической информации с языка нуклеотидов на язык аминокислот являются рибонуклеиновые кислоты (РНК), которые синтезируются на определенных участках ДНК как на матрицах в соответствии с их нуклеотидной последовательностью. РНК – это линейная полинуклеотидная молекула, отличающаяся от ДНК в двух отношениях. Во-первых, моносахаридом в РНК является рибоза, содержащая не одну, а две гидроксильные группы; они связаны с 2'- и 3'-атомами углерода. Во-вторых, одним из четырех оснований в РНК является урацил (U), занимающий место тимина. Большинство молекул РНК одноцепочечные, хотя часто в них имеются взаимнокомплементарные участки, образующие двух-цепочечные структуры – «шпильки» (рис. 3.8). Спаривание оснований происходит таким же образом, как и в ДНК, за исключением того, что вместо пары А–Т образуются A–U.
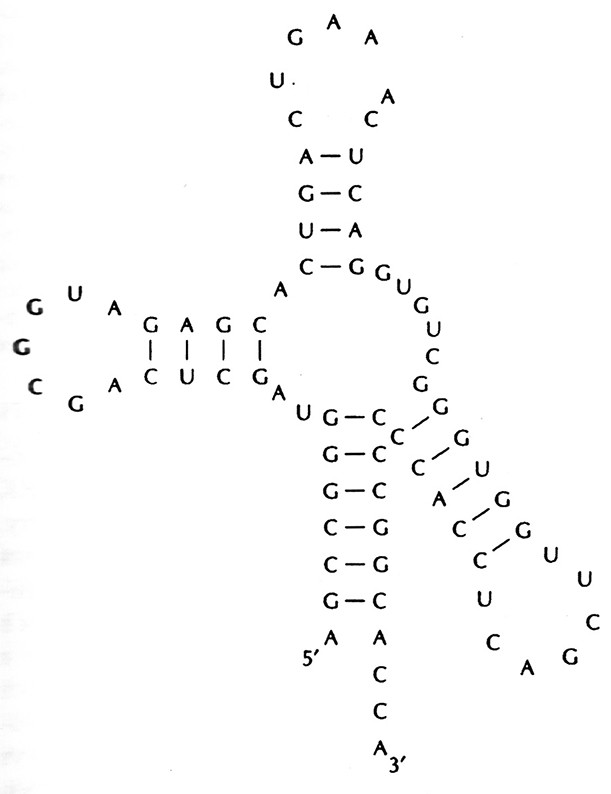
Рис. 3.8. Вторичная структура гипотетической молекулы РНК. Комплементарные основания соединены между собой водородными связями. Сахарофосфатный остов не изображен.
Существуют три основных типа РНК: информационная (мРНК), рибосомная (рРНК) и транспортная (тРНК). Все они играют важную роль в процессе расшифровки генетической информации. Синтез РНК на ДНК-матрице называется транскрипцией. У большинства прокариот транскрипция всех РНК осуществляется с помощью одной и той же РНК-полимеразы. У эукариот мРНК, рРНК и тРНК транскрибируются разными РНК-полимеразами.
Транскрипция во многом сходна с репликацией. Матрицей при синтезе РНК служит определенный участок одной из цепей ДНК. РНК-полимераза копирует этот участок, последовательно соединяя друг с другом с помощью 3'–5'-фосфодиэфирных связей рибонуклеотиды в соответствии с правилом комплементарности (рис. 3.9). В ходе транскрипции новосинтезированная молекула РНК отсоединяется от ДНК, и двойная спираль ДНК восстанавливается. Чтобы обеспечить транскрипцию только отдельных сегментов ДНК, должны существовать некие сигнальные последовательности, указывающие, где начинается (инициируется) транскрипция и где она останавливается (терминируется). Сигнал инициации обычно располагается перед кодирующей последовательностью, а сигнал терминации – вслед за ней. Участок ДНК, предшествующий транскрибируемому гену, называется 5'-фланкирующей последовательностью, а расположенный за ним – 3'-фланкирующей.
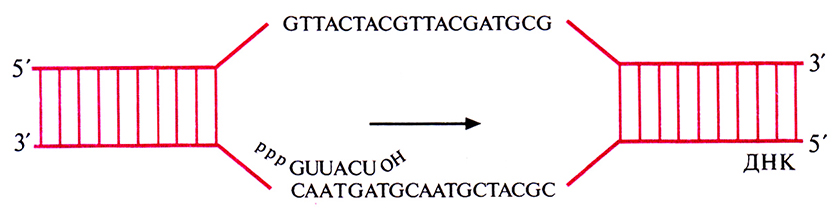
Рис. 3.9. Схематическое изображение транскрипции. Стрелкой указано ее направление.
С молекулярной точки зрения ген представляет собой специфическую нуклеотидную последовательность, транскрибируемую в РНК. Подавляющее большинство транскрибируемых последовательностей ДНК составляют так называемые структурные гены, на которых синтезируются мРНК. Конечным продуктом структурного гена является белок. У прокариот структурный ген представляет собой непрерывный участок молекулы ДНК. Транскрипция начинается со связывания РНК-полимеразы с промотором, и далее последовательно копируется весь структурный ген (кодирующая область) от первого нуклеотида до последнего с образованием функциональной мРНК (рис. 3.10). У эукариот большинство структурных генов состоит из нескольких дискретных кодирующих областей (экзонов), разделенных некодирующими областями (интронами). По завершении транскрипции эукариотического структурного гена интроны вырезаются из первичного продукта транскрипции с помощью ферментов, а экзоны сшиваются друг с другом «торец в торец» (сплайсинг) с образованием функциональной мРНК (рис. 3.11 и 3.12). Обычно длина экзонов составляет от 150 до 200 нуклеотидов, а длина интронов варьирует от 40 до 10 000 нуклеотидов. Очень немногие эукариотические структурные гены вообще не имеют интронов. Иногда сплайсинг мРНК может проходить по альтернативному варианту. Например, в одной ткани функциональная мРНК может образовываться в результате соединения всех экзонов первичного транскрипта, а в другой какой-то экзон будет вырезан вместе с фланкирующими его интронами и образуется другая функциональная мРНК. Благодаря альтернативному сплайсингу в разных тканях могут образовываться разные продукты одного и того же структурного гена (рис. 3.13).
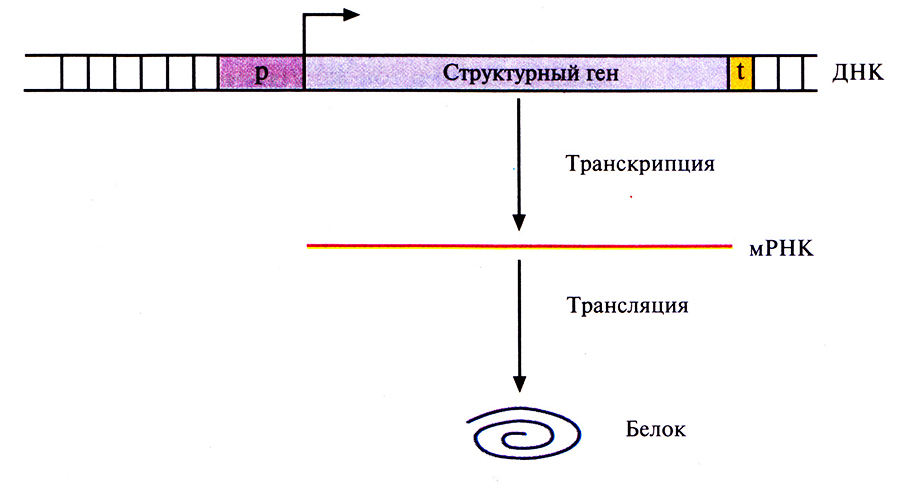
Рис. 3.10. Схематическое изображение прокариотического структурного гена. Указаны промотор (р), сайт инициции транскрипции и ее направление (горизонтальная стрелка), область терминации транскрипции, узнаваемая РНК-полимеразой (t). Сначала на ДНК как на матрице синтезируется мРНК (транскрипция), а затем осуществляется синтез белковой цепи (трансляция).
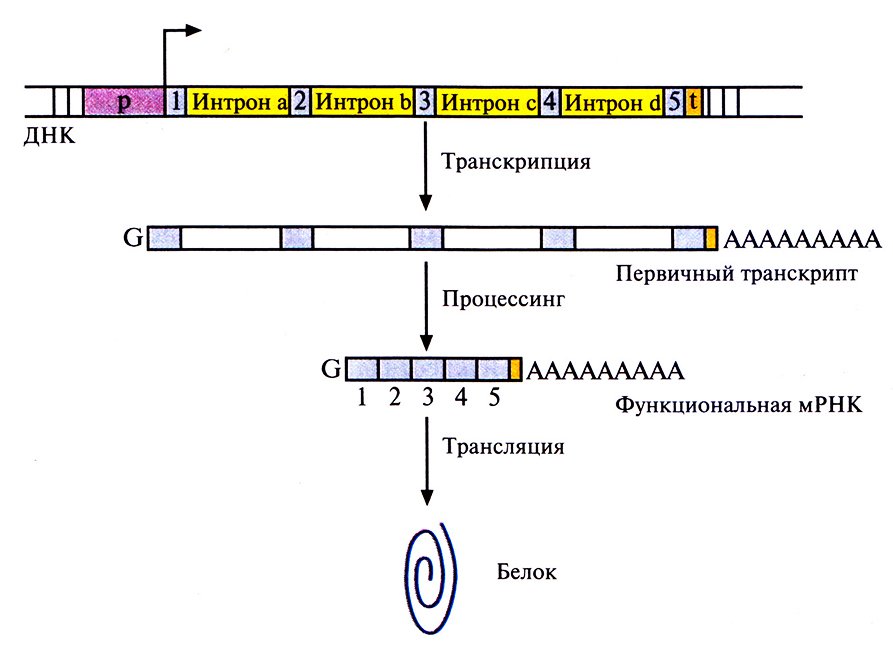
Рис. 3.11. Схематическое изображение эукариотического структурного гена. Указаны промотор (р), сайт инициации транскрипции и ее направление (горизонтальная стрелка), область терминации транскрипции, узнаваемая РНК полимеразой (t). 1–5 – экзоны, a–d – интроны. Первичный транскрипт содержит poly (А)-«хвост» на 3-конце и метилированный нуклеотид G («кэп») на 5'-конце. После транскрипции интроны из первичного транскрипта вырезаются (процессинг), и на образовавшейся функциональной РНК синтезируется белковая молекула (трансляция)
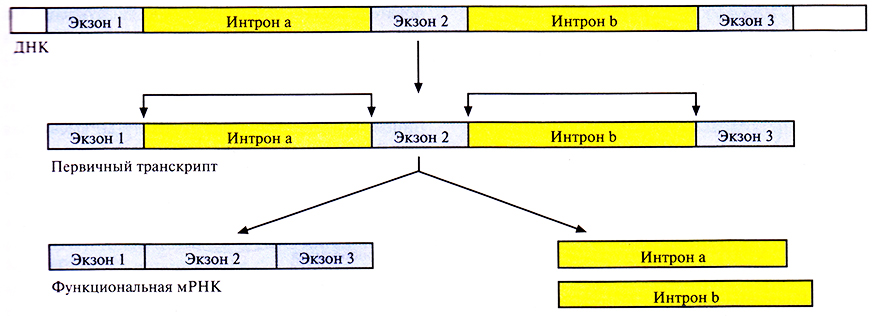
Рис. 3.12. Сплайсинг первичного транскрипта у эукариот. Угловыми стрелками указаны места соединения экзонов 1, 2 и 3 после удаления интронов а и b.
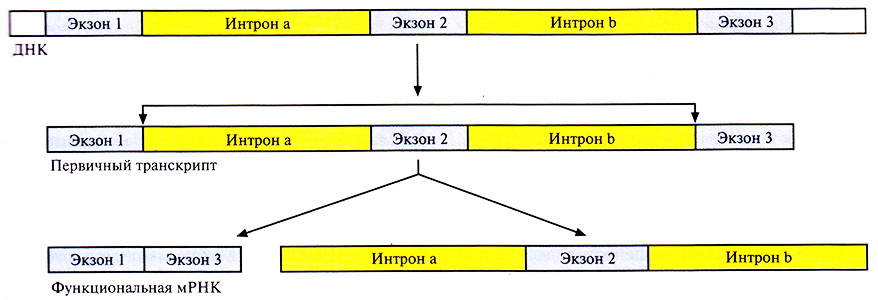
Рис. 3.13. Альтернативный сплайсинг первичного транскрипта у эукариот. Стрелками указаны места соединения экзонов после удаления интронов. Экзон 2, фланкируемый интронами 1 и 2, вырезается из первичного транскрипта, а экзоны 1 и 3 соединяются с образованием функционально активной мРНК.
В активно функционирующей клетке примерно 3–5% суммарной РНК приходится на долю мРНК, 90% – на долю рРНК и 4% – на долю тРНК. мРНК может быть представлена десятками различных типов молекул, а рРНК – всего двумя типами. Более крупная рРНК образует с белками рибонуклеопротеидный комплекс, называемый большой рибосомной субъединицей, а рРНК меньшего размера – комплекс, называемый малой рибосомной субъединицей. Во время синтеза белков субъединицы объединяются с образованием рибосомы. У эукариот обе рибосомные субъединицы крупнее, чем у прокариот.
Помимо тысяч рибосом, в клетке, активно синтезирующей белки, содержатся до 60 различных видов тРНК. тРНК – это линейная одноцепочечная молекула длиной от 75 до 93 нуклеотидов. В ней имеется несколько взаимнокомплементарных участков, спаривающихся между собой (рис. 3.8), а вся молекула укладывается в пространстве с образованием структуры, напоминающей букву L (рис. 3.14). С помощью специфических ферментов (аминоацил-тРНК–синтетаз) к 3'-концу тРНК присоединяется соответствующая аминокислота. Так, фермент аргинил-тРНК–синтетаза присоединяет к молекуле тРНКArg аминокислоту аргинин. Для каждой из двадцати аминокислот, из которых состоят все белки, существует по крайней мере одна специфическая тРНК. На другом конце молекулы тРНК расположена последовательность из трех нуклеотидов, которая называется антикодоном. Она распознает специфический кодон в мРНК и определяет, какая именно аминокислота будет присоединена к растущей полипептидной цепи.
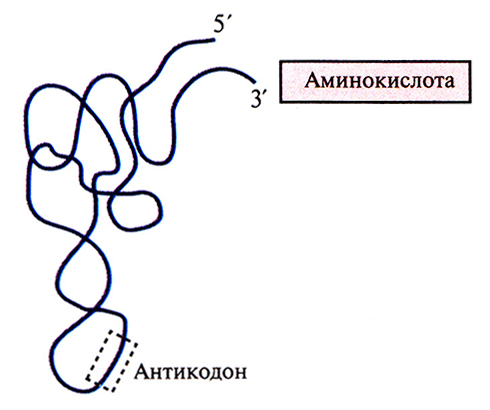
Рис. 3.14. Конформация тРНК, «нагруженной» аминокислотой. Штриховой прямоугольник – антикодон.
ТРАНСЛЯЦИЯ
Трансляция осуществляется при участии мРНК, разных тРНК, «нагруженных» соответствующими аминокислотами, рибосом и множества белковых факторов, обеспечивающих инициацию, элонгацию и терминацию синтеза полипептидной цепи. Трансляция в прокариотических клетках инициируется формилметиониновой тРНК, которая так и называется – инициаторная тРНК. При участии белковых факторов антикодон 3'-UAC-5' инициаторной тРНК,Меt (Met-модифицированный метионин, аминогруппа которого формилирована) связывается с кодоном 5'-AUG-3' мРНК, образующей комплекс с малой рибосомной субъединицей. Никакая другая тРНК соединиться с этим комплексом не может. В свою очередь связывание мРНК с малой рибосомной субъединицей осуществляется посредством образования нуклеотидных пар между последовательностью примерно из восьми нуклеотидов (последовательность Шайна–Дальгарно), которая расположена вблизи 5'-конца мРНК, и комплементарной 3'-концевой последовательностью рРНК, связанной с малой рибосомной субъединицей. К комплексу fMet-тРНKfMet-M РНК-малая субъединица присоединяется большая субъединица, и образуется инициаторный комплекс (комплекс инициации) (рис. 3.15).
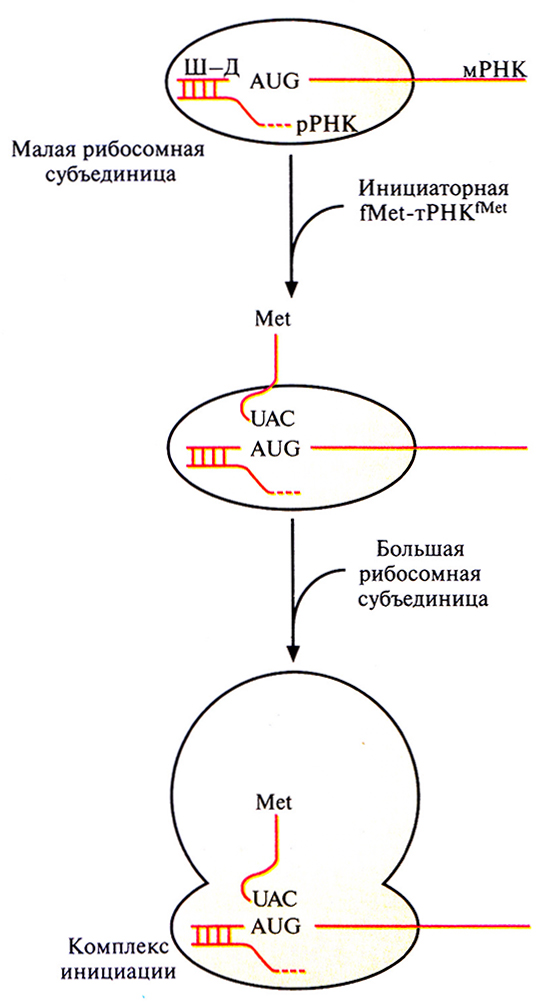
Рис. 3.15. Инициация трансляции в прокариотической клетке. Последовательность Шайна–Дальгарно (Ш–Д), находящаяся вблизи 5'-конца мРНК, связывается с комплементарной 3'-концевой последовательностью рРНК, образующей комплекс с малой рибосомной субъединицей. Антикодон (UAC) инициаторной fMet-тРНKfMet спаривается со старткодоном (AUG) мРНК. К образовавшемуся комплексу присоединяется большая рибосомная субъединица, и образуется комплекс инициации. Аминогруппа метионина, связанного с инициаторной тРНК, формилирована (СНО) (на рисунке не изображено). После трансляции формилметионин отщепляется от белковой цепи.
У эукариот трансляция инициируется связыванием специфической «нагруженной» инициаторной тРНК (Met-TPHKMet) и факторов инициации с малой рибосомной субъединицей. Затем мРНК присоединяется своим 5'-концом к комплексу тРНК–малая рибосомная субъединица, и комплекс продвигается по мРНК до старт-кодона (AUG). Далее антикодон UAC инициаторной Met-TPHKMet спаривается с кодоном AUG мРНК. К комплексу присоединяется большая рибосомная субъединица, и образуется инициаторный комплекс (рис. 3.16.)
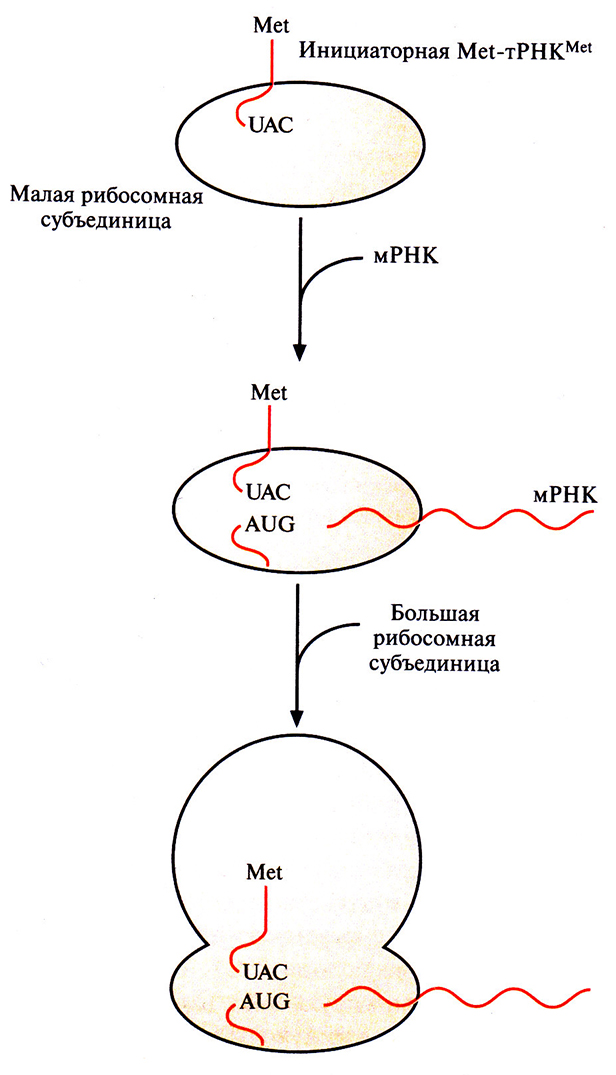
Рис. 3.16. Инициация трансляции в эукариотической клетке. Малая рибосомная субъединица связывается с инициаторной тРНК, «нагруженной» метионином (Met-TPHKMet), комплекс продвигается по мРНК, пока антикодон UAC инициаторной тРНК не спарится со старт-кодоном AUG мРНК. Далее к комплексу мРНК– тРНК–малая субъединица присоединяется большая субъединица и образуется комплекс инициации.
Этапы элонгации и терминации у про- и эукариот во многом сходны. Процесс элонгации включает образование пептидных связей между соседними аминокислотами, при этом очередность присоединяемых аминокислот определяется очередностью кодонов в мРНК (рис. 3.17). Рассмотрим процесс более подробно. После образования инициаторного комплекса кодон в молекуле мРНК, следующий за кодоном AUG, спаривается с комплементарным ему антикодоном соответствующей тРНК, определяя таким образом, какая из нагруженных тРНК присоединится к рибосоме (ненагруженные тРНК не связываются с рибосомами). Если вторым триплетом в мРНК оказывается CUG, то следующей к рибосомному комплексу присоединяется несущая лейцин тРНК с антикодоном 3'-GAC-5'. Когда эта тРНК оказывается на месте, между карбоксильной группой мегионина и аминогруппой лейцина с помощью ферментативной активности, присущей большой субъединице, образуется пептидная связь, при этом лейцин остается связанным со своей тРНК, а метионин отсоединяется от инициаторной тРНК, и последняя отделяется от рибосомы. Комплекс метионин–лейцин–тРНКLeu–мРНК «протягивается» через рибосому (транслокация), так что следующий кодон мРНК может связаться с нагруженной тРНК, несущей соответствующий антикодон. Если третьим кодоном мРНК является UUU, то следующей аминокислотой в растущей полипептидной цепи будет фенилаланин; его доставит к рибосоме тРНК с антикодоном AAA. Когда эта тРНК окажется на месте, между карбоксильной группой лейцина и аминогруппой фенилаланина образуется пептидная связь тРНКLeu отделится от рибосомы, произойдет транслокация пептидил-тРНКPhe (тРНК с присоединенной к ней растущей полипептидной цепью), и следующий кодон мРНК сможет связаться с антикодоном соответствующей нагруженной тРНК.
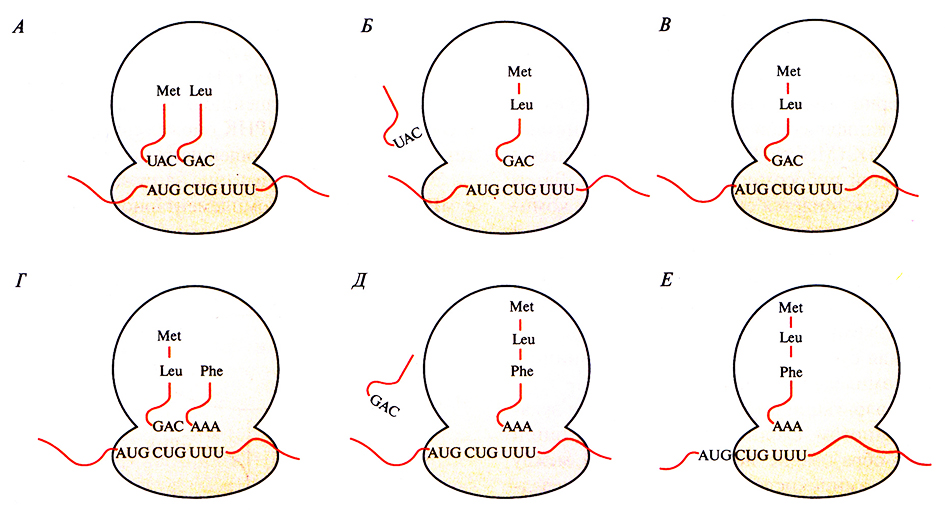
Рис. 3.17. Элонгация полипептидной цепи. А. Второй кодон (CUG) в мРНК связывается с антиколоном (GAC) Leu-тРНКLeu. Б. Метионин образует пептидную связь с лейцином, доставленным тРНКLeu, освободившаяся от аминокислоты инициаторная тРНК отсоединяется. В. Транслокация комплекса пептцдил-тРНК–мРНК с экспонированием следующего кодона (UUU). Г. Третий кодон (UUU) спаривается с антикодоном AAA Phe-TPHKphe. Д Лейцин образует пептидную связь с фенилаланином, доставленным тРНКPhe, освободившаяся от аминокислоты тРНКPhe отсоединяется от рибосомы. Е. Транслокация комплекса пептидил-тРНК–мРНК с экспонированием следующего кодона, и т.д.
Эти события – связывание нагруженной тРНК с мРНК благодаря комплементарному спариванию кодона с антикодоном, образование пептидной связи, отсоединение «разгруженной» тРНК, транслокация – продолжаются до тех пор, пока не соединятся друг с другом все аминокислоты, закодированные в мРНК. Трансляция происходит в направлении 5'–3' со скоростью примерно 15 аминокислот в секунду. Когда 5'-конец мРНК высвобождается из рибосомного комплекса, он может связаться с другим таким же комплексом, так что одна молекула мРНК может одновременно транслироваться множеством рибосом.
Элонгация продолжается до тех пор, пока рибосома не дойдет до кодона UAA, UAG или UGA (стоп-кодон, терминирующий кодон) (рис. 3.18). В норме в клетках отсутствуют тРНК с антикодонами, комплементарными сигналам терминации. Их узнают белковые факторы освобождения (терминации). При связывании фактора освобождения с рибосомой происходит гидролиз связи между последней тРНК и полипептидом, свободная тРНК, полипептидная цепь и мРНК отсоединяются от рибосомы. Рибосома диссоциирует на субъединицы, которые могут вновь участвовать в трансляции.
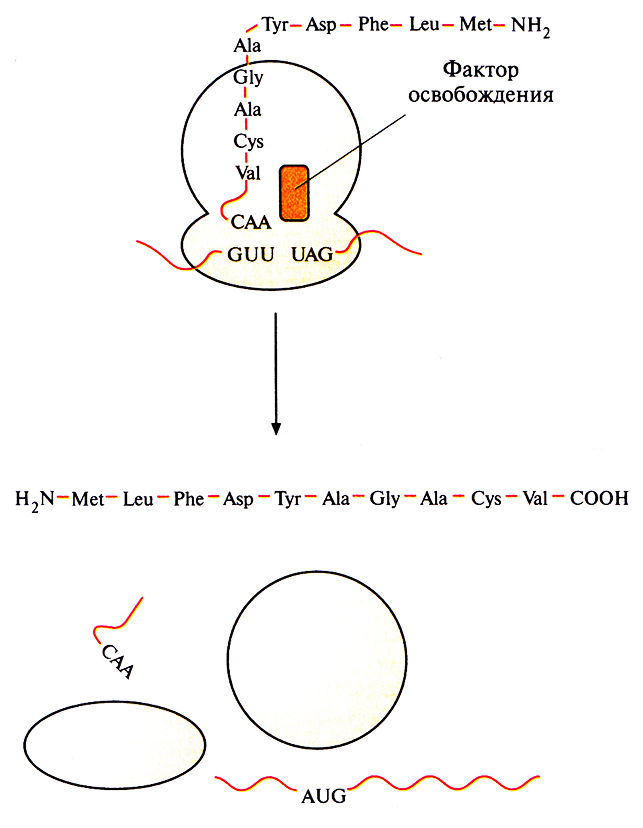
Рис. 3.18. Терминация трансляции. Co стоп-кодоном (UAG) связывается фактор освобождения, и трансляция завершается. Химическая связь между последней тРНК и полипептидной цепью разрывается, свободная тРНК, мРНК и готовая белковая цепь отсоединяются от рибосомы, и последняя диссоциирует на субъединицы.
После трансляции многие полипептиды подвергаются различным модификациям. У большинства из них отщепляется N-концевой метионин, так что N-концевым остатком становится вторая аминокислота. У эукариот происходит так называемый процессинг некоторых белков, когда полипептидная цепь расщепляется в определенных сайтах с образованием более коротких белковых молекул со специфическими функциями. В некоторых случаях, особенно в эукариотических клетках, к определенным аминокислотам ферментативным путем присоединяются фосфатные группы, липиды, углеводы или другие низкомолекулярные соединения. В результате этих химических модификаций образуются белки, выполняющие в клетке специфические функции.
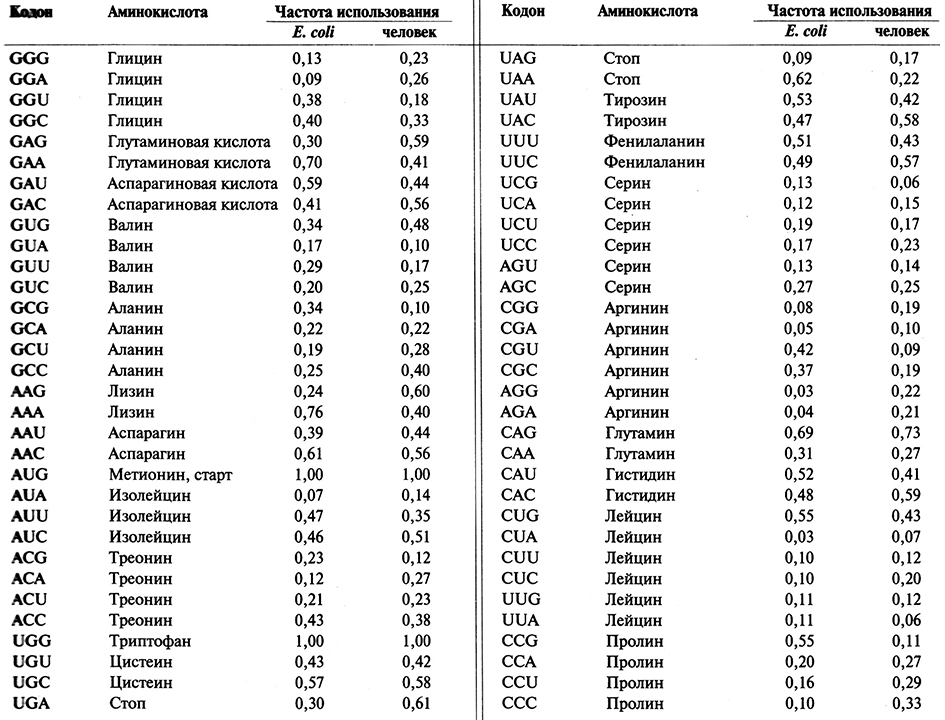
Генетический словарь состоит из 64 кодонов. Три из них – это стоп-кодоны, а один (AUG) – старт-кодон (табл. 3.2), кодирующий еще и аминокислоту метионин. Когда кодон AT TG находится не на 5'-коние молекулы мРНК, а в ее внутренней области, то он распознается другой тРНК (Met-TPHKMet), к которой присоединен немодифицированный метионин. Аминокислота триптофан кодируется всего одним кодоном (UGG), остальные аминокислоты, из которых состоят белки, – по крайней мере двумя, чаще четырьмя, а иногда и шестью кодонами. Например, для лейцина существует шесть кодонов: UUA, UUG, CUU, CUC, CUA и CUG. Синонимичные кодоны используются различными организмами с разной частотой. Из четырех кодонов для глицина GGA используется в структурных генах человека в 26% случаев, а в Escherichia сой – в 9%. Такая же ситуация наблюдается и для стоп-кодонов. Так, у человека частота использования кодонов UAA, UAG и UGA составляет 0,22, 0,17 и 0,61 соответственно, а у Е. coli – 0,62, 0,09 и 0,30. Несмотря на все эти различия, генетический код у всех организмов, за редким исключением, одинаков.
Таблица 3.2. Генетический код и частота использования разных кодонов в геноме Е. coli и человека
РЕГУЛЯЦИЯ ТРАНСКРИПЦИИ У БАКТЕРИЙ
Все процессы, протекающие в бактериальной клетке, – образование аминокислот, нуклеотидов и других важных метаболитов, репликация, транскрипция, трансляция, катаболизм, высвобождение энергии, реакции на внешние воздействия – требуют участия белков. Однако энергетических ресурсов клетки не хватает для одновременного осуществления транскрипции и трансляции (экспрессии) всех структурных генов. Поэтому постоянно экспрессируются только те гены, которые кодируют белки, поддерживающие основные клеточные функции, а транскрипция остальных структурных генов регулируется. Когда у клетки возникает потребность в каком-то белке (белках), то инициируется (включается) транскрипция соответствующего структурного гена (генов), а когда такая потребность исчезает, транскрипция выключается.
Часто у бактерий белки одного метаболического пути кодируются смежными структурными генами. Нуклеотидная последовательность, в которой закодировано более одного белка, называется опероном. Обычно оперон находится под контролем единственного промотора, и при его транскрипции образуется одна длинная молекула мРНК, кодирующая несколько белков. При трансляции такой мРНК, в которой стоп-кодон последовательности, кодирующей один белок, соседствует со старт-кодоном гена следующего белка, синтезируется набор дискретных белков.
В большинстве структурных генов Е. coli имеются два сайта связывания для РНК-полимеразы. Один из них обычно представляет собой нуклеотидную последовательность
ТАТААТ
АТАТТА
(ТАТА-бокс, или бокс Прибнова), а другой –
TTGAC
AACTG.
ТАТА-бокс и последовательность TTGAC расположены за 10 (область–10) и 35 (область –35) нуклеотидов до сайта инициации транскрипции соответственно (нуклеотид +1) (рис. 3.19). Обычно от участка между ТАТА-боксом и нуклеотидом +1 во многом зависит, будет ли происходить транскрипция данного оперона. В зависимости от способа регуляции транскрипции оперона этот участок называется оператором или активатором.
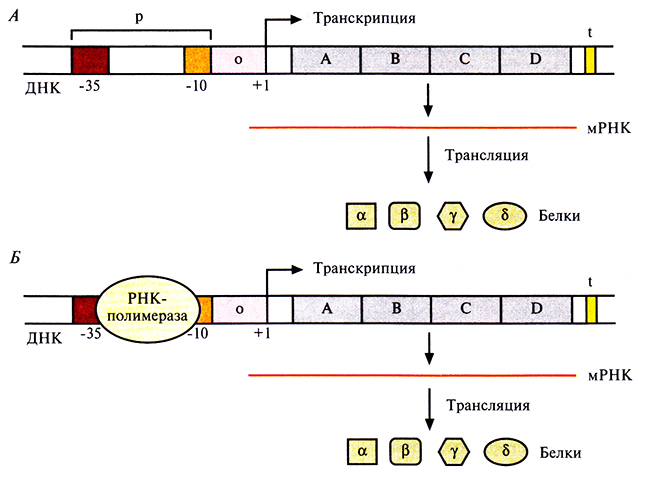
Рис. 3.19. Транскрипция в бактериальной клетке. А. Структурные гены (А, В, С и D) оперона находятся под транскрипционным контролем оператора (о) и промотора (р). РНК-полимераза связывается с участками, находящимися на расстоянии 10 (–10) и 35 (–35) пар оснований от сайта инициации транскрипции (+1). t – Стоп-сигнал, ответственный за остановку транскрипции, α, β, γ и S – белки, продукты генов А, В, С, D. Б. То же, что и на рис. А. но показано связывание РНК-полимеразы с промоторной областью.
Для включения и выключения разных оперонов в ходе эволюции сформировалось множество регуляторных систем. Например, с операторной областью может быть связан регуляторный белок, называемый репрессором; он мешает перемещению РНК-полимеразы вдоль молекулы ДНК, и транскрипция блокируется (рис. 3.20). Однако если с репрессором свяжется некое низкомолекулярное вещество (эффектор), то его конформация изменится таким образом, что его связывание с операторной областью станет невозможным, и транскрипция возобновится. Обычно эффектор разрушается клеточными ферментами. Когда его концентрация снижается, репрессор связывается с операторным участком, и транскрипция вновь прекращается. Операторный участок специфичен для каждого оперона, а эффектор взаимодействует только с определенным репрессором.
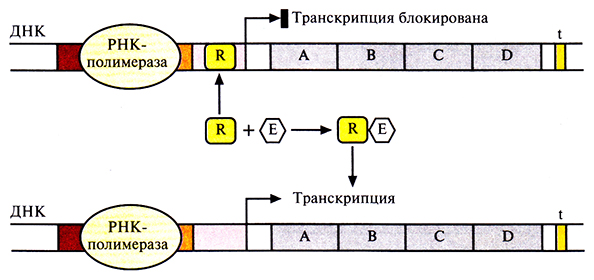
Рис. 3.20. Включение транскрипции бактериального оперона. Репрессор (R) связывается с оператором и блокирует транскрипцию. Связывание эффектора (Е) с репрессором изменяет его конформацию, и он не может связаться с оператором РНК-полимераза беспрепятственно перемещается вдоль молекулы ДНК, осуществляя транскрипцию.
В качестве иллюстрации рассмотрим такой пример. Предположим, что клетка способна метаболизировать определенный сахар. Тогда синтез ферментов, расщепляющих этот сахар, будет бесполезной тратой клеточных ресурсов, если он отсутствует в среде. С другой стороны, если этот сахар имеется в достаточном количестве и является единственным источником углерода, то ферменты, отвечающие за его утилизацию клеткой, становятся совершенно необходимыми. В этом случае сахар действует как эффектор, препятствуя связыванию репрессора с операторным участком и таким образом обеспечивая транскрипцию оперона и синтез ферментов.
При истощении запасов сахара в среде репрессор связывается с операторным участком, и транскрипция оперона прекращается.
Нормальным состоянием других оперонов может быть состояние, при котором осуществляется их транскрипция, поскольку репрессорный белок неактивен. В этом случае специфический эффектор (корепрессор), связываясь с неактивным репрессором, вызывает в нем такие конформационные изменения, которые обеспечивают связывание комплекса с операторным участком, и транскрипция оперона выключается (рис. 3.21). Сам по себе репрессор не способен связываться с оператором, поэтому при уменьшении концентрации корепрессора транскрипция возобновляется.
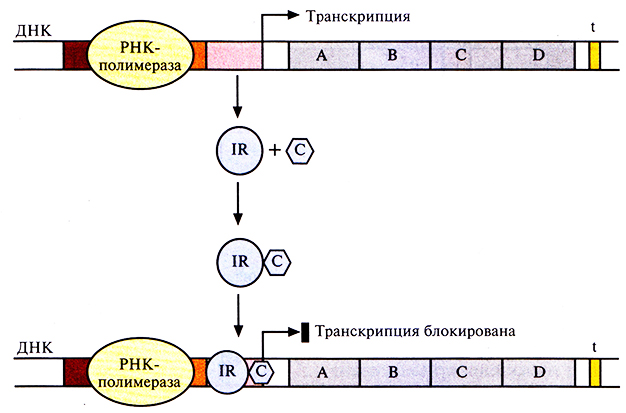
Рис. 3.21. Выключение транскрипции бактериального оперона. Связывание корепрессора (С) с неактивным репрессором (1R) изменяет конформацию последнего. Комплекс корепрессор–репрессор (С–IR) связывается с оператором и блокирует транскрипцию.
Регуляция транскрипции с помощью репрессора называется отрицательной. Если же система регуляции направлена на повышение скорости транскрипции, то она называется положительной. Рассмотрим вкратце этот процесс. Белок-активатор связывается с участком между ТАТА-боксом и сайтом инициации транскрипции. При этом он не только не блокирует перемещение РНК-полимеразы вдоль молекулы ДНК, а напротив, ускоряет его, действуя как своего рода «смазка». Активаторы специфичны для определенных сайтов активации. Иногда с работающим активатором связывается эффектор, переводящий его в неактивную форму, тогда скорость транскрипции уменьшается (рис. 3.22). В других случаях эффектор, напротив, активирует неработающий активатор. Чтобы понять детали регуляции транскрипции у бактерий, необходимо провести тщательный анализ мутации, которые влияют на данную регуляторную систему, и исследовать in vitro различные сайты связывания белков и ДНК.
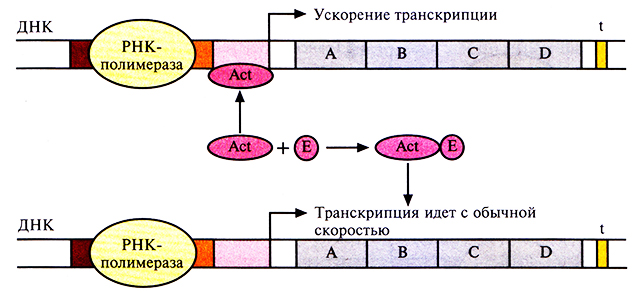
Рис. 3.22. Изменение скорости транскрипции. Активатор (Act) связан с участком между ТАТА-боксом и сайтом инициации транскрипции, скорость транскрипции повышена. Эффектор (Е) связывается с активатором и препятствует его соединению с ДНК; скорость транскрипции уменьшается
ВАЖНАЯ ВЕХА
Структура дезоксирибонуклеиновой кислоты
J.D. Watson, F.H.C. Crick Nature 171: 737-738, 1953
Выяснение молекулярной структуры генетического материала – ДНК – без сомнения стало одним из самых замечательных научных достижений XX в. Уотсон и Крик описали свое открытие так: «Мы хотим предложить структуру соли дезоксирибонуклеиновой кислоты (ДНК). Эта структура обладает весьма необычными свойствам! представляющими большой биологический интерес... Она образована двумя спиральными цепочками, закрученными вокруг общей оси... Обе спирали правые, но... последовательности атомов в них взаимно противоположны. Весьма интересен способ, с помощью которого цепочки удерживаются вместе... Пуриновые и пиримидиновые основания образуют пары, при этом пуриновое основание одной цепи соединяется водородными связями с пиримидиновым основанием другой... Если одно из оснований пары – это аденин, то... вторым основанием должен быть тимин; то же самое относится к гуанину и цитозину. Последовательность оснований в полинуклеотидной цепи может быть любой... Очень важно, что из предложенного нами механизма специфического спаривания непосредственно вытекает возможность копирования генетического материала». В следующей статье, опубликованной несколькими месяцами позже (Nature 171: 964, 1953), Уотсон и Крик уточняют «Сахарофосфатный остов в нашей модели абсолютно постоянен, но в эту структуру может вписаться любая последовательность пар нуклеотидов... В длинной молекуле возможно безграничное число перестановок, и нам кажется вполне вероятным, что точная последовательность оснований содержит в закодированном виде генетическую информацию... Наша модель дает объяснение многим феноменам. Например, спонтанная мутация может возникнуть в результате случайного перехода одного из оснований в редкую таутомерную форму, а образование пар гомологичных хромосом при мейозе может обусловливаться специфическим спариванием оснований».
За десять лет, прошедших после обнародования теории двойной спирали ДНК и принципа комплементарности, раскрыты молекулярные механизмы репликации ДНК; установлены процессы, отвечающие за расшифровку генетической информации и регуляцию синтеза генных продуктов: выяснены многие причины, по которым эти продукты синтезируются в измененном виде. Со времени выхода в свет этой публикации и до наших дней открытие Уотсона и Крика нисколько не утратило своего значения. В частности, если бы не была установлена структура ДНК, сейчас не существовало бы технологии рекомбинантных ДНК.
РЕГУЛЯЦИЯ ТРАНСКРИПЦИИ У ЭУКАРИОТ
Некий набор основных структурных генов, обеспечивающих жизнедеятельность клетки, – генов «домашнего хозяйства» – транскрибируется в большинстве активно функционирующих эукариотических клеток. В отличие от этого специфические гены, которые отвечают за уникальность тех или иных тканей или органов, транскрибируются и транслируются только в определенных клетках. Так, гены, кодирующие α- и β-субъединицы гемоглобина взрослого человека, экспрессируются исключительно в клетках – предшественниках эритроцитов. Число разных мРНК, специфичных для разных клеток, варьирует от единиц до десятков. Способность клеток включать (активировать) или выключать (ингибировать) структурные гены крайне важна для поддержания клеточной специфичности и экономного расходования энергетических ресурсов.
Для включения и выключения транскрипции различных эукариотических структурных генов используется множество разнообразных высоко-
специфичных процессов. Но так или иначе регуляция транскрипции у эукариот осуществляется с помощью специфических белков – факторов транскрипции. Многие из них связываются непосредственно с нуклеотидной последовательностью длиной менее 10 п.н., называемой по-разному: боксом, модулем, элементом инициации, регуляторным элементом. В отличие от прокариот у эукариот опероны в большинстве своем отсутствуют, т. е. каждый эукариотический структурный ген имеет свой собственный набор регуляторных элементов. Существенную роль в регуляции транскрипции у эукариот, помимо опосредованной взаимодействием между ДНК и белками, играют также белок – белковые взаимодействия.
Несмотря на индивидуальность набора регуляторных элементов у структурных генов эукариот, каждый из них имеет промоторный участок (ТАТА-бокс, или бокс Хогнесса) из восьми нуклеотидов, включающий последовательность TATA; последовательность ССААТ (САТ-бокс); участок из повторяющихся динуклеотидов GC (GC-бокс). Эти элементы находятся на расстоянии 25, 75 и 90 п.н. от сайта инициации соответственно (рис. 3.23). Транскрипция структурного гена эукариот начинается со связывания с ТАТА-боксом фактора транскрипции IID (TFIID), который представляет собой комплекс по крайней мере из 14 белков. Затем с TFIID и участками ДНК, примыкающими к ТАТА-боксу, связываются другие факторы транскрипции, и, наконец, со всем этим транскрипционным комплексом связывается РНК-полимераза II. Затем при участии дополнительных факторов происходит инициация транскрипции в точке +1 (рис. 3.24). Ясно, что если последовательность TATA отсутствует или существенно изменена, то транскрипция структурного гена становится невозможной. Идентифицированы также факторы транскрипции, специфичные для регуляторных элементов ССААТ и GC, но пока неясно, как ДНК-белковые взаимодействия могут влиять в этом случае на эффективность транскрипции, если элементы расположены на расстоянии более 75 п.н. от сайта инициации. Кроме того, на расстоянии сотен и даже тысяч пар оснований от сайта инициации находится так называемая энхансерная последовательность, которая многократно повышает скорость транскрипции структурных генов. По-видимому, сближение удаленных регуляторных элементов и соответствующего структурного гена происходит при укладке хромосомной ДНК. Кроме того, факторы транскрипции, которые связываются с определенными энхансерами и регуляторными элементами, могут образовывать цепочку, соединяющую удаленные друг от друга сайты.
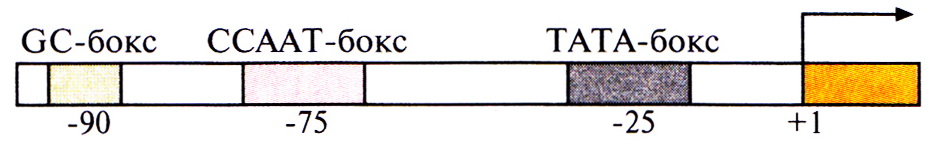
Рис. 3.23. Регуляторные элементы структурных генов эукариот. Знаки «–» при числах означают, что эти элементы находятся в молекуле ДНК слева от сайта инициации транскрипции (+1). Стрелка – направление транскрипции. Положение регуляторных элементов и их размер даны без соблюдения масштаба.
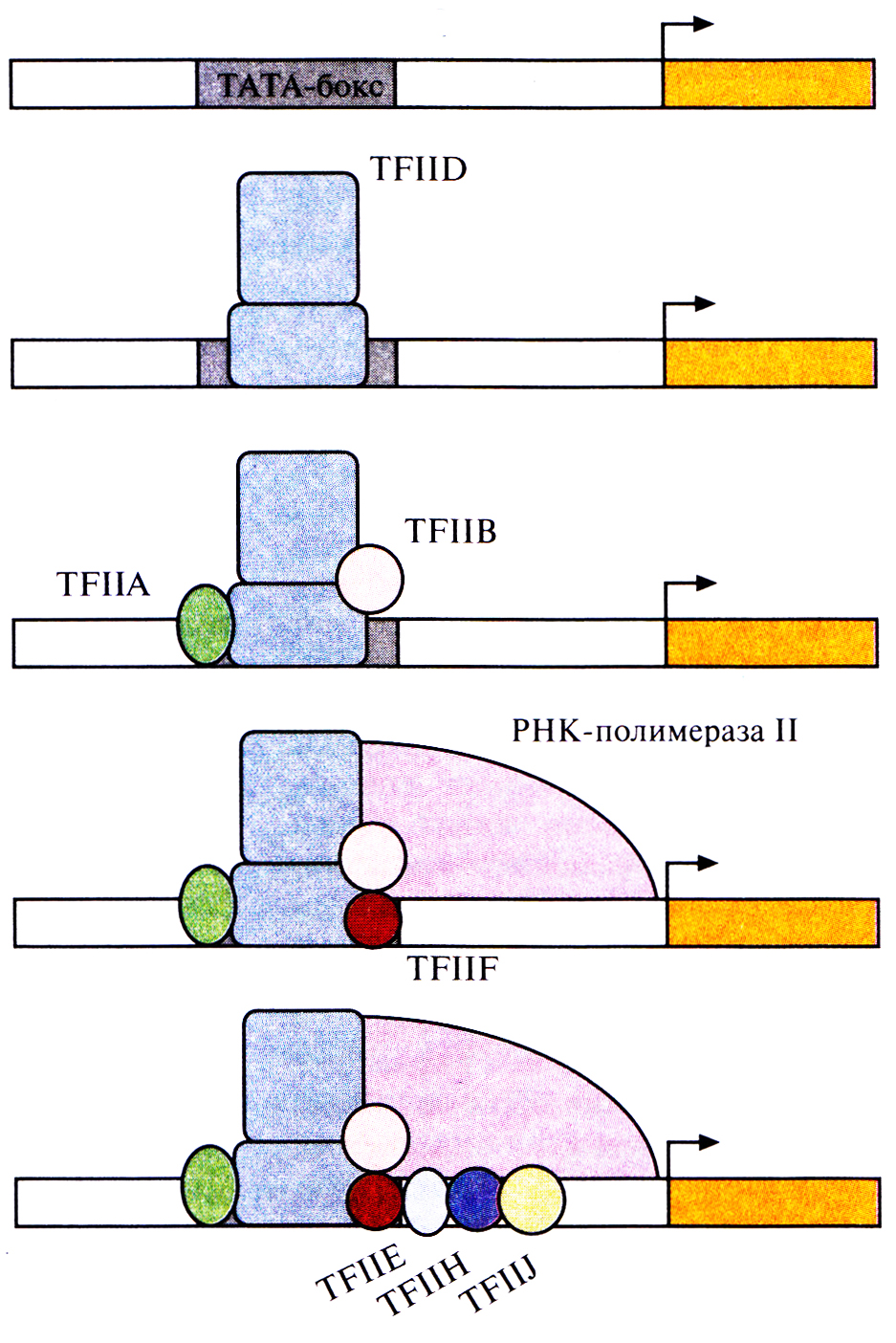
Рис. 3.24. Инициация транскрипции структурного гена эукариот. Сначала фактор транскрипции TFIID связывается с ТАТА-боксом, затем происходит присоединение других факторов транскрипции и РНК-полимеразы II и, наконец, вспомогательных факторов, запускающих транскрипцию. Стрелка – направление транскрипции.
Некоторые репрессированные (неэкспрессирующиеся) гены активируются каскадом событий, который запускается каким-либо специфическим внеклеточным сигналом, например повышением температуры или синтезом гормона. Гормон, поступив в кровоток, связывается с рецепторами специфических клеток, облегчающими его проникновение в клетку. Оказавшись в клетке, гормон вступает во взаимодействие с одним из клеточных белков и изменяет его конформацию. В таком измененном состоянии белок проникает в ядро и связывается со специфическим регуляторным элементом, который инициирует транскрипцию соответствующего гена.
Существуют также белки, которые, взаимодействуя с регуляторными элементами, блокируют транскрипцию. Например, известен класс генов позвоночных (примерно 18), активно транскрибирующихся только в нервных клетках. Каждый из этих генов имеет регуляторный элемент из 24 п.н., находящийся «левее» (upstream) сайта +1; он обозначается NRSE (от англ. neuron-restrictive silencer element). Во всех клетках, кроме нейронов, синтезируется NRSF-фактор (от англ. neuron-restrictive silencer factor), который связывается с NRSE и блокирует транскрипцию соответствующих генов. В нейронах NRSF не синтезируется, и упомянутые гены активно транскрибируются.
Итак, регуляция транскрипции у эукариот – это очень сложный процесс. Структурный ген может иметь множество регуляторных элементов, которые активируются специфическими сигналами в клетках разного типа в разное время клеточного цикла. Однако некоторые структурные гены находятся под контролем уникального фактора транскрипции. Специфические белки могут взаимодействовать с определенными ре гуля горными элементами и блокировать транскрипцию или связываться со всем транскрипционным комплексом еще до инициации транскрипции или во время элонгации.
ЗАКЛЮЧЕНИЕ
Молекула ДНК состоит из двух антипараллельных полинуклеотидных цепей, образующих двойную спираль. Их мономерной единицей является нуклеотид, который состоит из азотистого основания, дезоксирибозы и фосфатной группы. Соседние нуклеотиды в цепи связаны фосфодиэфирными связями, а цепи удерживаются вместе с помощью водородных связей, образующихся между комплементарными основаниями. При этом аденин образует водородные связи только с тимином, гуанин – только с цитозином. Процесс удвоения ДНК называется репликацией. В нем участвует множество различных белков, прежде всего ДНК-полимеразы. Каждая из цепей ДНК служит матрицей для синтеза комплементарной цепи. Комплементарность оснований противоположных цепей гарантирует идентичность новосинтезированной и исходной ДНК.
Ключевую роль в осуществлении всех биологических функций играют белки. Белковая молекула – это полипептид, состоящий из аминокислот, которые соединены друг с другом пептидными связями. Последовательность аминокислот в белке определяется последовательностью нуклеотидов в ДНК. В синтезе белков участвуют молекулы РНК (мРНК, рРНК и тРНК), различные ферменты и белковые факторы. Все РНК синтезируются на ДНК как на матрице; этот процесс называется транскрипцией. Правильность транскрипции, т. е. ее начало и завершение в нужных сайтах, обеспечивают специфические нуклеотидные последовательности в ДНК и белковые факторы. У эукариот большинство структурных генов состоит из кодирующих (экзоны) и некодирующих (интроны) участков. Первичные транскрипты содержат как те, так и другие. Однако по окончании транскрипции интроны вырезаются, а экзоны сшиваются с образованием функциональной мРНК. В мРНК содержится в закодированном виде информация о последовательности аминокислот в молекуле соответствующего белка.
Синтез белка называется трансляцией. Важную роль в нем играют молекулы тРНК и рРНК. В клетке присутствует более 50 разных тРНК.
Каждая из них строго специфически связывается своим 3'-концом с одной из 20 аминокислот. На 5'-конце тРНК находится последовательность из трех нуклеотидов (антикодон), обеспечивающая связывание тРНК с комплементарным участком из трех нуклеотидов в молекуле мРНК. Существуют две основные разновидности рРНК: малая и большая. Они объединяются соответственно с малой и большой субъединицами рибосомы – особой структуры, в которой и протекает синтез белка. У прокариот молекулы рРНК имеют меньший размер, чем у эукариот.
У прокариот трансляция начинается со связывания мРНК с малой рибосомной субъединицей. Затем происходит комплементарное спаривание первого кодона mРHK с антикодоном инициаторной тРНК (fMet-тРНК), к образовавшемуся комплексу присоединяется большая рибосомная субъединица, и образуется комплекс инициации (инициаторный комплекс), готовый к синтезу полипептидной цепи.
У эукариот трансляция начинается с присоединения инициаторной тРНК, которая несет остаток метионина (Met-TPHKMet), к малой рибосомной субъединице; с этой же субъединицей связывается своим 5'-концом мРНК. Малая субъединица перемещается вдоль мРНК до тех пор, пока не дойдет до первого AUG-кодона. Этот кодон образует комплементарную пару с антикодоном UAC инициаторной тРНК. Далее к этому комплексу присоединяется большая субъединица, и образуется рибосома, готовая к синтезу белка.
Элонгация и терминация трансляции у про- и эукариот во многом сходны. После образования инициаторного комплекса следующий кодон мРНК спаривается с антикодоном тРНК, несущей соответствующую аминокислоту (обозначим ее АК2). Первая аминокислота в полипептидной цепи, метионин, отщепляется от тРНК и соединяется с АК2 с помощью пептидной связи. Свободная тВНКМеt покидает рибосому. Рибосомный комплекс перемещается вдоль молекулы мРНК, и пептидил-тРНК, т. е. комплекс Met-AK2-TPHKAK2, занимает место, освобожденное отделившейся тРНК. Следующий кодон мРНК спаривается с соответствующим антикодоном тРНК, несущим аминокислоту АКЗ. АК2 отщепляется от своей тРНК и соединяется с АКЗ с помощью пептидной связи, образуя комплекс Met-АК2 АКЗ-тРНКакз. Освободившаяся от аминокислоты тРНК покидает рибосому. Рибосомный комплекс опять перемещается вдоль молекулы мРНК, и Мет-АК2-АКЗ-тРНКакз занимает вакантное место, занимаемое прежде предыдущей пептидил-тРНК. Эти события повторяются до тех пор, пока рибосома не дойдет до стоп-кодона. Антикодона, который был бы комплементарен стоп-кодону, нет ни у одной из тРНК. Однако стоп-кодон распознается неким белковым фактором освобождения; после присоединения этого фактора к рибосоме связь между последней тРНК и синтезированным полипептидом гидролизуется, тРНК, мРНК и полипептид высвобождаются, а рибосома диссоциирует на субъединицы.
Синтез мРНК и соответственно синтез белка должны строго регулироваться, поскольку у клетки недостаточно ресурсов для одновременной транскрипции и трансляции всех структурных генов. И про-, и эукариоты постоянно синтезируют только те мРНК, которые необходимы для выполнения основных клеточных функций. Экспрессия остальных структурных генов осуществляется под строгим контролем регуляторных систем, запускающих транскрипцию только в том случае, когда возникает потребность в определенном белке (белках). У прокариот транскрипция инициируется связыванием РНК-полимеразы с последовательностями TATA и TTGAC промоторной области структурного гена или оперона. Включение или выключение некоторых оперонов осуществляется при участии эффектора, который изменяет конформацию белка-репрессора и препятствует блокированию транскипции. При уменьшении концентрации эффектора в клетке репрессор связывается с участком ДНК, примыкающим к сайту инициации транскрипции, и препятствует перемещению РНК-полимеразы вдоль молекулы ДНК, блокируя таким образом транскрипцию. В других оперонах с участком ДНК, соседствующим с сайтом инициации траскрипции, связывается белок-активатор, который увеличивает скорость транскрипции. Связывание эффектора с активатором может снижать скорость транскрипции. ДНК-белковые взаимодействия, ответственные за регуляцию транскрипции, строго специфичны в отношении определенных структурных генов или оперонов. У эукариот РНК-полимераза II, которая транскрибирует структурные гены, связывается с целым набором белков – факторов транскрипции, которые последовательно присоединяются к ТАТА-последовательности промоторной области. За включение и выключение транскрипции отвечают дополнительные факторы транскрипции, которые связываются с соответствующими участками ДНК.

