Подкислителями считаются пищевые кислоты, используемые как вкусовые добавки для придания продуктам «острого» вкуса и для сохранения пищи.
Главными пищевыми кислотами считаются четыре органические кислоты: лимонная, молочная, уксусная и винная (иногда к ним причисляют яблочную).
Несмотря на значительный прогресс в области органического синтеза, многие пищевые кислоты получают в настоящее время микробиологическим синтезом (табл. 18.1).
Таблица 18.1. Пищевые кислоты и образующие их микроорганизмы
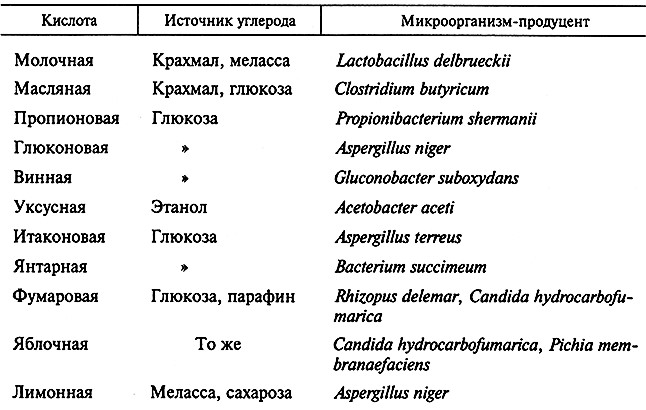
Продукты естественного брожения для пищевой промышленности более предпочтительны, чем синтетические кислоты, так как они безвредны для организма человека.
Для получения пищевых кислот используют как традиционные технологии, так и новейшие достижения биотехнологии.
18.1. ЛИМОННАЯ КИСЛОТА
Лимонная кислота (СН2СООН–СОНСООН–СН2СООН) – трехосновная оксикислота, кристаллизующаяся из водных растворов с одной молекулой воды в виде бесцветных, прозрачных кристаллов ромбической формы. Из всех пищевых кислот она обладает наиболее мягким вкусом и не оказывает раздражающего действия на слизистые оболочки желудочно-кишечного тракта. Регуляторами рН пищевых систем являются соли лимонной кислоты – цитраты натрия, калия, кальция, магния и аммония.
В природных условиях лимонная кислота встречается главным образом в незрелых плодах цитрусовых, ананасов, груш, инжира, брусники, клюквы и др. Первые заводы по производству кристаллической лимонной кислоты из природных источников – апельсинов и лимонов – были созданы в Италии в середине XIX в.
В настоящее время по объему производства лимонная кислота является одним их главных продуктов микробного синтеза. Ее общий выпуск в различных странах достигает 800 тыс. т в год.
Годовой прирост производства лимонной кислоты составляет 5 % существующего уровня. Около 70 % производимой лимонной кислоты используют в пищевой промышленности, 18–20 % – в виде ее соли, цитрата натрия, для изготовления экологически чистых моющих средств.
Многие органические вещества могут быть трансформированы микромицетами в лимонную кислоту, но ее максимальный выход достигается при биосинтезе из сахарозы или фруктозы.
Химизм образования лимонной кислоты
Синтез лимонной кислоты связан с циклом дикарбоновых кислот и происходит в результате конденсации щавелево-уксусной кислоты, содержащей четыре атома углерода и две карбоксильные группы, с уксусной кислотой, имеющей два атома углерода и одну карбоксильную группу (рис. 18.1).
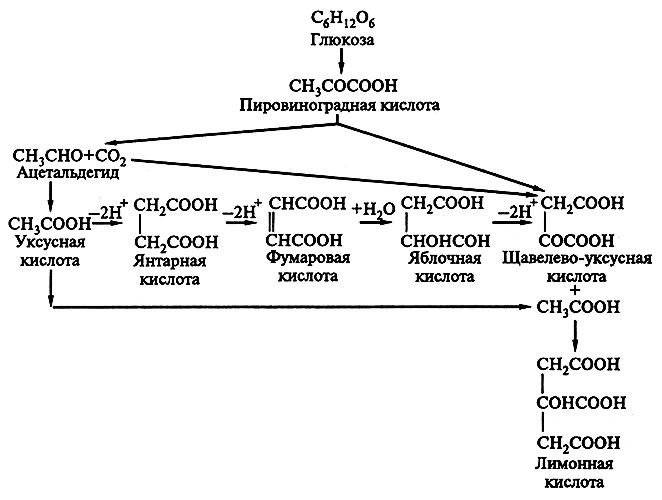
Рис. 18.1. Химизм образования лимонной кислоты
Промышленным способом лимонную кислоту получают из мелассы микробиологическим синтезом, применяя главным образом мутантные штаммы микроскопического гриба Aspergillus niger. Заводы малой и средней мощности производят лимонную кислоту поверхностным методом культивирования. Глубинный метод экономически выгоден, если мощность завода превышает 2500 т лимонной кислоты в год.
Меласса считается пригодной для производства лимонной кислоты поверхностным способом, если съем лимонной кислоты при контрольном сбраживании составляет не менее 1,25 кг/м2 в сутки, глубинным способом – 10–12 кг/м3.
Хорошо сбраживаемые мелассы обычно содержат, %: инвертного сахара – не более 1, СаО – 1, SО2 – 0,06 при общем содержании сухих веществ не менее 75 и сахара более 46.
Производство лимонной кислоты включает следующие основные технологические стадии:
- получение посевного материала;
- подготовка мелассы к сбраживанию;
- сбраживание растворов мелассы в лимонную кислоту;
- отделение мицелия;
- выделение из сброженных растворов лимонной кислоты;
- получение ее в кристаллическом виде и высушивание.
Тщательно проверенную на микробиологическую чистоту и
биохимическую активность музейную культуру используют для приготовления посевного материала. Посевной материал размножают в пробирках с агаризованной средой (сусло-агар), а затем в колбах и кюветах – на твердой питательной среде. Длительность каждой стадии 2–7сут, оптимальная температура выращивания 32 °С.
В зависимости от способа сбраживания мелассу разбавляют и готовят растворы с различной концентрацией сахара: для поверхностного выращивания A. niger до 13–15 %, для глубинного культивирования – 3–4 и 25–28 %. рН приготовленных растворов доводят H2SCО4 до 6,8–7,5. Для выращивания продуцентов лимонной кислоты возможно использование крахмалосодержащего сырья. Предварительно осуществляют гидролиз крахмальной суспензии, содержащей 26–30% СВ, ферментным препаратом бактериальной а-амилазы, взятым в количестве 1,5–2,0ед. амилолитической активности (АС) на 1 г СВ крахмала, при повышенной температуре и избыточном давлении. К гидролизату добавляют минеральные соли в виде сульфатов цинка, железа (И), меди в количестве (2,0–7,0)10–3 г/дм3 гидролизата крахмала.
Поверхностный способ. При этом способе выращивания A. niger подготовленную мелассу подают в варочный аппарат, где разбавляют кипящей водой в соотношении 1:1, рН раствора доводят до 6,8–7,2. При кипячении вводят раствор желтой кровяной соли для осаждения железа и солей тяжелых металлов с таким расчетом, чтобы избыток свободного ферроцианида, угнетающего развитие микроорганизма, не превышал 10мг%.
Для активного биосинтеза лимонной кислоты в питательной среде кроме сахара должно содержаться 0,07 % азота, 0,02 % Р2О5, а также цинк, магний, калий и другие микроэлементы, которые вводят в среду в виде солей. Готовая среда с температурой 45 ...50 °С поступает в бродильные камеры. Культивирование гриба осуществляют в кюветах из нержавеющей стали или алюминия, установленных на стеллажах. После предварительной стерилизации камер парами формалина, дегазации газообразным аммиаком и охлаждения до 30...40 °С воздухом производят заполнение кювет питательной средой (толщина слоя от 8 до 18 см). В камере предусмотрена система вентиляции для подачи нагретого (до 30...32 °С) стерильного кондиционированного воздуха из расчета 3–18 м3/ч на 1 м2 поверхности кювет. В питательную среду через воздуховоды с помощью специального устройства для распыления вносят посевной материал из расчета 50–75 мг конидий на 1 м2 площади кюветы.
Наиболее эффективный режим культивирования – так называемый бессменный способ с доливом. Суть его заключается в том, что раствор мелассы в количестве 30–35 % начального объема вводят под пленку гриба. Долив питательной среды производят один или несколько раз, начиная с четвертых-пятых суток роста, через каждые 36–48 ч. Добавляемый раствор мелассы содержит 8,5–11,0 % сахара и не имеет в своем составе питательных солей и антисептиков. Такой режим обеспечивает увеличение съема лимонной кислоты с 1 м2 бродильной поверхности на 15–20% и снижает удельный расход мелассы на 10–45% по сравнению с другими методами.
Брожение прекращают, когда в растворе остается 1–2 % сахара и общая титруемая кислотность в сброженном растворе достигает 12–20 %. Сброженный раствор сливают в сборник. Для промывки мицелия под грибную пленку подливают горячую воду. После слива промывных вод мицелий по вакуум-линии транспортируют в запарник для отмывания от кислоты горячей водой. Кислые растворы (концентрация 2,5–6,0%), собранные из-под ложного днища запарника, подают на фильтр-пресс. Выгруженный из запарника с помощью шнека мицелий используют на корм скоту.
При поверхностном способе выращивания A.niger основные растворы содержат от 12 до 20 % органических кислот в пересчете на лимонную кислоту, 0,5–2,0 % несброженных Сахаров и другие продукты метаболизма. Содержание лимонной кислоты в сброженных растворах составляет 94–98 %.
Глубинный способ. При глубинном способе выращивание A. niger ведут в ферментерах (рис. 18.2). Конидии проращивают в посевных аппаратах (инокуляторах).
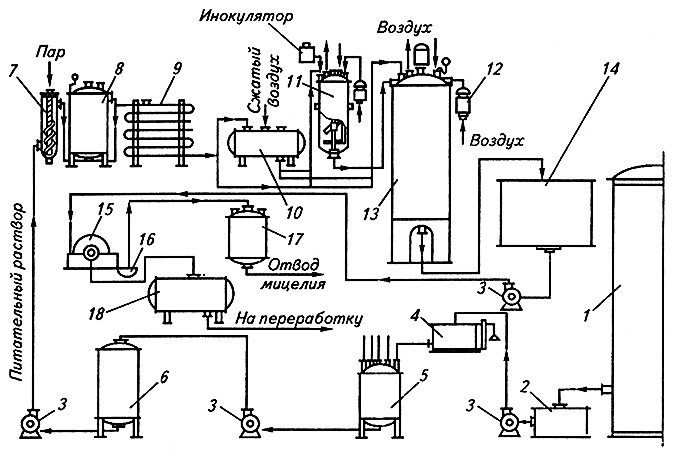
Рис. 18.2. Аппаратурно-технологическая схема получения лимонной кислоты глубинным способом:
1 – резервуар с мелассой; 2 – приемный бак; 3 – насос; 4 – весы; 5 – варочный аппарат;
6 – промежуточная емкость; 7– стерилизационная колонка; 8 – выдерживатель; 9 – холодильник;
10 – емкость для хранения мелассы; 11 – посевной аппарат; 12 – противобактериальные фильтры;
13 – производственный ферментер; 14 – промежуточный сборник; 15 – барабанный вакуум-фильтр;
16 – приемник мицелия; 17 – вакуум-сборник для мицелия;
18 – вакуум-сборник фильтрованного (сброженного) раствора
Раствор мелассы, содержащий 3–4 % сахара, для посевных аппаратов готовят в варочном аппарате. Мелассу разбавляют кипящей водой, устанавливают рН 7,0–7,2, для удаления железа при кипячении добавляют желтую кровяную соль, растворы NH4CI и MgSО4 вводят в регламентированных количествах. Подготовленный раствор стерилизуют при 128...130 °С в течение 12–15 мин. В раствор мелассы, охлажденный в посевном аппарате до 35...36 °С, добавляют стерильные растворы К2НРО4 и MgSО4. Для производственного ферментера раствор мелассы готовят в той же последовательности. Растворы питательных солей готовят отдельно и стерилизуют при температуре 123...125 °С. Воду стерилизуют при 128...130 °С.
Подливной раствор должен иметь 25–28%-ю концентрацию по сахару и температуру 34...36 °С, как и основной сбраживаемый раствор. Подливной раствор направляют в сборник. Посевной аппарат засевают предварительно подготовленной суспензией конидий (З г сухих конидий суспендируют в 2–3 дм3 стерильного раствора мелассы или питательной среды). Культуру выращивают при 34...35 °С при постоянном перемешивании, дробной аэрации и избыточном давлении в аппарате 10–20 кПа.
Процесс подращивания мицелия заканчивается через 30–36 ч. Общая титруемая кислотность культуральной жидкости составляет 1–2%. Подращенный мицелий передают для засева среды в производственном ферментере.
Процесс кислотообразования продолжается 5–7сут при температуре 31...32 °С, непрерывном перемешивании и дробной аэрации от 1,0 до 1,5 м3/(м3 • ч).
Начиная со 2-х суток после посева по мере снижения концентрации сахара в среде 2–3 раза проводят дробное введение подливного 25–28%-го раствора, обычно из расчета доведения конечной концентрации сахара в сбраживаемом растворе до 12–15 %. После окончания процесса сброженный раствор нагревают острым паром до 60...65 °С и сливают в сборник, откуда его подают на вакуум-фильтр для отделения мицелия и промывки его горячей водой. Отделенный и промытый мицелий направляется на корм скоту. Основной раствор лимонной кислоты вместе с промывными водами передается в химический цех для выделения лимонной кислоты.
При глубинном способе сбраживания основные растворы содержат от 5 до 12 % органических кислот, 0,2–1,5 % сахара, а лимонная кислота составляет 80–98% суммы всех кислот. Схема выделения лимонной кислоты из сброженных растворов представлена на рисунке 18.3.
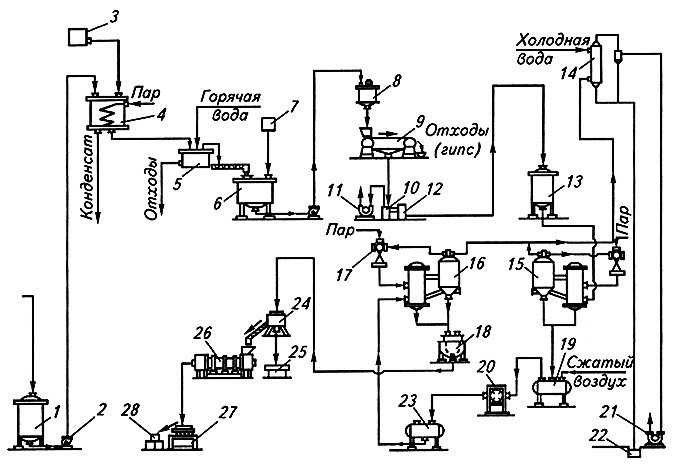
Рис. 18.3. Технологическая схема химической стадии производства лимонной кислоты:
1 – сборник сброженных растворов; 2 – насос; 3 – сборник известкового молока; 4 – нейтрализатор;
5 – фильтр для отделения цитрата кальция; 6 – реактор; 7 – бачок-мерник серной кислоты;
8 – промежуточный сборник; 9 – ленточный вакуум-фильтр для отделения гипса; 10 – вакуум-сборник;
11 – вакуум-насос; 12 – насос; 13 – сборник раствора лимонной кислоты;
14 – барометрический конденсатор с ловушкой; 15 – вакуум-аппарат первой выпарки;
16– вакуум-аппарат второй выпарки; 17 – пароструйный компрессор; 18 – кристаллизатор;
19 – монтежю; 20 – фильтр-пресс; 21 – вакуум-насос; 22 – барометрический ящик;
23 – промежуточный сборник; 24 – центрифуга; 25 – сборник маточного раствора;
26 – барабанная сушилка; 27 – трясосито; 28 – упаковочный аппарат
Сброженные растворы представляют собой смесь лимонной, глюконовой и щавелевой кислот, несброженного сахара и минеральных примесей. Лимонную кислоту из раствора выделяют путем связывания ее катионами кальция с образованием слаборастворимой соли цитрата кальция.
Сброженный раствор нагревают в нейтрализаторе до кипения, после чего в него при непрерывном перемешивании вводят известковое молоко. Нейтрализация считается законченной при рН 6,8–7,5. При нейтрализации сброженного раствора образуются кальциевые соли лимонной, глюконовой и щавелевой кислот:
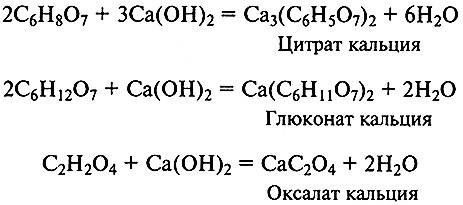
Кальциевые соли лимонной и щавелевой кислот выпадают при этом в осадок, а кальциевая соль глюконовой кислоты и основная часть органических и минеральных веществ мелассы остаются в растворе. После отделения маточного раствора осадок на вакуум-фильтре промывают горячей водой (температура около 95 °С).
Перевод лимонной кислоты в свободное состояние и отделение ее от оксалата кальция достигается обработкой осадка H2SO4 с последующим фильтрованием. Разложение цитрата кальция осуществляют в реакторе, снабженном мешалкой и паровым барботером. В реактор подают воду из расчета 0,25–0,5 м3 на 1 т лимонной кислоты и при работающей мешалке загружают туда же цитрат кальция с таким расчетом, чтобы после его разложения концентрация лимонной кислоты в растворе была не ниже 25 %. В качестве осветлителя в реактор вводят активированный уголь (2 % массы лимонной кислоты), содержимое реактора нагревают до 60 °С и при перемешивании подают из мерника серную кислоту (плотность 1,8–1,84) из расчета 0,425 дм3 на 1 кг лимонной кислоты в цитрате. Смесь кипятят в течение 10–20 мин.
Разложение цитрата кальция серной кислотой протекает по уравнению
Са3(С6Н607)2 + 3H2SО4 = 2С6Н8О7 + 3CaSО4
После полного разложения цитрата кальция в реактор вводят гранулированный сернистый барий (из расчета 0,1–0,15 кг на 100 кг лимонной кислоты) для осаждения тяжелых металлов. Для отделения раствора лимонной кислоты от осадка, содержащего гипс, оксалат кальция, уголь, сернистые соединения, тяжелые металлы и берлинскую лазурь, горячую реакционную смесь направляют из реактора на вакуум-фильтр. Отфильтрованный раствор передают на дополнительное выпаривание, а осадок на фильтре промывают горячей водой (90 °С). Промывку осадка прекращают при содержании лимонной кислоты в промывной воде 0,1 %. Средняя концентрация раствора лимонной кислоты (вместе с промывными водами) должна быть не ниже 16 %.
Выпаривание осуществляют в вакуум-аппаратах и проводят в две стадии с промежуточным освобождением раствора от осадка гипса. В первом аппарате раствор выпаривают до плотности 1,24–1,26 кг/дм3, осадок отделяют на фильтре-прессе. Во втором аппарате прозрачный раствор выпаривают до плотности 1,35–1,36 кг/дм3, что соответствует 80%-й концентрации лимонной кислоты, и передают на кристаллизацию (температура раствора 70 °С), затем раствор охлаждают до 35... 37 °С и вносят в него затравку – кристаллы лимонной кислоты. Кристаллизацию проводят при непрерывном перемешивании и медленном охлаждении до температуры 8... 10 °С, при этой температуре раствор выдерживают не менее 30–45 мин. Кристаллы отделяют в центрифуге, промывают их небольшим количеством холодной воды и передают на сушку.
Сушку проводят в ленточных или барабанных пневматических сушилках при температуре воздуха не более 35 °С. В товарном продукте должно содержаться не менее 99,5 % лимонной кислоты (в пересчете на моногидрат), зольность не более 0,1 % для высшего сорта и 0,35 % для I сорта.
Лимонную кислоту широко используют в кулинарии и пищевой промышленности для приготовления хлебного кваса, безалкогольных напитков, мармелада, вафель, пастилы и др. Лимонная кислота включена в рецептуру некоторых сортов колбас и сыра, ее применяют в виноделии, для рафинирования растительных масел, для производства сгущенного молока. С ее помощью сохраняют естественный вкус и аромат мяса и рыбы при длительном хранении.
Пищевые добавки на базе солей лимонной кислоты, придающие целевые функциональные свойства пищевому сырью и продуктам питания, считаются наиболее безопасными.
Целесообразно применение цитрата кальция, малая растворимость которого сбалансирована со скоростью всасывания кальция в кишечном тракте.
О широком применении таких добавок в мировой практике (в основном за рубежом) свидетельствуют данные, приведенные в таблице 18.2.
Таблица 18.2. Применение солей лимонной кислоты
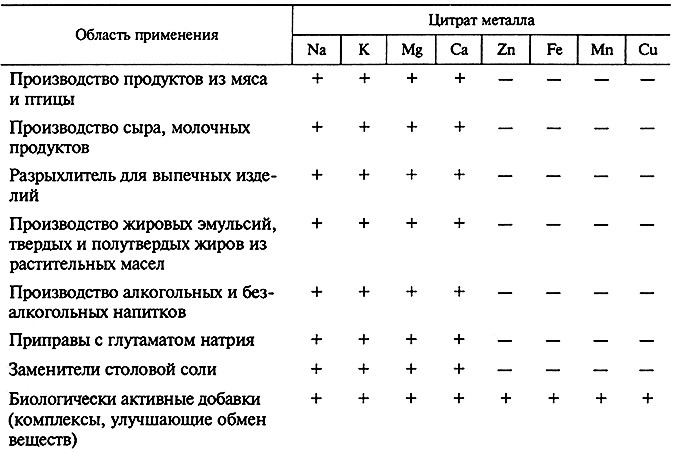
Применение цитратов при производстве различных напитков позволяет обогащать их важными минеральными добавками, а также модифицировать органолептические показатели (цвет, вкус). Цитраты кальция и магния используют в диетических составах, заменяющих столовую соль.
Замена поваренной соли цитратом калия позволяет выпекать лечебный ахлоридный хлеб для больных сердечно-сосудистыми заболеваниями.
Интерес к применению цитратов при производстве продуктов питания в последние годы увеличивается, однако по мере развития и углубления исследований возможного влияния добавок (микроэлементов, витаминов) меняются (в основном ужесточаются) допустимые нормы содержания отдельных добавок в пищевых продуктах, устанавливаются нормативы для отдельных групп населения, уточняются нормативы для диетического питания, например верхний уровень допустимой дозы кальция для взрослых – 2500 мг/сут, магния – 350 мг/сут.
В ближайшем будущем лимонная кислота и ее соли найдут более широкое применение в нашей стране в составе продуктов нового поколения, что будет способствовать оздоровлению всего населения.
18.2. УКСУСНАЯ КИСЛОТА
Уксусная кислота (СН3СООН) – наиболее известная пищевая кислота, представляющая собой бесцветную жидкость с резким запахом. В результате перегонки перебродившего спиртового раствора получают 70–80%-й раствор уксусной кислоты, известный под названием уксусной эссенции. Из товарных форм уксусной кислоты известны чистая пищевая (70–80%), безводная или ледяная (98–99 %), выпадающая при охлаждении в осадок в виде кристаллов.
Уксусная кислота находит широкое применение в пищевой промышленности. Ежегодно в мире производят более 100 тыс. т уксусной кислоты, причем более половины – микробиологическим синтезом.
Уксуснокислое брожение основано на способности уксуснокислых бактерий рода Acetobacter окислять этанол в уксусную кислоту. В реакции образования уксусной кислоты участвует фермент алкогольоксидаза. Окисление этанола в уксусную кислоту может быть описано уравнением
СН3СН2ОН + О2 = СН3СООН + Н2О + 490 кДж
В промышленных условиях уксуснокислое брожение проводят непрерывным способом при глубинном проточном культивировании уксуснокислых бактерий в батарее последовательно соединенных аппаратов. Схема производства включает следующие основные технологические стадии:
- получение посевного материала;
- подготовка сырья;
- уксуснокислое брожение;
- розлив готового продукта.
Способностью превращать этанол в уксусную кислоту обладают различные виды уксуснокислых бактерий. В уксуснокислом брожении используют в основном два вида бактерий: Bacterium schutzenbachii и Bacterium curvum.
Для уксуснокислого брожения благоприятны температуры 28 °С для культуры В. schutzenbachii и 35 °С для культуры В. curvum, а также кислая реакция среды.
Для получения посевной культуры уксуснокислые бактерии выращивают в колбах на жидкой питательной среде, а затем в лабораторном аппарате объемом 30 дм3.
Наилучшее сырье для уксуснокислого брожения – этанол, полученный из зернового и картофельного сырья. Для переработки используют как ректификат, так и спирт-сырец.
На жизнедеятельность уксуснокислых бактерий большое влияние оказывает реакция среды. Принято считать, что оптимальные значения рН для их развития находятся в пределах 3–3,2, однако избыток уксусной кислоты в сбраживаемой среде угнетает жизнедеятельность бактерий-продуцентов. Для сохранения естественной чистоты бактериальной популяции оптимальной считается концентрация кислоты около 10 %. Важным показателем является и предельная концентрация этанола в сбраживаемой среде. Для В. schutzenbachii она составляет 6–7 об. %, для В. curvum – 9–14.
В промышленности уксуснокислое брожение проводят в батарее, состоящей из пяти последовательно соединенных ферментеров. Первый аппарат батареи является генератором уксуснокислых бактерий и непрерывно снабжает все последующие аппараты активной культурой. В нем создаются условия, способствующие быстрому размножению уксуснокислых бактерий. Кроме того, в аппарате происходит интенсивное окисление этанола в уксусную кислоту. Для осуществления этих процессов в первый аппарат непрерывно подается среда, суммарная концентрация этанола и уксусной кислоты в которой составляет 6,4–6,7 %.
В процессе уксуснокислого брожения температура от ферментера к ферментеру снижается. Если в первом она равна 28 °С, то в последнем – 25 °С. Уменьшается также и аэрация с 0,35–0,40 м3/(м3-мин) в первом ферментере до 0,1–0,15 м3/(м3-мин) в последнем. В каждом ферментере создаются условия, способствующие интенсивному окислению этанола в уксусную кислоту. Для поддержания заданной концентрации спирта во второй, третий и четвертый аппараты подают среду с 40%-м этанолом. Процесс ведут таким образом, чтобы из пятого аппарата выводилась культуральная жидкость с концентрацией уксусной кислоты не ниже 9–9,3 %. Из 100 дм3 безводного спирта получают 75–90 кг уксусной кислоты.
Перед розливом 9%-ю уксусную кислоту (столовый уксус) осветляют бентонитом с добавлением небольшого количества лимонной кислоты. Отфильтрованный на фильтре-прессе раствор поступает на розлив.
В производстве уксуса спиртовое брожение лучше всего осуществляют отселекционированные штаммы винных дрожжей (например, Saccharomyces ellipsoideus), которые помимо этанола синтезируют побочные продукты метаболизма, улучшающие вкус и аромат. Уксус, полученный микробиологическим путем (пищевая уксусная кислота, столовый уксус), как и вино, различается по сортам в зависимости от характера сбраживаемого субстрата. Известны яблочный, виноградный, грушевый и другие сорта уксуса. Уксус, полученный при брожении, имеет приятные аромат и вкус, которые обусловливают побочные продукты брожения: сложные эфиры, высшие спирты, органические кислоты.
Уксусная кислота стала первым микробиологическим продуктом, полученным с помощью иммобилизованных клеток. В течение длительного времени применяется адсорбирование уксуснокислых бактерий на древесной стружке, древесном угле, коксе и других субстратах. Пропуская раствор этанола через генераторы с иммобилизованными бактериями, получают 10–15%-й раствор уксусной кислоты.
Действие уксусной кислоты, основанное обычно на снижении рН консервируемого продукта, проявляется при концентрации выше 0,5 % и направлено главным образом против бактерий. Ее используют при изготовлении майонезов, соусов, при мариновании рыбной продукции, овощей, ягод и фруктов. Уксусную кислоту также широко применяют как вкусовую добавку.
Применение ацетата калия, натрия, кальция и аммония разрешено в производстве овощных консервов и маринованных продуктов.
18.3. МОЛОЧНАЯ КИСЛОТА
В настоящее время около половины мирового производства молочной кислоты (СН3СНОНСООН) осуществляется микробиологическим методом, основанным на сбраживании таких ценных углеводсодержащих субстратов, как сахар, рафинадная патока, меласса, сахарный сироп и др., что существенно увеличивает себестоимость конечного продукта. Относительно высокая стоимость молочной кислоты – основной фактор, ограничивающий ее широкое применение в качестве подкислителя, консерванта, регулятора рН, улучшителя вкуса, запаха и структуры пищевых продуктов.
Для получения молочной кислоты микробиологическим методом используют анаэробное превращение углеводов молочнокислыми бактериями. Гидроксильная группа этой кислоты может находиться в двух (α и β) положениях углеродной цепи. Промышленное значение имеет α-оксипропионовая кислота, продуцируемая в процессе молочнокислого брожения.
В промышленных условиях обычно применяют штаммы: Lactobacillus delbrueckii, L. leichmannii, L. bulgaricus, Streptococcus lactis. Различают гомо- и гетероферментативное молочнокислое брожение. В первом случае образуется почти исключительно молочная кислота; во втором – и другие продукты брожения.
Образование молочной кислоты из глюкозы при сбраживании гомоферментативными молочнокислыми бактериями (Lactobacillus) происходит согласно уравнениям:
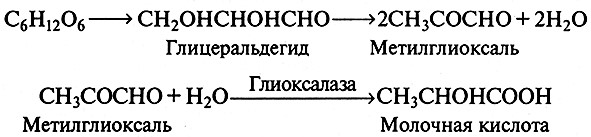
Расщепление глюкозы происходит по ФДФ-пути, бактерии имеют для этого все необходимые ферменты, включая альдолазу.
Другой вариант схемы молочнокислого брожения включает распад глюкозы до пировиноградной кислоты и восстановление пировиноградной кислоты до молочной:
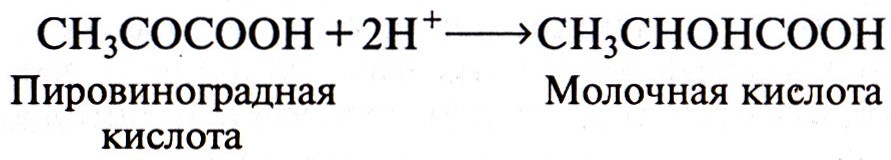
Кристаллы молочной кислоты при атмосферном давлении быстро плавятся с образованием бесцветной сиропообразной жидкости без запаха с резко кислым вкусом.
В промышленных условиях молочную кислоту получают глубинным способом с помощью культуры L. delbrueckii (рис. 18.4). В качестве основного сырья используют мелассу, сахарозу, гидролизаты крахмала, кукурузный сироп. Концентрация сахара в среде составляет 5–20 %, рН 6,3–6,5. Во время ферментации рН среды поддерживают при помощи СаСО3, который добавляют 3–4 раза в сутки. Молочнокислое брожение проводят при строго постоянной температуре 50 °С. Снижение температуры до 46...48 °С вызывает резкое ослабление биохимической активности культуры и способствует развитию посторонней микрофлоры. Повышение температуры, например до 53...55 °С, также вызывает инактивацию культуры и замедление брожения.
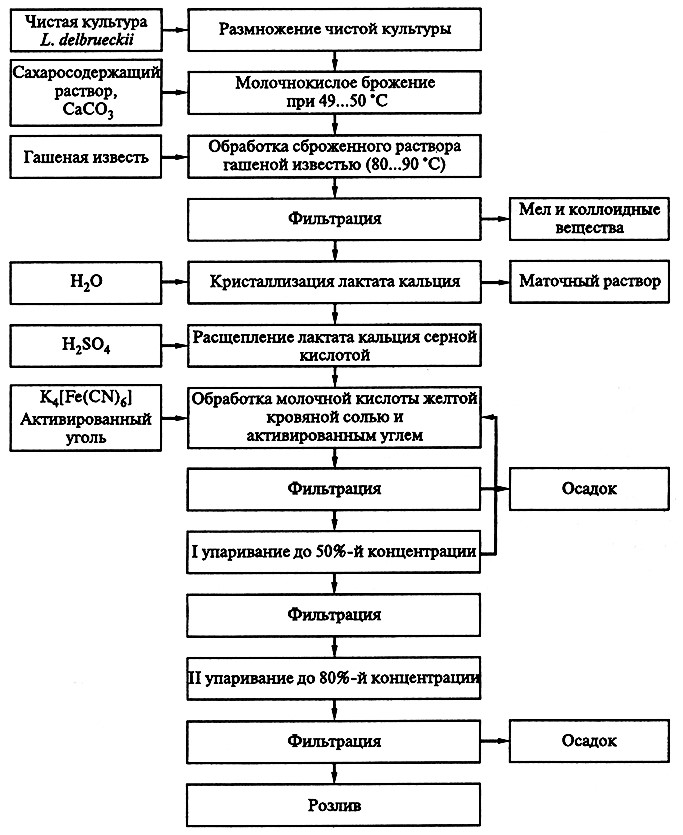
Рис. 18.4. Принципиальная технологическая схема процесса производства молочной кислоты
При нормальном брожении бактерии сбраживают за сутки 1–1,5 % сахара, и весь цикл брожения заканчивается за 7–11 сут. При этом количество несброженного сахара составляет 0,5–0,7 %, а концентрация лактата кальция – 10–15%. Для отделения СаСО3 и коллоидов сброженный раствор нагревают до 80...90 °С, а затем обрабатывают гашеной известью до слабощелочной реакции и отстаивают в течение 3–5 ч.
Фильтрацию проводят при температуре раствора лактата кальция 70...80 °С. Полученный фильтрат упаривают до концентрации 27–30 %, затем охлаждают до температуры 25...30 °С и выдерживают 36–48 ч в кристаллизаторе. Кристаллизация считается законченной, если в маточном растворе остается не более 5–6% растворенного лактата кальция.
Промытый холодной водой лактат кальция отделяют на центрифуге и расплавляют. С целью предохранения лактата от обугливания расщепление лактата кальция серной кислотой с выделением свободной молочной кислоты проводят при 60...70 °С.
Для отделения ионов железа полученную сырую молочную кислоту при температуре 65 °С обрабатывают K4[Fe(CN)6] (желтой кровяной солью). В осадок выпадает берлинская лазурь. Тяжелые металлы и мышьяк осаждают Na2SО4 и Ba2S. Для освобождения молочной кислоты от красящих веществ используют активированный уголь. После обработки полученную смесь фильтруют, а осадок гипса промывают для извлечения оставшейся молочной кислоты.
После расщепления кристаллического лактата кальция и последующей обработки получают 18–20%-ю молочную кислоту, которую упаривают до 50%-й и осветляют активированным углем, затем обрабатывают желтой кровяной солью. Отфильтрованную 50%-ю молочную кислоту сливают в сборник готовой продукции, а из него подают на фасовку.
Для получения 80%-й кислоты 50%-ю молочную кислоту вторично упаривают при большом разрежении в вакуум-аппаратах. 80%-ю молочную кислоту фильтруют на фильтре-прессе и подают на розлив или на приготовление 80%-й пастообразной кислоты, которую получают внесением в нее небольших количеств мела (4 % массы кислоты).
Один из возможных путей создания высокоэффективных и ресурсосберегающих технологий производства молочной кислоты – расширение сырьевой базы для культивирования молочнокислых бактерий для замены дорогостоящих и дефицитных источников углеводов более дешевым и доступным сырьем, например разнообразными отходами перерабатывающей промышленности и сельского хозяйства.
В качестве основных углеводсодержащих субстратов для молочнокислого брожения возможно использование молочной сыворотки, а также яблочных выжимок и нестандартного, дефектного яблочного сырья.
Для ферментации молочной сыворотки оптимально использование культуры Lactobacillus acidophilus ВКМ 1660 (Т), для ферментации плодового сырья и отходов переработки сельскохозяйственного сырья – культуры Lactobacillus plantarum ВКМ 578, как обеспечивающих высокий выход молочной кислоты и высокую бродильную активность.
В качестве питательной среды для культивирования кислотообразующих бактерий могут быть использованы заводская нефильтрованная сыворотка и осветленная сыворотка (полученная при сепарировании и ультрафильтрации). Активнее процесс накопления молочной кислоты происходит на осветленной молочной сыворотке. В этом случае выход молочной кислоты в 1,5–1,7 раз выше, чем на неосветленных образцах сыворотки, и в 1,1–1,2 раза больше, чем на ультрафильтрате.
Ферментацию молочной сыворотки с применением культуры L. acidophillus ВКМ 1660 (Т) осуществляют анаэробно, при температуре 30 °С, рН 6–6,5. Посевной материал, выращенный в течение 48 ч и содержащий не менее 109 клеток/см3, вносят в ферментационную среду в дозировке 20 % общего объема. Начальная концентрация лактозы составляет 5–10 %.
При сбраживании молочной сыворотки без проведения под- титровки молочнокислые бактерии могут накапливать до 2,2 % молочной кислоты. Содержание в растворе более 2,5 % молочной кислоты подавляет развитие бактерий, поэтому образующуюся в процессе ферментации молочную кислоту периодически нейтрализуют СаС03. Это позволяет добиться увеличения выхода молочной кислоты.
По отношению к различным титрантам (20%-й КОН, NaOH, NH4OH, СаСО3, MgCО3, СаО) молочнокислые бактерии ведут себя практически одинаково. Установлено, что подтитровку нужно проводить до содержания свободной кислоты в среде 0,2–0,5 %, рН 5–5,5. При этом процесс накопления молочной кислоты продолжается до 6 сут.
Получаемая молочная кислота обогащена аминокислотами и микроэлементами, нетоксична, а осадок, получаемый при производстве молочной кислоты, можно использовать в качестве полноценной кормовой добавки.
На основе подробного химического анализа, а также микробиологической оценки установлено, что яблочное сырье (яблочные выжимки, смесь кожуры и семян, а также дефектное и нестандартное сырье) может служить полноценной питательной средой для молочнокислых бактерий.
Содержащиеся в яблочном сырье макро- и микроэлементы, витамины оказывают положительное влияние на биосинтез молочной кислоты.
Подготовка яблочного сырья к сбраживанию включает стадию измельчения и резки. Размеры частиц яблочной мезги должны составлять от 2 до 5 мм. Оптимальным является режим разваривания яблочного сырья при гидромодуле 2,5 в течение 30 мин при 120 °С.
Эффективное расщепление полисахаридов яблочного сырья возможно с помощью ферментных препаратов пекто- и целлюло- литического действия. После проведения ферментативной обработки и последующего брожения среда лучше подвергается фильтрации и дальнейшим конечным производственным операциям, что является положительным фактором при промышленном производстве.
Возможно использование ферментных препаратов в концентрациях: Пектофоетидина П10Х – 0,03%, Целлюлазы – 0,06% массы сырья. Режим обработки ферментами – 1ч при температуре 32...35 °С.
При ферментации полисахаридов яблочного сырья можно технологически совместить стадии ферментативной обработки сырья и культивирования бактериальной культуры.
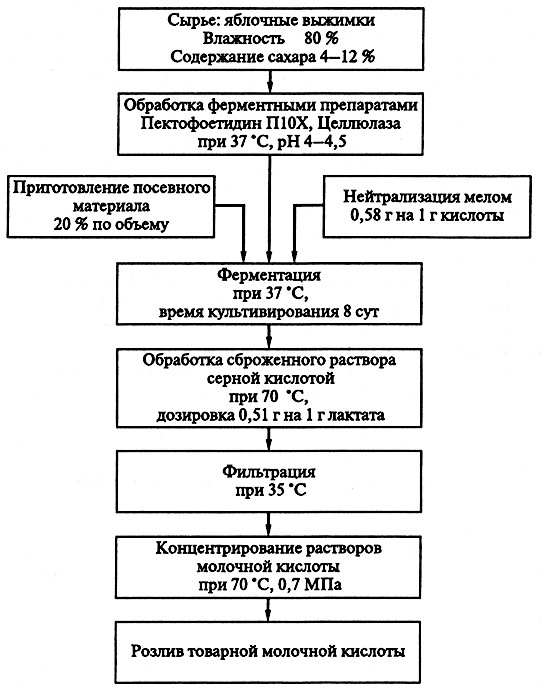
Рис. 18.5. Принципиальная технологическая схема получения молочной кислоты из яблочных выжимок
Культура Lactobacillus plantarum BKM 578 обеспечивает на яблочном сырье достаточно продолжительный и стабильный синтез молочной кислоты при начальной концентрации углеводов 4,5–5%. Наилучшие показатели достигаются в случае дробной подачи сгущенного яблочного сока до содержания в среде СВ 15 %.
Раствор молочной кислоты, полученный на яблочном сырье, представляет собой коричневую или темно-коричневую жидкость.
Очистка получаемой молочной кислоты от примесей осуществляется активированным углем марки БАУ А, наилучший режим осветления: температура 50 °С, дозировка активированного угля 4 %, время экспозиции 30 мин.
Принципиальная технологическая схема представлена на рисунке 18.5.
Возможно получение молочной кислоты из пшеничной муки II сорта (сырья с невысокой стоимостью) с использованием в качестве продуцента бактерий вида Streptococcus bovis.
Str. bovis обладает способностью гидролизовать сырой зерновой крахмал, поэтому для организации производства молочной кислоты не требуется сложного оборудования.
Осуществляют ферментацию сред с мукой II сорта, содержащих 5–20 % Сахаров, концентрация посевного материала составляла 5–20%.
Молочную кислоту выпускают в виде 40%-го раствора и концентрата, содержащего не менее 70 % кислоты. В пищевых продуктах разрешено использование ее солей: лактатов натрия, калия, кальция, аммония и магния, которые вводят в пищевую систему отдельно или в комбинации. Молочная кислота используется в производстве пива, кваса, безалкогольных напитков, карамельных масс, кисломолочных продуктов, ограниченно – в продуктах детского питания.
18.4. ДРУГИЕ ОРГАНИЧЕСКИЕ КИСЛОТЫ,
ПОЛУЧАЕМЫЕ МИКРОБИОЛОГИЧЕСКИМ ПУТЕМ
Винная, или виннокаменная, кислота (СООНС-НОНСНОНСООН) в свободном виде или в виде солей часто встречается в природе. Она входит в состав многих плодов и овощей, выделяется в виде кальциевых солей при изготовлении вин. Винную кислоту можно получать из остаточных винных дрожжей. С этой целью разработаны эффективные технологические приемы. Микробиологическим путем винную кислоту возможно получить из глюкозы с помощью бактерий Gluconobacter suboxydans. В результате жизнедеятельности этих бактерий глюкоза окисляется в глюконовую кислоту, которая затем превращается в 2- и 5-кетоглютаровую кислоты. Последняя распадается на винную и гликолевую кислоты. Однако до сих пор винную кислоту выгоднее получать химическим путем из винного камня, который накапливается на внутренней поверхности емкостей в процессе выдержки вина.
Винная кислота не оказывает какого-либо существенного раздражающего действия на слизистые оболочки желудочно-кишечного тракта и не подвергается обменным превращениям в организме человека. Основная часть (около 80 %) разрушается в кишечнике под действием бактерий. Винная кислота применяется в кондитерских изделиях и в безалкогольных напитках.
Яблочная кислота (СООНСН2СНОНСООН) приобретает все большее значение. Она содержится во фруктах. Ее получают путем химического синтеза из малеиновой кислоты, предшественником которой является фенол, но возрастающий спрос на яблочную кислоту стимулирует разработку способов ее микробиологического синтеза с помощью дрожжей родов Candida и Pichia.
Пищевыми добавками являются соли яблочной кислоты – малаты аммония, натрия, калия и кальция. Яблочная кислота обладает химическими свойствами оксикислот. При нагревании до 100 °С превращается в ангидрид. Применяется в кондитерском производстве и при получении безалкогольных напитков.
Глюконовая кислота [СН2ОН(СНОН)4СООН] образуется из глюконо-5-лактона, который представляет собой продукт ферментативного окисления D-глюкозы, катализируемого в аэробных условиях ферментом глюкозооксидазой:
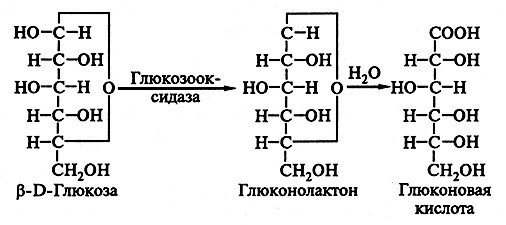
Гидролиз глюконо-8-лактона с образованием глюконовой кислоты зависит от температуры, концентрации и рН раствора, что создает возможность регулирования выхода глюконовой кислоты.
Продуцентами глюконовой кислоты служат микроскопические грибы родов Aspergillus и Penicillium. Глюконовую кислоту можно получать как при поверхностном, так и при глубинном культивировании, применяя при этом концентрированные (30–35 %) растворы глюкозы. Кроме глюкозы сбраживаемая среда обычно содержит MgSО4-7H2О, КН2РО4, (NH4)2HPО4 и СаСО3. Среда засевается проросшей культурой гриба A. niger. Брожение заканчивается, когда содержание сахара в среде становится менее 1 %.
Чаще всего готовый продукт получают в виде соли кальция. Сброженный раствор фильтруют и нейтрализуют глюконовую кислоту. Кристаллизацию глюконата кальция проводят при температуре ниже 20 °С в течение 24–48 ч. Кристаллы глюконата кальция отделяют от маточного раствора на центрифуге и дважды промывают холодной водой, а затем высушивают при температуре не выше 80 °С.
Глюконовую кислоту применяют в качестве регулятора кислотности и разрыхлителя в продуктах из мясных фаршей (сосисках, сардельках и т.п.) и десертных смесях.
Пропионовую кислоту (СН3СН2СООН) используют в пищевой промышленности главным образом в виде солей – пропионатов натрия, калия и кальция. Антимикробное действие про- пионовой кислоты в значительной степени зависит от рН консервируемого продукта, ее можно использовать для консервирования пищевых продуктов с высокими значениями рН. Она обладает более слабым микробным действием, чем другие консерванты.
Микробный синтез пропионовой кислоты осуществляют факультативно анаэробные бактерии рода Propionibacterium. Большинство видов пропионовокислых бактерий были выделены из микрофлоры сыра, рубца и кишечника жвачных животных. При производстве сыра пропионовокислые бактерии способствуют образованию специфического вкуса и запаха.
Среди многих бактерий для промышленного получения пропионовой кислоты используют виды Pr. shermanii, Pr. rubrum, Pr. arabinosum и др. Пропионовокислые бактерии получают энергию в результате брожения. Они растут и синтезируют пропионовую кислоту на питательных средах с лактозой, глюкозой, мальтозой, сахарозой, глицерином, яблочной и молочной кислотами и др.
Пропионовокислые бактерии сбраживают различные сахара с образованием пропионовой и уксусной кислот и выделением СО2. Но наиболее характерная их особенность – способность сбраживать молочную кислоту, которая затем частично восстанавливается ими до пропионовой кислоты, частично дает начало образованию уксусной кислоты и СО2.
В промышленных условиях пропионовую кислоту получают методом анаэробного глубинного культивирования на питательных средах, содержащих глюкозу (2 %), источники органического азота, например дрожжевой экстракт (0,4 %), а также соли молочной кислоты. Процесс протекает 7–12 сут при рН 6,8–7,2 и температуре 30 °С. Более 75 % сброженного сахара превращается в пропионовую и уксусную кислоты (5:1), менее 20 % расходуется на образование СО2.
Пропионовую кислоту применяют при производстве сыров и в хлебопечении. Она влияет на вкус и запах пищевых продуктов.

