Около десяти лет назад в области исследований возобновляемых источников энергии было сделано замечательное открытие. Было показано, что если взять мембраны, содержащие хлорофилл, и добавить к окружающему раствору ферменты, действующие как катализаторы, то на свету будет происходить разложение воды (фотолиз) на водород и кислород (рис. 2.6).
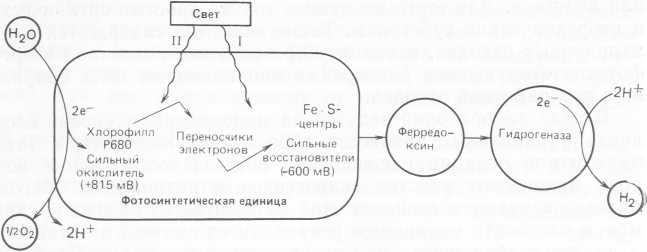
Рис. 2.6. Схема сопряжения процессов поглощения солнечной энергии и образования водорода на основе стабилизированных хлоропластных мембран и гидрогеназных ферментов (Hall, 1982).
Это открытие было первым шагом на пути к созданию фотореактора, при помощи которого энергия Солнца может запасаться в ценном топливе — водороде. Фотохимики и фотобиологи проявляют большой интерес к этим исследованиям, поскольку получение «солнечного водорода» из воды открывает новые перспективы в энергетике. Процессу фотолиза присущ ряд особенностей, которых нет у каких-либо других систем преобразования энергии. Субстратом в нем является обычная вода, источником энергии с неограниченным запасом-—солнечный свет, а продуктом — водород. Его просто хранить, он не загрязняет окружающую среду. Процесс этот циклический, поскольку при потреблении водорода регенерируется субстрат — вода. Система привлекательна и тем,, что она работает при обычной температуре; в ней не образуются токсичные промежуточные соединения.
Задача создания стабильной биологической системы, способной работать многие годы, а не часы, чрезвычайно сложна и,, быть может, нерешаема. Если бы мы смогли понять суть биологических процессов, нам, возможно, удалось бы их имитировать путем создания полной системы синтеза. Такие системы могли бы использовать свет любой интенсивности в широком диапазоне температур и этим напоминали бы производящие электроэнергию солнечные батареи. Надо сказать, что фотобиологический способ производства водорода не вышел еще из стен лабораторий. Целесообразность его дальнейшего развития только предстоит доказать в ходе многоплановых исследований. Впрочем, наши представления о возможностях использования этой системы в практике могут быстро измениться: достаточно будет и одного крупного открытия при изучении фотобиологических и фотохимических реакций разложения воды.
Несмотря на успешные опыты по стабилизации мембран хлоропластов (для этого применялась иммобилизация ферментов и- закрепление их в пленках альгинатного геля и полиуретановых матрицах), они вряд ли войдут как составная часть в промышленные системы по улавливанию солнечной энергии. Тем не менее результаты изучения состава хлоропластов и обмена веществ в них могут послужить основой для создания таких систем. Чего же мы можем ожидать от исследований в этой области? В реакциях фотолиза воды в мембранах хлоропластов, идущих при участии фотосистемы II, принимает участие комплекс белков с хлорофиллом и магнием. Сегодня нам мало что известно и о расположении в нем ионов магния, и о механизмах фотолиза воды в растениях.
Для практических целей может оказаться необходимым отделить активируемую светом стадию фотосинтеза, на которой образуется кислород, от стадии темновых реакций, где выделяется водород. Одностадийная система будет продуцировать смесь кислорода и водорода, и их улавливание и разделение со всей площади коллектора солнечной энергии могут оказаться невыполнимыми. Но можно представить себе и двухстадийный процесс, на первом этапе которого будет функционировать фотока- талитическая система, в которой образуются неокисляемый переносчик и кислород. Кислород можно улавливать, а образовавшийся переносчик водорода будет использоваться на второй стадии, когда осуществляется темновая реакция образования водорода. Вслед за этим переносчик направляется обратно в первый отсек установки, восстанавливается там в ходе световой реакции и может использоваться для повторного цикла реакций.
Переломный момент в проводимых сегодня исследованиях наступит, когда удастся разработать эффективную стабильную* систему, имитирующую фотосистему II мембран хлоропластов, т. е. процесс, в ходе которого вода разлагается на кислород и водород с образованием протонов и восстановительных эквивалентов. Со вторым этапом, связанным с выделением водорода в системе, ситуация, видимо, обстоит проще, поскольку в нашем распоряжении есть большой выбор необходимых переносчиков электронов и катализаторов образования водорода. Отметим, однако, что чувствительность многих этих веществ к кислороду ограничивает возможность их применения. Очень важно отыскать соединение, которое могло бы выполнять функции гидрогеназы, т. е. служить кислородоустойчивым редокс- и протонным переносчиком.
Остановимся теперь на водородном фотореакторе. Если бы нам удалось обойтись без реакции расщепления воды и просто шспользовать восстановленные соединения, например аскорбиновую кислоту, сульфид натрия, ЭДТА или дитионит в качестве .доноров электронов, то можно было бы без труда получить стабильную систему, интенсивно образующую водород. В роли •фотокатализатора в ней мог бы выступить какой-нибудь пигмент (например, флавин или даже стабильная фотосистема I мембран хлоропластов), а в роли переносчиков протонов и электронов— красители, гидрогеназа или платина. Можно использовать для этого стабильные ферменты и иммобилизованные системы. Уже созданы небольшие фотореакторы, в которых при надлежащих условиях образование водорода идет с высокой •скоростью, до нескольких литров H2 в минуту.
Не так-то просто будет получить искусственные мембраны .для замены нестабильных биологических прототипов, но исследования в этом направлении уже ведутся. Делаются попытки применить для этой цели различные решетки с набухающим слоем, силикаты глин (монтмориллониты и гекториты). Последние, как известно, способны образовывать стабильные интерка- ляционные соединения с разнообразными ионными комплексами и полярными молекулами, например с водой.

