7.1. Роль и значение ферментов
Ферменты, или энзимы, – это биологические катализаторы, обладающие способностью избирательно катализировать многие химические превращения как в живой клетке, так и вне организма. Еще русский физиолог И.П. Павлов называл их истинными двигателями всех природных процессов.
Ферменты нетоксичны, работают при нормальных условиях, обладают высокой специфичностью и эффективностью действия, сохраняют свои свойства вне клетки. Все это позволяет применять их в качестве экологически чистых и недорогих биокатализаторов для технологических процессов в химической, текстильной, кожевенной, пищевой, сельскохозяйственной и других отраслях промышленности.
Значительна роль ферментов в фармакологии и медицине (рис. 7.1). Их широко используют в заместительной терапии при лечении большого числа заболеваний. Так, амилазы, липазы, пепсин, трипсин и химотрипсин (в виде ферментных препаратов и их смесей – фестал, панзинорм, мезим и др.) применяют для лечения заболеваний желудочно-кишечного тракта и печени; протеазы – для лечения злокачественных новообразований; плазмин (фибринолизин), стрептокиназу, урокиназу – для растворения тромбов в кровеносных сосудах; β-галактозидазу – для восстановления способности к усвоению молочных продуктов у людей, страдающих недостаточностью этого фермента в желудочно-кишечном тракте. Эластаза задерживает развитие атеросклероза.

Рис. 7.1. Использование ферментных препаратов в промышленности
Изменение уровня активности определенного фермента или соотношения его множественных форм и изоферментов позволяет проводить диагностику заболевания того или иного органа (энзимо диагностика). Например, повышение в сыворотке крони активности фруктозо-1,6-дифосфатальдолазы свидетельствует об инфекционном гепатите, раке печени, инфаркте миокарда; повышение в плазме крови активности креатинкиназы – о мышечной дистрофии, а возрастание активности аланинаминотрансферазы – о болезнях печени и т. д.
Ферменты применяют при создании новых технологий очистки сточных вод, а также при использовании содержащихся в них веществ. Например, во Франции активно внедряется новая технология производства кормовых белков из аминокислот и пептидов сточных вод. Она основана на открытой А.Я. Данилевским в 1886 г, реакции пластеинообразования (образование белковоподобных веществ – пластеинов), в которой участвуют протеолитические ферменты.
Источником для крупномасштабного выделения ферментов служат организмы, в которых содержание требуемого фермента составляет не менее 1 %. К ним относятся бактерии (рис. 7.2), некоторые растения (например, проростки злаков, бобовых растений), отдельные ткани и органы животных (например, слизистая оболочка желудочно-кишечного тракта).
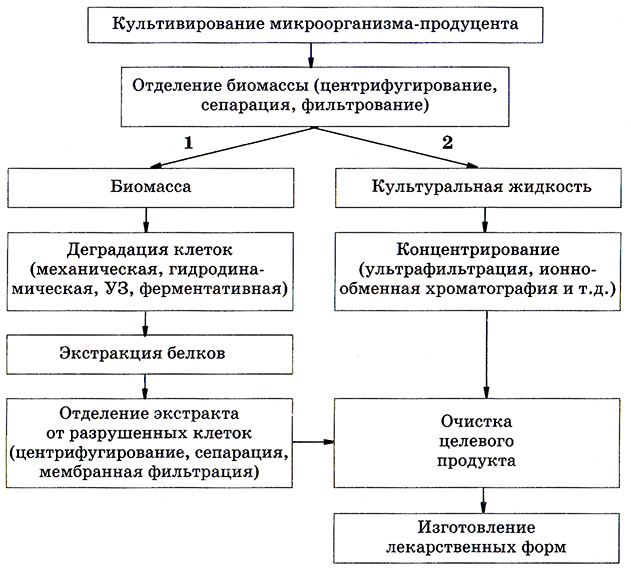
Рис. 7.2. Технология получения ферментов биотехнологическими методами:
1 – внутриклеточные ферменты; 2 – внеклеточные ферменты
Широкое применение ферментативных препаратов определяет темпы их производства и потребления. Лидерами этого направления на мировом рынке являются США, Япония и страны Западной Европы. Так, объем продаж ДНКазы составил в 2000 г. примерно 100 млн долларов.
В то же время препараты чистых ферментов имеют ряд недостатков: они достаточно дороги, нестабильны и быстро разрушаются при хранении либо требуют специальных условий хранения (низкая отрицательная температура – до –80 °С, добавление коферментов и субстратов), их невозможно использовать многократно, трудно отделить от исходных субстратов и продуктов реакции.
Решить эти проблемы удалось с помощью инженерной энзимологии – науки, появившейся в 1960-е гг. и создавшей иммобилизованные ферменты. Достижения инженерной энзимологии дали начало развитию нового направления аналитической химии – безреагентных методов анализа, основанных на использовании различных биохимических сенсоров. Наличие в устройстве биоматериала с уникальными свойствами позволяет с высокой селективностью определять нужные соединения в сложной по составу смеси, не прибегая ни к каким дополнительным операциям, связанным с использованием других реагентов, концентрированием и т. д. (отсюда и название – безреагентные методы анализа).
7.2. Иммобилизованные ферменты
Иммобилизованными называют такие ферменты, которые выделены из клетки, искусственно закреплены на носителе и сохраняют свойственную им каталитическую активность.
Иммобилизация – это технология, согласно которой молекулу фермента включают в какую-либо фазу или соединяют с нерастворимым носителем. Комплекс «фермент – носитель» отделен от раствора, но при этом может обмениваться с ним молекулами субстрата, эффектора или ингибитора. В промышленных целях для иммобилизации используют главным образом энзимы, выделенные из микроорганизмов. Они примерно в 100 раз дешевле, чем ферменты животного или растительного происхождения, и более доступны.
По сравнению со свободными ферментативными препаратами, иммобилизованные ферменты имеют существенные преимущества:
- они обладают высокой стабильностью, в несколько тысяч раз превышающей стабильность свободных ферментов, и поэтому достаточно долговечны;
- они легко отделимы от реакционной среды, что позволяет получать чистые продукты реакции;
- иммобилизация дает возможность многократно использовать ферментативный препарат;
- иммобилизованные ферменты технологичны, что позволяет либо вести процесс непрерывно, регулировать его скорость и, соответственно, выход продукта, либо в любой момент остановить реакцию;
- с помощью подбора носителей и методов иммобилизации можно целенаправленно изменять некоторые свойства ферментов (специфичность, рНи температурозависимость, стабильность) для оптимизации процесса.
Процесс иммобилизации как способ сохранения активности выделенного из клетки фермента был открыт еще в начале XX в. В 1916 г. Дж. Нельсон и Е. Гриффин показали, что сахараза, адсорбированная на угле, сохраняла свою каталитическую активность. Однако первый патент на применение иммобилизованных ферментов был выдан только в 1939 г. Дж. Пфанмюлеру и Г. Шлейху, которые предложили использовать протеолитические ферменты, адсорбированные на древесных опилках, для обработки шкур животных. В 1953 г. Н. Грубхофер и Д. Шлейт разработали принципиально новый метод для иммобилизации ферментов – ковалентное связывание. Что касается термина «иммобилизованные ферменты», то он был узаконен в 1971 г. на первой конференции по инженерной энзимологии, которая проходила в США.
Носители для иммобилизации ферментов должны обладать определенными свойствами:
- высокой биологической и химической стойкостью;
- нерастворимостью;
- высокой механической прочностью;
- значительной гидрофильностью, которая обеспечивает связывание фермента с носителем в водной среде;
- достаточной проницаемостью для ферментов, коферментов, субстратов и продуктов реакции, пористостью, большой удельной поверхностью;
- легкостью активации комплекса «фермент – носитель»;
- возможностью создания различных структур (мембран, пластин, трубочек, гранул);
- низкой стоимостью.
В зависимости от структуры, носители подразделяют на природные и синтетические, органические и неорганические, полимерные и низкомолекулярные.
Природные полимерные носители по своей химической природе подразделяют на белковые (кератин, фиброин, коллаген, желатин), полисахаридные (целлюлоза, декстран, агароза, каррагинан, альгиновые кислоты и их соли, аминополисахариды – хитин и хитозан) и липидные (модель «фермент – липид» в виде монослоя или бислоя сферической формы – липосома), наиболее приближенные к естественным комплексам, существующим в клетке.
Синтетические полимерные носители подразделяют на три группы – полиметиленовые, полиамидные и полиэфирные. Благодаря разнообразию, механической прочности и доступности, они широко используются для иммобилизации. Кроме того, при производстве синтетических полимеров можно значительно разнообразить их форму (гранулы, трубочки и т. д.), варьировать величину пор, вводить различные функциональные группы.
Носители неорганической природы могут быть представлены материалами из глины, стекла, керамики, силикагеля, графитовой сажи, а также оксидами металлов и т. д. Преимущества этой группы носителей состоят в легкости регенерации, возможности получения любой их формы при производстве и вариабельности размера пор.
Методы иммобилизации ферментов. Иммобилизацию ферментов можно осуществлять физическими и химическими методами (рис. 7.3).
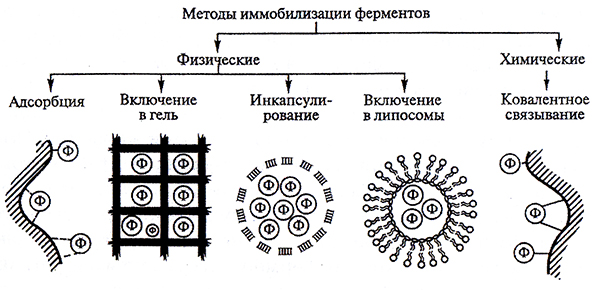
Рис. 7.3. Методы нммобплизлщш ферментов: Φ – фермент
Физические методы основаны на адсорбции фермента на нерастворимом носителе, на включении фермента в поры поперечносшитого геля, в полупроницаемые структуры.
Адсорбция ферментов на нерастворимом носителе. Молекула фермента удерживается на поверхности носителя благодаря электростатическим, гидрофобным, дисперсионным взаимодействиям или возникновению водородных связей. Прочность связывания фермента с носителем небольшая.
Иммобилизация ферментов путем включения в гель (обычно – полимерный гель). Метод обеспечивает равномерное распределение фермента в объеме носителя, достаточно прост и применяется для иммобилизации отдельных молекул определенного энзима, мультиферментных комплексов и интактных клеток. Однако он непригоден для работы с ферментами, которые воздействуют на водонерастворимые субстраты.
Иммобилизация в полупроницаемые структуры, В этом случае раствор фермента и раствор субстрата разделяют с помощью полупроницаемой мембраны (микрокапсулирование, включение в липосомы). Метод используется главным образом в фундаментальных научных исследованиях и в медицине.
Использование химических методов приводит к возникновению ковалентных связей между ферментом и носителем. Этот способ получения промышленных биокатализаторов наиболее распространен.
Химическое присоединение энзима к носителю отличается высокой эффективностью и прочностью связи. Однако химические методы иммобилизации сложны и дороги, но незаменимы в научных исследованиях при создании ферментов с контролируемыми свойствами. Рассмотрим некоторые из этих методов.
Иммобилизация на носителях, несущих гидроксигруппы. В этой группе наиболее распространен бромциановый метод, который позволяет связывать фермент с полисахаридным или синтетическим носителем.
Иммобилизация на носителях, несущих аминогруппы. Аминогруппы носителя превращают в соли диазония, к которым впоследствии присоединяют молекулы ферментов за счет взаимодействия с фенольными, аминными, имидазольными, тиольными, гуанидиновыми группами этих ферментов.
Иммобилизация на носителях, несущих сульфгидрильные группы. Если и носитель, и фермент несут сульфгидрильные группы, то под воздействием кислорода воздуха эти группы легко окисляются с образованием дисульфидных связей.
Среди всех методов иммобилизации оптимальным считается метод включения ферментов в полимерные гели. Также широко распространены адсорбционное присоединение и химические методы, основанные на ковалентном связывании. Достаточно часто иммобилизацию проводят за счет включения ферментов в мембраны и микрокапсулы, тогда как другие приемы используют в единичных случаях.
Применение иммобилизованных ферментов. Иммобилизованные ферменты находят широкое применение в различных отраслях народного хозяйства:
- в промышленности – в качестве активных компонентов стиральных и моющих средств, в дубильных процессах, в пищевых производствах, например при обработке мяса; в качестве катализаторов при проведении различных технологических процессов, для анализа различных веществ;
- в медицине – в качестве противовоспалительных, тромболитических и фибринолитических препаратов;
- в фармации – в медицинской диагностике при анализе лекарственных веществ белковой природы;
- в качестве биокатализаторов в биотехнологических производствах.
Созданы искусственные аналитические системы для анализа различных веществ – ферментные электроды, проточные анализаторы и т. д. В настоящее время разрабатываются новые поколения биодатчиков на базе аффинных взаимодействий.
О широком применении ферментов в медицине уже шла речь выше. Однако использование белковых препаратов в качестве лекарственных средств может быть ограничено их иммуногенностью, аллергенностью, малым временем действия в организме человека или животного. В связи с этим в медицине более перспективно применение иммобилизованных ферментов, которые менее аллергенны и иммуногенны, более стабильны, обладают пролонгированным действием. Например, при включении в липосомы ферменты защищены от эндогенных протеиназ организма пациента, а сами липосомы утилизируются в организме. В иммобилизованном виде применяют тромболитические ферменты, предотвращающие образование тромбов в кровеносных сосудах. Иммобилизованные протеолитические ферменты помогают при лечении ожогов, абсцессов, ран. Иммобилизованная уреаза используется в аппарате «искусственная почка». Микрокапсулы, заполненные аспарагиназой, применяют для лечения аспарагинзависимых опухолей.
7.3. Иммобилизованные полиферментные системы
Первая искусственная биферментная система, включающая ковалентно связанные с носителем иммобилизованные ферменты – гексокиназу и глюкозо-6-фосфатдегидрогеназу, была создана в 1970 г. К. Мосбахом. В настоящее время известно несколько десятков иммобилизованных полиферментных систем, состоящих из двух, трех, четырех и более энзимов. Эффективность таких комплексов намного выше, чем у свободных ферментов, за счет локального концентрирования субстрата около второго и всех последующих ферментов, входящих в систему.
Иммобилизованные полиферментные системы применяют в промышленных технологиях, иногда – в научных исследованиях при изучении метаболизма клеток, транспортных процессов и т. д. Следует, однако, отметить, что результаты, полученные с помощью таких систем, не всегда правильно отражают процессы, происходящие в клетках. Это объясняется тем, что в живых клетках комплексы энзимов чаще всего располагаются упорядоченно в мембранах клетки, что позволяет регулировать скорость протекания ферментативных процессов, тогда как в полиферментных комплексах иммобилизованные ферменты связываются с носителем случайным образом.
Современные методы иммобилизации позволяют создавать не только полиферментные комплексы, связывать с носителями удается субклеточные структуры и даже целые клетки. Такие системы очень удобны, поскольку можно, не выделяя чистые ферментные препараты, получать естественные полиферментные системы, осуществляющие многостадийные процессы.
7.4. Биосенсоры
Биосенсоры – это аналитические устройства, в которых чувствительный слой, содержащий биологический материал, реагирует на присутствие определяемого компонента и генерирует электрический сигнал, функционально связанный с наличием и концентрацией этого вещества. Биоматериалом могут служить ферменты, ткани, бактерии, дрожжи, антигены/антитела, липосомы, органеллы, рецепторы, ДНК, а также клетки, которые иммобилизованы на физических датчиках. Следовательно, биосенсорная технология сочетает в себе достижения биологии и современной микроэлектроники.
Идея создания такого рода устройств возникла сравнительно недавно, в 1960-х гг. Впервые ее высказали JI. Кларк и К. Лионе в 1967 г. Идея Кларка состояла в использовании ферментного электрода, т. е. электрохимического датчика с иммобилизованным на его поверхности ферментом. Затем в обиход вошло понятие «биосенсор».
Большинство биосенсоров используется для анализа биологических жидкостей. Так, в крови находятся тысячи различных соединений, и бывает необходимо быстро и эффективно определить концентрацию нужного соединения, например глюкозы. Для людей, страдающих диабетом, это жизненно важный клинический анализ. Биосенсоры обеспечивают такую возможность.
Функционально биосенсоры сопоставимы с датчиками живого организма – биорецепторами, способными преобраловывать все типы сигналов, поступающих из окружающей среды, в электрические.
Принципы конструирования биосенсоров. Конструктивно биосенсор представляет собой устройство, состоящее из двух преобразователей, или трансдьюсеров, – биохимического и физического, находящихся в тесном контакте друг с другом (рис. 7.4).
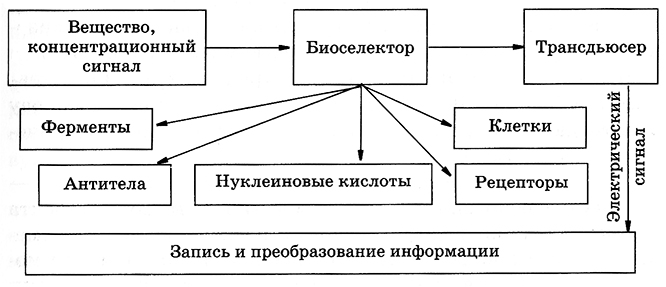
Рис. 7.4. Схема биосенсора
Биохимический преобразователь сигнала (или биотрапсдьюсер, биоселектор) выполняет функцию биологического элемента распознавания, преобразуя определяемый компонент (а точнее, информацию о химических связях) в физическое или химическое свойство или сигнал. В этом качестве выступают все типы биологических структур: ферменты, антитела, рецепторы, нуклеиновые кислоты и даже живые клетки.
Физический преобразователь сигнала (или трансдьюсер) преобразует определяемый компонент (а точнее, концентрационный сигнал) в электрический с помощью специальной аппаратуры. Для считывания и записи информации используют электронные системы усиления и регистрации сигнала. Существует большое разнообразие физических трансдьюсеров: электрохимические, спектроскопические, термические, пьезоэлектрические, различного рода оптические преобразователи, гравитационные, калориметрические, резонансные системы и т. п.
Все виды биоселектирующих элементов можно комбинировать с различными трансдьюсерами и тем самым создавать большое разнообразие различных типов биосенсоров.
Основными характеристиками, позволяющими биосенсорному анализу успешно конкурировать с традиционными методами, являются оперативность анализа, высокая специфичность и чувствительность при низкой стоимости, отсутствие необходимости использовать дорогостоящую аппаратуру.
Наличие в устройстве биоматериала с уникальными свойствами позволяет с высокой селективностью определять нужные соединения в сложной по составу смеси.
Разновидности биосенсоров и их применение. Разработка биосенсоров относится к наукоемким технологиям и представляет собой одну из ветвей современной биотехнологии. Существует несколько типов биосенсоров, среди которых наибольшее развитие получили ферментные и клеточные биосенсоры.
Ферментные биосенсоры могут быть представлены ферментными электродами, ферментными микрокалориметрическими датчиками, биодатчиками на основе хемии биолюминесценции.
Ферментные (или безреагентные) электроды – устройства основаны на применении электрохимического способа определения веществ, образующихся в ходе ферментативного превращения. Представляют собой электрод с нанесенным поверхностным слоем (каким-либо природным полимером), содержащим один или несколько иммобилизованных ферментов (иногда фермент может находиться в растворенном состоянии в приэлектродном слое, окруженном мембраной). В зависимости от типа взятого за основу электрода, устройства подразделяют на потенциометрические и амперометрические.
Ферментные микрокалориметрические датчики – устройства основаны на использовании теплового эффекта ферментативной реакции. Состоят из двух колонок (измерительной и контрольной), заполненных носителем с иммобилизованным ферментом и снаряженных термисторами. При пропускании через измерительную колонку анализируемого образца происходит химическая реакция, которая сопровождается регистрируемым тепловым эффектом. Данный тип датчиков интересен своей универсальностью.
Хеми- и биолюминесцентные датчики – регистрируют световое излучение с различной длиной волны, испускаемое продуктами ферментативной реакции, находящимися в возбужденном состоянии. Конструкция включает колонку с иммобилизованными на носителе ферментами (люциферазой, пероксидазой) и светоприемное устройство. Заложенный в систему этого типа датчиков аналитический метод характеризуется прежде всего крайне высокой чувствительностью, позволяя определять фемтомольные (10–12 М) количества вещества.
Электроды, в которых применены иммобилизованные ферменты, во много раз долговечнее и позволяют провести несколько сот измерений, тогда как электроды, в которых используются естественные ферментные препараты, – только около 50.
В настоящее время наиболее распространен амперометрический биосенсор для определения сахара в крови (на основе иммобилизованной глюкозоксидазы). В качестве физического трансдьюсера в нем использован так называемый электрод Кларка. Исторически этот биосенсор является самым «древним».
Для контроля содержания пенициллина в питательной среде для выращивания бактерий используют пенициллиновый электрод – рН-датчик, покрытый иммобилизованным ферментом пенициллазой.
Биосенсоры, основанные на кислородном электроде как физическом трансдьюсере, позволяют определять разнообразные субстраты ферментов: лактаты, L-аминокислоты, салицилаты, оксалаты, пируваты, т. е. анионы соответствующих карбоновых кислот.
С помощью биосенсоров можно решать и обратную задачу: при некоторой определенной концентрации субстрата оценивать активность собственно фермента по величине измеряемого сигнала (потенциала, тока и т. д.). Из описания работы фермента следует, что измеряемый сигнал зависит не только от концентрации субстрата, но и от каталитической активности биологического преобразователя, т. е. фермента. Такое применение биосенсоров позволяет измерить активность большого числа ферментов, например, в крови. Оценка активности ферментов, связанных с сердечной деятельностью (таких, как аспартамаминотрансфераза, креатинкиназа), дает возможность в клинических условиях оценивать глубину инфаркта миокарда. Измерения активности фермента амилазы используют в педиатрии.
Клеточные биосенсоры. Одно из достижений биотехнологии связано с развитием методов включения живых клеток в полимеры и твердые носители различной природы и применением такого рода материалов для решения задач медицины и управляемого биосинтеза.
Методы иммобилизации клеток – физические и химические – сходны с методами иммобилизации отдельных ферментов. Стабильность иммобилизованных клеток определяется их метаболизмом, свойствами носителя и среды.
Наибольшее применение для иммобилизации нашли клетки микроорганизмов, которые легко культивируются, воспроизводятся и поддерживаются в чистой культуре, а также клетки растений, животных, человека. В отличие от ферментов, при их использовании не требуется дорогостоящих стадий очистки.
Имеющиеся методы позволяют получить клетки, сохраняющие около 100 % активности ферментов и способные функционировать достаточно длительные промежутки времени (в некоторых случаях такие клетки сохраняют жизнеспособность и активность ферментных систем в течение нескольких лет). Клетки, как правило, сохраняют все системы жизнеобеспечения, что позволяет проводить сложные последовательные реакции, осуществляя многостадийные процессы.
Для многих типов клеток, особенно микробных, разработаны эффективные методы генетических трансформаций, позволяющие получать мутанты с высоким содержанием того или иного белка или фермента, что дает возможность оперировать с высокоэффективными каталитическими системами. Клетки сохраняют аппарат биосинтеза белка. На основе этого могут быть разработаны высокоэффективные методы генодиагностики.
Основные недостатки клеточных биосенсоров заключаются в медленном отклике электрода (что связано с необходимостью использовать толстые мембраны), а также в сравнительно низкой селективности, обусловленной присутствием в клетке или тканях нескольких ферментных систем. В процессе роста и размножения интактные клетки разрушают носитель, а дочерние клетки загрязняют получаемый продукт. Эта проблема решается торможением роста, что достигается созданием дефицита фитогормонов для иммобилизованных клеток растений либо добавлением антибиотиков при применении клеток бактерий.
Для создания биосенсоров используют различные микроорганизмы: Neigrospora еигореа – для определения аммиака, Trichosporon brassicae – для определения уксусной кислоты, Sarcina flava – для определения глутамина, Azotobacter vinelaudit – для определения нитратов и др. На основе гриба Aspergillus niger группой японских ученых созданы биосенсоры для определения биогенных аминов в мясных продуктах. В тканевых электродах нашли применение срезы почек и печени свиньи, желтой тыквы, банана и др.
Первоначально для иммобилизации клеток с сохранением их активности применяли материалы природного происхождения: желатин, агар, альгинат кальция, каррагинан. В последние годы разработаны и развиты методы включения живых клеток в синтетические полимерные гели.
В пищевой, фармацевтической, текстильной, металлургической, химической и других отраслях промышленности используется большое количество разнообразных химических соединений: органических кислот и их солей, аминокислот, витаминов и т. д. Эти вещества можно синтезировать как химическим, так и биотехнологическим способом. Причем биотехнологический синтез предпочтительнее для пищевой и фармакологической промышленности, так как в этом случае продукты получаются более чистыми и дешевыми.
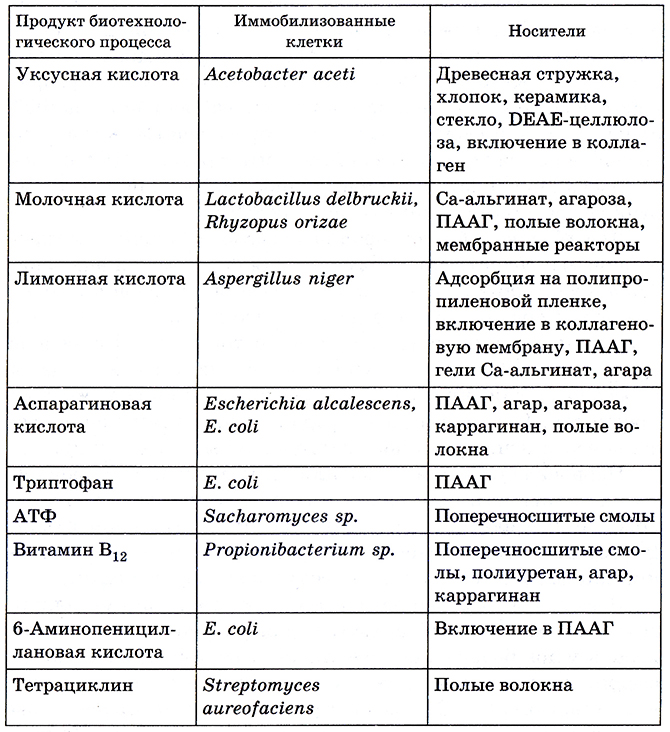
Иммобилизованные клетки нашли применение в различных отраслях народного хозяйства для синтеза разнообразных химических соединений биотехнологическим способом (табл. 4).
Таблица 4. Промышленное применение клеточных биосенсоров
Биосенсоры можно использовать также для:
- измерения пищевой ценности, свежести и безопасности продуктов питания;
- экспресс-анализа крови непосредственно у кровати больного;
- обнаружения и измерения степени загрязнения окружающей среды:
- детекции и определения количества взрып'штмх веществ, токсинов и возможного биологического оружия;
- извлечения металлов из сточных вод;
- изготовления водородных солнечных элементов;
- очистки природных и сточных вод.
Распознавание определяемого вещества с помощью иммобилизованного биоматериала оказалось востребованным. Некоторые биосенсоры уже получают распространение для индивидуального применения в домашних аптечках (чаще всего для определения уровня сахара в крови). На очереди разработка конструкций биосенсоров, заменяющих рецепторы живых организмов, что позволит создать «искусственные органы» обоняния и вкуса, а также применять подобные разработки для возможно более точной и информативной диагностики ряда заболеваний.
7.5. Биочипы
Успехи в области развития молекулярной биологии и микроэлектроники подтолкнули разработчиков конструкций биосенсоров к новым решениям. Оказалось перспективным использовать так называемую планарную технологию (фотолитографию, полупроводниковую технику покрытий и т. д.) для изготовления биочипа, объединяющего сенсорную систему, трансдьюсер, аналого-цифровой преобразователь и микропроцессор с целью измерения аналитического сигнала и расчета результатов анализа.
Прообразом современных биочипов послужил Саузернблотт, изготовленный в 1975 г. Э. Саузерном. Он использовал меченую нуклеиновую кислоту для определения специфической последовательности фрагментов ДНК, зафиксированных на твердой подложке. В России ученые начали активно разрабатывать биочипы только в конце 1980-х гг. в Институте молекулярной биологии РАН под руководством А.Д. Мирзабекова.
Технология микрочипов – это принципиально новый уровень лабораторных исследований, который позволяет проводить одновременное тестирование тысяч образцов. Тысячи молекул ДНК или белков помещают на пластинки для создания соответственно ДНК-чипов или белковых чипов. Эти миниатюрные приборы используют для анализа специфических взаимодействий биологических макромолекул. Зондами в таких чипах могут служить олигонуклеотиды, фрагменты геномной ДНК, РНК, белки, рецепторы, лиганды и др.
За короткое время биочипы выделились в самостоятельную область анализа с приложениями – исследования фундаментальных проблем молекулярной биологии и молекулярной эволюции до практического применения в медицине, фармакологии, экологии, судебно-медицинской экспертизе и др.
Биочип и принцип его работы. Существует несколько разновидностей биочипов – матричные (с иммобилизованной ДНК), микрофлюидные (капиллярные) и биочипы с использованием микросфер с цветовой кодировкой.
У современных микрочипов размеры ячеек лежат в пределах 50-200 микрон; характерные объемы, относящиеся к отдельной ячейке, составляют примерно от 1 нл до 1 мкл; значения концентраций анализируемых макромолекул находятся обычно в пределах до 10 мкМ. Общее число ячеек на чипе составляет 103-105, а его линейные размеры составляют приблизительно 1 см.
Микрозонды, которые должны взаимодействовать с образцом, наносят на подложку размером не больше почтовой марки. Каждый микрозонд имеет форму капельки, составляющей около 100 микрон в поперечнике. Все ячейки одного микрозонда одинаковы по размеру и располагаются с плотностью 10-30 «капелек» на 1 мм2. Чипы, на которых проходит ферментативная реакция, имеют более редкое расположение ячеек, чем чипы, на которых идет ДНК-реакция. Такая технология позволяет на одном биочипе разместить анализатор фактически всего генома человека – от 30 до 100 тыс. генов. При этом детектируется наличие участков ДНК длиной от шести до нескольких тысяч нуклеотидов – в зависимости от поставленной задачи.
Чаще всего для изготовления чипов служат пластинки из стекла, пластика, полупроводника или металла, на которые наносят биологические макромолекулы (ДНК, белки, ферменты), способные избирательно связывать вещества, содержащиеся в анализируемом растворе.
Во всех многопараметрических биочипах используют какой-либо механизм химического взаимодействия. Молекулы исследуемого образца соединяются со своей «парой» (микрозондом), помещенной в одну из нескольких тысяч ячеек на чипе. Например, нити ДНК соединяются со своей комплементарной парой, антиген – со своим антителом, субстрат – со своим ферментом. Наличие того или иного вещества или гена в образце определяют по люминесцентному свечению на прореагировавшем чипе. Флуоресценция является основным, но далеко не единственным методом изучения гибридизации. В частности, данные о характере гибридизации можно получить также с помощью массспектрометрии, атомной силовой микроскопии и др.
В зависимости от того, какие макромолекулы используются, выделяют различные виды биочипов, ориентированные на разные цели. В настоящее время преобладает производство ДНК-чипов (94 %), т. е. матриц, несущих молекулы ДНК. Оставшиеся 6 % составляют белковые чипы.
В основе принципа работы всех типов биочипов с иммобилизованной ДНК лежит точное соответствие между прямой и комплементарной ДНК по правилу Уотсона – Крика (А/Т или G/C). Гибридизуемая ДНК обычно заранее нарабатывается в достаточных количествах с помощью полимеразной цепной реакции (ПЦР). Далее в ходе реакции на чипе происходит взаимодействие комплементарных цепей ДНК: одна из них с известной последовательностью нуклеотидов зафиксирована на пластине, а другая одноцепочечная ДНК-мишень, меченная флуоресцентной меткой, наносится на ДНК-чип.
Иммобилизуемая ДНК наносится на поверхность через игольчатые растры (пины) механического робота или с помощью технологии типа струйного принтера. Гибридизуемая ДНК в растворе метится с помощью флуоресцентной или радиактивной метки. Свойства флуоресцентного красителя не должны сильно зависеть от состава ДНК (А/Т или G/C) и температуры.
При взаимодействии биочипа с исследуемым образцом, предварительно обработанным светящимся (флуоресцентным) красителем, в соответствующих ячейках происходит химическая реакция, и тогда эти ячейки начинают светиться – тем сильнее, чем интенсивнее процесс. Анализ прореагировавших чипов производится автоматически с помощью анализатора (чип-детектора), который представляет собой широкопольный микроскоп, соединенный с видеокамерой и компьютером. По сути, именно в выявлении и сопоставлении наиболее ярко светящихся ячеек и заключается работа прибора – анализатора биочипов. Так определяются различные характеристики образца, например присутствие в организме тех или иных возбудителей инфекций или наличие в геноме каких-либо измененных генов.
В гелевых биочипах ДНК иммобилизуется в слое полиакриламидного геля толщиной 10-20 микрон, нанесенного на специально обработанную поверхность стекла. Иммобилизация осуществляется за счет образования ковалентных связей с помощью фотореакции при облучении ультрафиолетовым излучением. В гелевых биочипах взаимодействие между молекулами ДНК примерно такое же, как и в растворе. Кроме того, благодаря трехмерной конфигурации ячейки, в таких биочипах общее число иммобилизуемых молекул ДНК существенно выше, чем в поверхностных микрочипах, что приводит, соответственно, к более сильному сигналу флуоресценции из ячейки.
Особенностью российских гелевых биочипов является то, что такие гели удерживают большее количество пробы, нежели двухмерные, и потому чувствительность отечественных биочипов выше, а следовательно, ниже требования к регистрирующей аппаратуре. Немаловажно и то, что реакции в объемном геле протекают так же, как и в жидкостях, т. е. как в живом организме. Это позволяет получить результат, максимально приближенный к реальности.
На Западе исследователи пошли по другому пути и разработали для создания ДНК-чипов процесс фотолитографии, аналогичный процессу производства кремниевых процессоров. Например, Affimetrix (США) создал GeneChipтехнологию, основанную на высокоплотных чипах, содержащих ДНК-последовательности.
ДНК-микрочипы применяют с целью практического использования информации, полученной в результате секвеиирования геномов человека и других живых организмов, а именно для:
- идентификации мутаций в генах, связанных с различными заболеваниями;
- наблюдений за активностью генов;
- диагностики инфекционных заболеваний и определения наиболее эффективного метода терапии;
- идентификации генов, важных для продуктивности сельскохозяйственных культур;
- скрининга микроорганизмов, как патогенных, так и полезных, например используемых для восстановления зараженных органическими отходами почв.
Чтобы использовать известные последовательности генов и геномных карт, необходимо определить функции входящих в их состав генов. Без белковых микрочипов эта работа очень трудоемка.
Белковые биочипы, несущие молекулы, «чувствительные» к различным низкомолекулярным соединениям, уже в скором будущем позволят определять наличие широкого спектра лекарственных веществ, гормонов, наркотиков, ядов, пестицидов практически в любом анализируемом материале (кровь, вода, пища или образец почвы), а также множество различных аллергенов, онкогенов, биологически активных веществ и даже генетических дефектов. Технология белковых биочипов заменит целые иммунологические лаборатории и даст возможность увеличить производительность большинства диагностических методов в тысячи раз, резко снизив себестоимость анализов.
Белковые микрочипы предполагается использовать для:
- обнаружения белковых биомаркеров, характерных для различных заболеваний и даже разных их стадий;
- оценки потенциальной эффективности и токсичности препаратов в доклинических испытаниях;
- измерения различий в синтезе белков отдельными типами клеток; клетками, находящимися на разных стадиях
- развития; здоровыми и патологически измененными клетками;
- изучения взаимосвязи между структурой и функциями белков;
- оценки экспрессии белков с целью выявления мишеней для новых лекарственных препаратов;
- изучения взаимодействий между белками и другими молекулами.
Фундаментальный принцип, положенный в основу технологии микрочипов, вдохновил исследователей на создание большого числа устройств для решения широкого спектра научных задач и создания новых продуктов. Это тканевые и клеточные микрочипы, микрочипы на основе малых молекул.
Применение биочипов. Биочипы применяют как для исследовательских целей, так и в практической медицине. Они помогают в поиске и установлении функций различных генов. За короткий промежуток времени становится возможным проанализировать генетические мутации и выявить предрасположенность человека, например, к онкозаболеваниям (она выявляется у 60 % больных раком). В настоящее время в процессе сертификации находится биочип для диагностики лейкемии.
Поскольку существуют не только генные, но и белковые онкомаркеры (молекулы, сигнализирующие о раке), были разработаны и соответствующие биочипы. То же самое касается биозондов, определяющих совместимость при переливании крови, анализирующих организм пациентов на гепатит и СПИД.
Используя биочипы, можно диагностировать не только наследственные заболевания, но и болезни, являющиеся результатом прижизненных мутаций в генетическом коде.
Микрочипы помогают изучать молекулярные механизмы и осуществлять проверку действия различных лекарств, причем показания и противопоказания по применению препаратов можно выявлять на индивидуальном уровне.
Существенную помощь призваны оказать биочипы и при пересадке органов. Основная проблема при подобного рода операциях заключается в отторжении имплантированных тканей иммунной системой человека. Маркерами, которые находятся в каждой человеческой клетке и служат для идентификации своих клеток, являются белки главного комплекса гистосовместимости. Для того чтобы избежать отторжения, необходимо, чтобы белки-маркеры на имплантированной ткани как можно меньше отличались от белков-маркеров пациента. Биочипы облегчат подбор наиболее подходящих доноров, пересадка органов от которых вызовет минимальный иммунный ответ.
Разрабатываются также биочипы для диагностирования различных форм туберкулеза. В настоящее время появилось множество разновидностей туберкулезной палочки, устойчивых к воздействию антибиотиков. Биочип позволит выявить все известные на сегодняшний день формы возбудителя туберкулеза, а также определить, каким именно антибиотиком нужно лечить конкретную форму заболевания. Причем вероятность выявления биочипом формы заболевания туберкулезом с устойчивыми к лекарствам возбудителями близка к 100 %. Диагностику можно будет провести в течение дня, тогда как другие традиционные методы требуют нескольких недель или даже месяцев.
Биочипы можно применять для контроля за некоторыми смертельно опасными бактериями (так, есть биочипы, позволяющие определять возбудителей сибирской язвы, оспы, чумы и бруцеллеза), а также для диагностики гриппа и определения его штаммов. Российские ученые получили грант Американского центра по контролю заболеваний (CDC) для совместной работы по выявлению штаммов вирусов гриппа.
Биочипы могут работать и дистанционно. Российские ученые предоставили свои технологии и оборудование в Университет Джорджа Вашингтона в Сиэтле, а также в американскую организацию Grand CRDF, которая работает с NASA. Последний проект касается возможности обнаружения жизни вне Земли, что связано с необходимостью многопараметрического анализа с помощью автономной системы с использованием биочипов.
Приведенные примеры свидетельствуют в пользу того, что в ближайшее время технология биочипов будет стремительно развиваться, а их массовое производство приведет к резкому уменьшению стоимости этой продукции. Сейчас число размещаемых на биочипе ячеек достигает уже нескольких тысяч, что соответствует тысячам пробирок с проводимыми в них анализами. Такие биочипы представляют собой целые экспресс-лаборатории, которые позволяют сэкономить массу времени как врачам, так и пациентам. Развитие технологии использования биочипов не только приведет к резкому сокращению сроков проведения анализов, но и даст возможность осуществлять диагностику на индивидуальном уровне.

