Метод Кьельдаля. Содержание белка вычисляют на основании определения количества азота в навеске молока. Все азотсодержащие составные части молока при нагревании с концентрированной серной кислотой переходят в (NH4)2S04. При этом выделяются тяжелые пары S02, поэтому сжигание следует производить в вытяжном шкафу.
Чтобы ускорить разрушение органических соединений, добавляют в качестве катализаторов CuS04, HgO или Н202, а с целью повышения точки кипения — K2SO4 или безводный Na2S04. По окончании реакции в результате взаимодействия концентрированной щелочи с сернокислым аммонием выделяется свободный аммиак, который отгоняется из водного раствора в приемную колбу и поглощается кислотой определенной концентрации, взятой в определенном количестве.
Избыток кислоты оттитровывают щелочью. Разница между количествами взятой и остаточной кислоты составляет количество кислоты, нейтрализованной аммиаком. 1 мл 0,1 н. кислоты эквивалентен 0,0014 г азота.
Чтобы вычислить содержание белка во взятой навеске, количество азота умножают на 6,38.
10 мл молока вносят пипеткой в колбу Кьельдаля. Вес молока определяют, взвешивая отдельно молоко, вылитое из той же пипетки.
Прибавляют в колбу Кьельдаля 25 мл химически чистой кои- центрированной серной кислоты, стараясь смыть оставшееся на стенке колбы молоко, и кристаллик CuS04 (около 0,3 г). Перемешивают вращательными движениями содержимое колбы, которое сильно разогревается и чернеет. Укрепляют колбу зажимом в наклонном положении на нагревательном приборе.
В горло колбы вкладывают небольшую стеклянную воронку или грушу для предотвращения сильного выкипания кислоты, (рис. 48). Сначала содержимое колбы нагревают слабо, следя, чтобы масса сильно не вспенивалась. Когда начнут выделяться тяжелые белые пары, вносят около 10 г K2S04 и усиливают нагревание. Периодически вращая колбу, смывают с ее стенок обугливающиеся частицы молока.
После того как жидкость над белым осадком станет прозрачной, слегка зеленоватого или желтоватого оттенка, нагревание продолжают еще час.
После охлаждения содержимое колбы Кьельдаля разводят осторожно водой (при этом происходит сильное разогревание) и переносят количественно в дистилляционную колбу емкостью 750—1000 мл. Объем жидкости должен быть около 500 мл. Бросают в колбу лакмусовую бумажку, щепотку порошкообразной пемзы или 5 г мелко гранулированного цинка (для предотвращения вспенивания) и 75—80 мл 45%-ного раствора NaOH, который приливают по стенке на дно колбы, где он образует под кислотой слой.
Дистилляционную колбу 1 (рис. 48) соединяют через каплеуловитель 3 с холодильником 4 и трубкой 5, погруженной в раствор, находящийся в приемнике 2. Приемник содержит 50 мл 0,1 н. раствора НС1 или H2S04 (растворы 6 и 7) и несколько капель 0,2%-ного раствора метилрота или смешанного индикатора (раствор 18 или 22).
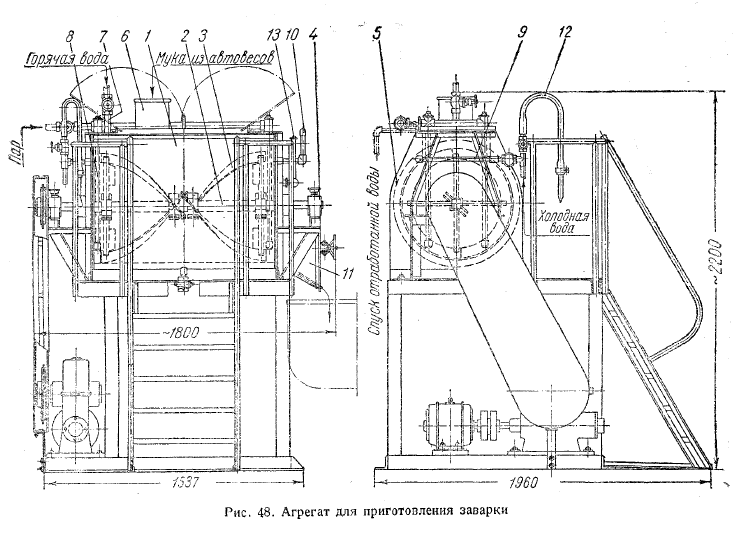
Перемешивают содержимое дистилляционной колбы, которое должно иметь щелочную реакцию, что определяют по окраске лакмусовой бумажки, и начинают перегонку, считая, что весь аммиак должен отогнаться с первыми 250 мл дистиллята.
Необходимо постоянное наблюдение за ходом перегонки, так как с уменьшением степени нагревания возможно втягивание жидкости из приемной колбы в холодильник. В случае подъема жидкости в трубке, на короткое время, не прекращая нагревания, вынимают ее из приемной колбы; поднявшаяся жидкость стекает обратно, после этого конец трубки вновь опускают в приемную колбу.
Окончание перегонки определяют лакмусовой бумажкой. Трубку 5 вынимают из жидкости приемной колбы и ополаскивают наружные стенки ее дистиллированной водой из промы- валки. Затем одной-двумя каплями стекающей из холодильника жидкости смачивают красную лакмусовую бумажку. Если выделение аммиака в дистилляционной колбе прекратилось, красная бумажка не синеет.
Если бумажка посинела, отгонку продолжают до получения отрицательной реакции на аммиак по лакмусу. При прекращении перегонки, не отнимая нагревательного прибора, отсоединяют трубку 5 от холодильника и отставляют приемную колбу с трубкой в сторону. Ополаскивают трубку снаружи и внутри водой, сливая воду в ту же приемную колбу. Избыток 0,1 н. раствора H2SO4 оттитровьгвают 0,1 н. раствором NaOH (раствор 5), окраска метилрота изменяется от красного цвета до желтого, а смешанного индикатора — от фиолетового (кислая) до зеленого (щелочная реакция). Титрование ведут осторожно; заканчивают его, прибавляя по каплям 0,1 н. раствор NaOH до ясного изменения окраски. Делают контрольный опыт, применяя все реактивы, взятые в том же количестве, что и в рабочем опыте.
Количество миллилитров 0,1 н. раствора H2SO4, вступивших в реакцию с аммиаком, а определяют по формуле:
а = 50 — (б+ в),
где: 50 — количество 0,1 и. раствора кислоты в приемной колбе в мл;
б — количество 0,1 н. раствора щелочи, пошедшее на обратное титрование H2SO4, в мл; в—количество миллилитров 0,1 н. раствора щелочи, пошедшее на контрольный опыт, в мл.
Содержание азота N вычисляют по формуле:

Содержание белка в молоке определяют, умножая количество азота в % на 6,38, т. е. % белка = 6,38И.
Разница между параллельными определениями не должна быть более 0,02 %.
В помещении, где определяют белок, не допускается работать с аммиаком или хранить его.
Сжигание с применением пергидроля (метод Верещагиной и Мещеряковой). В качестве катализатора вместо CUSO4 применяют 30%-ный раствор Н202 (пергидроль).
К 5 мл молока приливают 5 мл H2SO4 (плотность 1,833, 95%), молоко сильно нагревается и чернеет; добавляют 5 мл пергидроля, начинают нагревание. Сначала содержимое колбы обесцвечивается, но через 15—20 мин смесь снова чернеет. Охладив колбу, вновь добавляют 5 мл пергидроля и продолжают нагревание.
Пергидроль добавляют до тех пор, пока жидкость не станет бесцветной и прозрачной. Появление белых паров указывает, что процесс сжигания заканчивается. Последние порции пергидроля прибавляют по каплям и после обесцвечивания жидкость нагревают еще несколько минут. Сжигание закончено, когда бесцветная, прозрачная жидкость при охлаждении не темнеет. На 5 мл молока расходуется 15—20 мл пергидроля, сжигание заканчивается за полтора-два часа.
Аммиак перегоняют так, как указано выше. Полученные результаты на 0,1—0,2% выше, чем при анализе методом Кьельдаля.
Метод Кофрани. При нагревании белков в щелочной среде количественно с водяным паром отгоняют аммиак, который образуется главным образом в результате гидролиза двух аминокислот: глютаминовой и аспарагиновой, и только незначительная часть его — вследствие гидролиза других аминокислот.
Эти два процесса протекают с разной скоростью. В то время как гидролиз глютаминовой и аспарагиновой кислот заканчивается в течение 7 мин, полное расщепление белков происходит очень медленно.
Аммиак перегоняют в строго установленных условиях, содержание белка в процентах находят, умножая количество кислоты, связанной аммиаком, на коэффициент, найденный экспериментально, путем сравнительных определений белка в молоке по Кьельдалю.
Преимущества метода — возможность проведения анализа без вытяжного шкафа, экономия реактивов, простота выполнения анализа, который длится 15—20 мин.
В дистилляционную колбу 4 емкостью 250 мл (рис. 49) вносят 10 мл молрка, 10 мл нормального раствора NaOH и 10 мл 10%-ного раствора ВаС12 (для предотвращения пенообразования) и быстро соединяют с парообразователем 1, в котором вода была уже нагрета до кипения, а приемная колба 7, содержащая 20 мл 0,02 н. раствора H2SO4 и 7—8 капель смешанного индикатора (раствор 22), подставлена под холодильник 6.
Дистилляцию продолжают 10 мин. Для поддержания равномерного давления пара служит барометрическая трубка 3. Температура дистиллята не должна быть выше 20 °С. Через 10 мин отсоединяют приемную колбу, ополаскивают небольшим количеством воды наружный кончик трубки, погружаемой в приемник, и содержимое колбы титруют 0,02 н. раствором NaOH.
Содержание белка в молоке х в % находят по формуле:
х=0,154 а,
где: а — количество 0,02 н. раствора H2SO4, связанное с аммиаком, в мл
0,154 — коэффициент, установленный экспериментально.
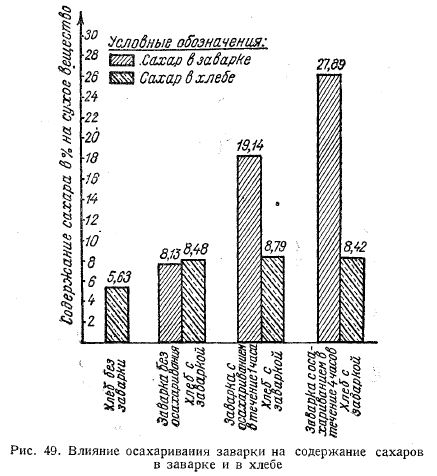
Точность анализа зависит от точного соблюдения продолжительности перегонки; при отклонении ± 1 мин разница в количестве определяемого белка достигает 0,5%. Концентрация щелочи должна быть 10 н.±0,2 н. с повышением концентрации щелочи до 10,9 н., результат завышается на 0,05—0,09%. На результат анализа влияют также неравномерное давление пара и температура дистиллята.
Для поглощения аммиака вместо 0,02' н. раствора H2SO4 можно применять 20 мл 3%-ного раствора борной кислоты и 7—8 капель смешанного индикатора (раствор 22). При перегонке следить, чтоб дистиллят хорошо охлаждался, температура его не должна быть выше 20° С.
Аммиак поглощается борной кислотой с образованием борнокислого аммония:
Борнокислый аммоний оттитровывают 0,02 н. раствором H2SO4:
2 (NH4)3B03 + 3H2S04 = 3 (NH4)3S04 + 2Н3ВО,.
При применении для поглощения аммиака борной кислоты требуется только один титрованный раствор — 0,02 н. раствор H2S04) вместо двух — 0,02 н. раствора щелочи и 0,02 н. раствора кислоты.
В этом случае в формуле для определения содержания белка а показывает количество миллилитров 0,02 н. H2S04. израсходованное на титрование борнокислого аммония.
Перед работой прибор тщательно промывают и пропускают через него пар.
Определение общего белка и казеина методом формольного титрования (по Каруниной и Шиловичу). Метод основан на свойстве нейтрального водного раствора аминокислот в присутствии нейтрального формалина повышать кислотность с образованием соединений, в которых оба Н+ аминогруппы замещаются метиленовой группой:
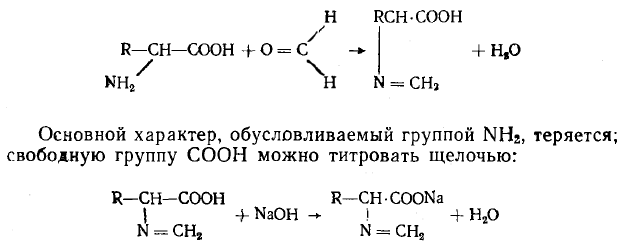
К 10 мл свежего молока (кислотность не выше 22 °Т) прибавляют 10—12 капель 1%-ного спиртового раствора фенолфталеина и титруют 0,1 н. раствором щелочи до слабо-розового окрашивания, не исчезающего при взбалтывании. После этого в эту пробу приливают 2 мл нейтрализованного формалина (раствор 34).
Содержимое взбалтывают или перемешивают стеклянной палочкой. Розовое окрашивание, появившееся при начальном титровании, исчезает. Продолжают титровать пробу щелочью до появления вновь неисчезающего такого же слабо-розового окрашивания. Количество 0,1 н. раствора щелочи, пошедшее на титрование. 10 мл молока после добавления формалина, умножают на 1,92 и получают содержание общего белка в молоке в %.
Чтобы определить содержание казеина, количество миллилитров 0,1 н. раствора щелочи, пошедшее на титрование 10 мл молока после добавления формалина, умножают на 1,51.
Метод рекомендуется только для анализа сборного молока. Получаемые результаты отклоняются от полученных методом Кьельдаля на ±0,05%, что составляет 1,4% белка.
Основным условием более точного определения общего белка и казеина методом формального титрования является одинаковая интенсивность окраски раствора при первом и втором титровании.
По результатам начального титрования можно определить кислотность молока. Так как титрование производят без воды, но с добавлением большего количества фенолфталеина, то из полученного градуса кислотности вычитают 1. Например, на начальное титрование израсходовано 2 мл. Следовательно, кислотность молока составит: 20—1= 19 °Т.
Определение общего белка методом формольного титрования (по Дуденкову). Чтобы повысить точность определения, при титровании применяют эталон окраски и добавляют к молоку нейтральный раствор гексаметафосфата, который, образуя с кальцием устойчивые растворимые комплексные соединения, исключает влияние кальция и образует более прозрачные растворы, в которых легче установить конечную точку титрования.
В химический стакан отмеривают 20 мл молока, 2 мл 20%-ного нейтрализованного раствора гексаметафосфата натрия (раствор 66), 0,25 мл 2%-ного раствора фенолфталеина и через 2 мин титруют 0,1 н. раствором едкого натра до появления розовой окраски, соответствующей эталону: смесь 20 мл молока, 2 мл раствора гексаметафосфата натрия и 1,1 —1,2 мл 0,0005%-ного раствора основного фуксина (раствор 356). Затем вносят 4 мл нейтрализованного свежеприготовленного формалина (раствор 34) и вторично титруют до той же окраски. Количество миллилитров 0,1 н. раствора NaOH, израсходованное на второе титрование, умноженное на 0,861, дает содержание общего белка в молоке в процентах.

