Продукты, образующиеся в процессе жизнедеятельности дрожжей
Они представляют собой отходы, от которых организм освобождается, выделяя их в среду. Некоторые продукты обмена веществ дрожжей представляют большой интерес для виноделия, так как они обусловливают букет и вкус вина.
Обычно продукты распада углеводов при брожении, за исключением этилового спирта и углекислого газа, называют вторичными. Продукты, образованные из белков, т. е. из аминокислот, называют побочными. Однако строго разграничить происхождение вторичных и побочных продуктов невозможно, поскольку одни и те же вещества, например высшие спирты, образуются как из углеводов, так и из аминокислот.
Ко вторичным продуктам брожения относятся глицерин, янтарная кислота, уксусный альдегид, уксусная, пировиноградная, молочная и лимонная кислоты, 2,3-бутиленгликоль, ацетоин, диацетил, эфиры, высшие спирты [124].
Механизм образования вторичных продуктов брожения еще не вполне ясен. Однако установлено, что первоначально возникают глицерин и уксусный альдегид, а все остальные указанные соединения, по-видимому, можно рассматривать как продукты превращения последнего.
Количественное соотношение вторичных продуктов может быть выражено уравнением Женевуа:

Коэффициенты перед буквами обозначают число молекул уксусного альдегида, затраченных на синтез одной молекулы данного вещества.
На обширном экспериментальном материале французские ученые показали, что образование вторичных продуктов брожения и их количественное соотношение зависят от фазы брожения и условий (температуры, аэрации, pH, состава среды, окислительно-восстановительного потенциала, типа используемых дрожжей – с превалирующим аэробным или анаэробным метаболизмом). Однако во всех случаях уравнение Л. Женевуа справедливо [265].
Глицерин образуется в процессе брожения, когда уксусный альдегид связывается с бисульфитом натрия (по второй форме брожения Нейберга), а также при брожении в щелочной среде. Образование глицерина значительно сильнее в начале брожения. Благодаря сладкому вкусу и маслянистости, он играет определенную роль во вкусовой гармонии вин. В обычных винах глицерин содержится в количествах от 7 до 14 г/л; в винах, приготовленных из винограда, поврежденного грибком Botrytis cinerea, – до 20 г/л. При хересовании вин содержание глицерина снижается на 7з от исходного количества [178]. Различия в содержании глицерина в винах зависят от технологии, температуры брожения, сульфитации и расы дрожжей [277, 278].
Ацетоин и диацетил влияют на качество вин, хотя количество их невелико – ацетоина от 2,0 до 84 мг/л, диацетила – от ОД до 1,8 мг/л. Присутствие их в винах является интересным по двум причинам: потенциальному влиянию на букет и аромат и роли в биохимических превращениях. Диацетил имеет определенный запах при низких концентрациях. Большие количества диацетила (более 1 мг/л) придают вину тон окисленности, иногда переходящий в мышиный. Сухие столовые вина и шампанское высокого качества содержат следы диацетила, низкого качества – выше 1 мг/л [160–163].
Образование диацетила и ацетоина при брожении находится в обратной зависимости от сульфитации [133]. Максимальное содержание ацетоина в несульфитированном сусле в 2 раза превышает максимум ацетоина, образующегося в сульфитированном сусле.
В процессе брожения, особенно при аэрации сусла, количество диацетила увеличивается, однако накопление его не аналогично образованию ацетоина. Максимальное количество (100 мг/л) ацетоина достигается в середине брожения сусла, а к концу он весь восстанавливается в 2,3-бутиленгликоль. Таким образом, все эти 3 вещества (диацетил, легко восстанавливающийся в ацетоин, а последний – в 2,3-бутиленгликоль) образуют в средах окислительно-восстановительную систему.
Количества диацетила, ацетоина и 2,3-бутиленгликоля, образуемых при брожении, находятся в зависимости и от исходной концентрации сахаров в сусле: чем выше концентрация сахаров (2, 5 и 10 г/100 мл), тем больше накапливается диацетила. Расы дрожжей, используемые при изготовлении вин, различаются по биосинтетической способности: одни, например раса Туркестанская 36/5, образуют диацетила 0,5 мг/л, ацетоина 9,7 мг/л, другие, например раса Кахури 7, – диацетила 9,6 мг/л, ацетоина 64,7 мг/л.
Из альдегидов в вине наиболее часто встречаются уксусный, пропионовый, масляный, валериановый, энантовый и др. В неразбавленном, виде альдегиды имеют острый запах. При разбавлении альдегидов, кроме уксусного, появляются приятные фруктовые тона [161]. Особенно много уксусного альдегида накапливается при брожении сульфитированного сусла. При этом образуется связанная сернистая кислота (альдегидсернистая кислота), количество которой при выдержке вина уменьшается вследствие распада ее и накопления в вине уксусного альдегида.
В присутствии кислорода воздуха винные дрожжи способны окислять этанол в уксусный альдегид [41, 178]. Небольшие количества уксусного альдегида (до 10 мг/л) образуются винными дрожжами при сбраживании глюкозы.
Хересные дрожжи способны активно окислять этанол в альдегид. На образование продуктов окисления расходуется не более 4% общего количества спирта [178].
Ацетали обнаружены в винах в незначительных количествах, кроме вин типа херес, где содержание альдегидов и ацеталей повышенное. Н. Ф. Саенко установила связь синтеза ацеталей с изменением ОВ-потенциала и отсутствие связи ацеталеобразования с жизнедеятельностью хересной пленки [178].
Кислоты. В составе летучих кислот обнаружены: уксусная, пропионовая, изомасляная, масляная, изовалериановая, валериановая, капроновая, каприловая. Следы энантовой кислоты выявлены только в аэробных условиях брожения. Содержание летучих кислот в виноматериалах, приготовленных в различных условиях брожения, показано в табл. 12. Летучие кислоты в основном накапливаются на начальных этапах брожения. Наибольший удельный вес к общему количеству образовавшихся кислот приходится на уксусную: в аэробных условиях брожения количество ее составило 82–90%, в анаэробных – 92–94% и. при избыточном давлении СО2–98%. Повышенный синтез капроновой и каприловой кислот наблюдался в анаэробных условиях брожения.
Уксусная кислота быстро образуется в начале брожения, а затем к концу брожения ее содержание может резко понижаться [154]. Некоторые дрожжи способны использовать уксусную кислоту. Так, Ж. Вантр еще в 1937 г. показал, что летучие кислоты, внесенные в сусло, частично исчезают в процессе брожения.
На этом свойстве дрожжей основана рекомендация посредством возобновления брожения снижать содержание летучих кислот в испорченном вине.
Н. Ф. СаеНко [173] предложен способ лечения больных вин хересными дрожжами, так как при этом не образуется много альдегидов и столовые вина не теряют своих особенностей.
Таблица 12
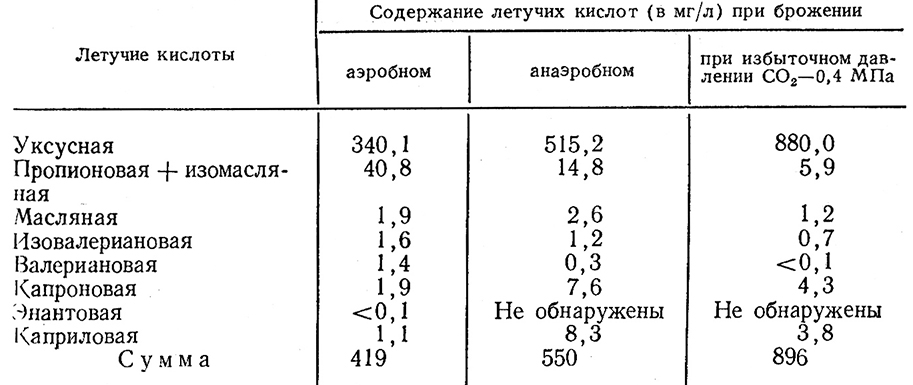
Янтарная кислота полностью отсутствует в винограде и обнаружена в вине как продукт спиртового брожения в количестве 0,1–0,4%.
Молочная кислота всегда образуется в процессе спиртового брожения – около 0,5% сбраживаемых сахаров расходуется на образование молочной кислоты. В здоровых белых винах количество молочной кислоты достигает 2,5 г/л, в красных – 4,5 г/л. Молочную кислоту, синтезированную дрожжами в процессе брожения, можно отличить от молочной кислоты яблочно-молочного брожения по оптической активности: D(–)-молочная кислота образуется дрожжами в анаэробных условиях, a L( + )-молочная – бактериями яблочно-молочного брожения из L-яблочной кислоты [244, 267]. Из остаточных гексоз и пентоз определенные виды молочнокислых бактерий могут синтезировать небольшие количества D-молочной кислоты.
Лимонная кислота появляется в случае нормального брожения в очень малом количестве – в пределах 0,3–0,8 г/л.
Яблочная кислота в сусле с высокой титруемой кислотностью присутствует в сравнительно большом количестве – 3,0– 4,5 г/л. В процессе брожения яблочную кислоту используют дрожжи, содержание ее уменьшается примерно на 25% [124, 161].
Повышенное количество яблочной кислоты в вине вызывает резкое вкусовое ощущение, определяемое как «зеленая кислотность».
Кетокислоты в вине представлены пировиноградной, щавелевоуксусной, а-кетоглутаровой и др.
Содержание пировиноградной кислоты колеблется в винах от 11 до 460 мг/л, α-кетоглутаровой – от 2 до 341 мг/л [124, 237].
При брожении в условиях избыточного давления СО2 содержание пировиноградной кислоты уменьшается, тогда как а кетоглутаровой – увеличивается [167].
Согласно данным С. Лафон-Лафуркад и Э. Пейно, образование пировиноградной и а-кетоглутаровой кислот зависит от рас дрожжей, различающихся по активности карбоксилазы: чем активнее пируваткарбоксилаза, тем меньше образуется пировиноградной кислоты.
Б. Ранкин [313] нашел, что некоторые расы дрожжей Sacch. cerevisiae и других видов, например Sacch. oviformis, Sacch. carlsbergensis, давали различные количества пировиноградной кислоты. Это имеет некоторое значение в практике виноделия, так как пировиноградная кислота связывает SO2 и таким образом снижает его антисептическую активность.
Эфиры при брожении образуются в заметных количествах и считаются важнейшей ароматической составляющей вин, среди которых этилацетат превалирует в количественном отношении. Этилацетат имеет простой фруктовый аромат. Этиловые эфиры масляной кислоты, а также эфиры высших спиртов обладают фруктово-цветочным запахом. Данные по образованию сложных эфиров дрожжами различных родов и видов свидетельствуют об их неодинаковых биосинтетических способностях. Так, Sacch. oviformis синтезируют гораздо больше этилацетата (в анаэробных условиях – 80 мг/л, в аэробных – 40 мг/л) и изоамилацетата (в анаэробных–1,21 мг/л и аэробных – 0,14 мг/л), чем Sacch. vini (в анаэробных условиях соответственно – 64 и 0,62 мг/л, в аэробных – 36 и 0,13 мг/л). Порог ощущения этилацетата в вине 180–200 мг/л. При более низких концентрациях влияет непосредственно на вкус вина, усиливая неблагоприятное впечатление жесткости и горечи [161].
В шампанских винах особое значение придается содержанию высококипящих эфиров – этилкапроната, этилкаприлата, этил-каприната, изоамилкапроната. Из липидов образуются этиловые эфиры линолевой, линоленовой и других кислот. Исследования [57] свидетельствуют о том, что 5-суточные дрожжи более богаты ароматообразующими веществами, чем 2-суточные, причем такое увеличение наблюдается в основном за счет этиллинолеата, обусловливающего подсолнечный тон шампанского (0,78 мг/кг – у 2-суточных и 5,8 мг/кг – у 5-суточных). Небольшое количество легколетучих сложных эфиров – этилацетата, этилизобутирата – также положительно влияет на букет шампанского.
По нашим данным, при брожении виноградного сусла наблюдается накопление эфиров как низкокипящих, так и высококипящих. Условия брожения влияют только на количественный состав эфиров. В анаэробных условиях уровень накопления эфиров увеличивается в 6 раз по сравнению с брожением в присутствии кислорода воздуха и в 4 раза по сравнению с брожением в условиях избыточного давления СО2 (табл. 13).
Таблица 13
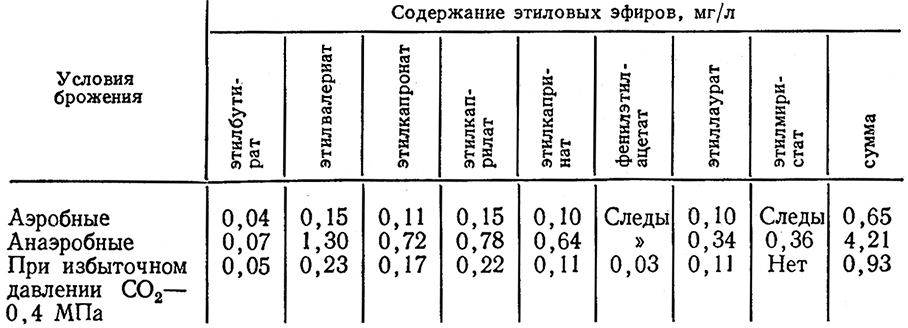
Выдержка виноматериалов, сброженных в аэробных и анаэробных условиях, на дрожжевом осадке привела к снижению процентного содержания высококипящих эфиров и увеличению низкокипящих и, наоборот, виноматериалы, полученные при брожении в условиях избыточного давления СО2, имели наиболее высокое процентное содержание высококипящих эфиров.
В вине содержатся значительные количества этиловых эфиров высших жирных кислот (энантовых эфиров), образуемых дрожжами в процессе брожения [8, 162]. Липиды наряду с другими компонентами вина участвуют в окислительных процессах при выдержке белых столовых вин, выполняя роль антиокислителей, а в определенной концентрации придают мягкость и гармоничность букету и вкусу вина [8, 162, 214]. Для анаэробного роста дрожжей рода Sacch. cerevisiae требуются олеиновая, линолевая и линоленовая кислоты. Эргостерин и некоторые другие стеролы также необходимы при анаэробном росте дрожжей. По-видимому, потребность в ненасыщенных жирных кислотах обусловлена тем, что синтез их в анаэробных условиях не происходит [232, 240, 307].
Липиды являются смесью истинных жиров (эфиры жирных кислот и глицерина), восков (эфиры жирных кислот и высших спиртов), фосфолипидов (содержащие жирную кислоту, глицерин, неорганический фосфат и амин или аминокислоту), стеринов. Клетки дрожжей Sacch. cerevisiae способны накапливать от 12,6 до 42,8% липидов по отношению к сухим веществам. Особенно они богаты стеринами, в основном эргостерином, содержание которого достигает 3% на сухую массу [6].
Синтез липидов у дрожжевых организмов тесно связан с продуктами углеводного обмена.
Липиды, содержащиеся в вине, могут иметь двоякое происхождение: из виноградной ягоды и из дрожжей. Семена винограда содержат масла, которые при брожении переходят в вино. В виноградное сусло попадает воск, находящийся на поверхности ягод винограда, основной составной частью которого является олеанолевая кислота и спирты [307].
Увеличение содержания липидов в вине по сравнению с суслом свидетельствует о том, что кроме липидов сусла в нем есть липиды, синтезируемые дрожжами. Так, по данным Н. А. Мехузлы и др. [111], в виноградном сусле количество общих липидов составляло 50 мг/л, в крепленом вине – 73 мг/л, в сухом вине – 113 мг/л.
Работы, выполненные нами совместно с Н. Я. Портновой, по изучению содержания липидов в вине и в дрожжах в зависимости от условий культивирования показали, что имеются количественные различия содержания их в процессе брожения и при выдержке виноматериала на дрожжевом осадке. Влияние условий брожения на содержание липидов в виноматериале и в дрожжах показано в табл. 14. В процессе выдержки вина на дрожжевом осадке содержание липидов в дрожжах несколько возрастает при аэробном брожении и снижается при анаэробном и под давлением СО2. При выдержке вина протекают 2 противоположно направленных процесса: синтез липидов в живых клетках за счет внутриклеточных сахаров [62] и извлечение липидов из мертвых клеток, содержание которых в дрожжах при брожении в анаэробных условиях и под давлением СО2 значительно выше, чем при брожении в аэробных условиях.
Таблица 14

При сравнительном изучении состава жирных кислот липидов дрожжей и вина установлено, что в процессе брожения дрожжи потребляют из виноградного сусла ненасыщенные жирные кислоты (олеиновую, линолевую, линоленовую), причем наиболее интенсивно в условиях брожения под давлением СО2. В условиях недостатка кислорода’ эти кислоты наиболее необходимы дрожжам для их жизнедеятельности [232]. Выдержка вина на дрожжевом осадке приводит к обогащению его преимущественно олеиновой и линолевой кислотами. Среди насыщенных жирных кислот как в сусле, так и в вине и дрожжах преобладают пальмитиновая и стеариновая.
Таким образом, изменяя условия брожения, можно влиять на липидный состав виноматериалов, а следовательно, и на вторичный процесс брожения, поскольку ненасыщенные жирные кислоты являются необходимым фактором роста дрожжей в анаэробных условиях.
Высшие спирты образуются путем дезаминирования или переаминирования аминокислот, последующего декарбоксилирования кетокислот и восстановления альдегидов в процессе спиртового брожения. Убедительно доказано, что высшие спирты могут образовываться и в результате превращений углеводов при брожении [157, 293, 323]. И. Я. Веселовым и И. М. Грачевой [36, 49] установлено, что высшие спирты при брожении возникают главным образом в фазе размножения дрожжей, т. е. процесс этот является результатом конструктивного обмена, связанного с ростом и размножением. Высшие спирты являются продуктами, синтез которых совершается на грани углеводного и азотистого обмена дрожжей.
При введении аммонийных солей в среду, обедненную по содержанию азота, снижается образование высших спиртов в 1,4–1,7 раза. Введение в эту среду избытка аминокислот а-аланина, а-аминомасляной кислоты, лейцина, изолейцина и валина способствует накоплению не только спирта, соответствующего строению аминокислоты, но и ряда других высших спиртов.
В вине найдены следующие спирты: метанол, н-пропанол, изопропанол, н-бутанол, изобутанол, н-пентанол (амиловый спирт), 2-метилбутанол (оптически активный амиловый спирт), 3-метилбутанол (изоамиловый спирт), н-гексанол, β-фенилэтиловый спирт, триптофол. Содержание их в вине в зависимости от условий брожения виноградного сусла показано в табл. 15.
Таблица 15

В условиях избытка кислорода воздуха сумма высших спиртов выше, чем в анаэробных и под давлением СО2.
По мере сбраживания сахаров биосинтез высших спиртов продолжается, однако он для отдельных спиртов идет неравномерно и зависит от условий брожения. Так, при брожении под давлением СО2 снижается содержание высших спиртов, особенно изобутилсвого и изоамилового; повышается процентное содержание β-фенилэтилового спирта. Это является положительным явлением, поскольку изобутиловый и изоамиловый спирты, особенно плохо влияющие на вкус, составляют 90% всех спиртов вина.
Приятным ароматом обладают спирты с циклическим строением, такие, как р-фенилэтиловый, тирозол, триптофол. Н. М. Сисакян, А. К. Родопуло, И. А. Егоров и Н. Г. Саришвили [145] добавляли в тиражированное шампанское фенилаланин, тирозин. Качество шампанского после выдержки в течение года улучшалось на 0,6–0,7 балла. Сочетание незначительных количеств высших спиртов, полученных из этих аминокислот, придавало вину характерные тона бутылочной выдержки.
Л. Уссеглио-Томассе [327], исследуя 25 образцов итальянских вин разных типов, полученных из различных сортов винограда разных лет урожая, показал, что при изменении содержания р-фенилаланина в сусле можно получить вино с различным содержанием фенилэтилового спирта. Образование фенилэтилового спирта во время брожения сусла находится в соответствии с образованием этилового спирта. Отдельные культуры дрожжей различаются по своей способности образовывать фенилэтиловый спирт. Установлено, что дрожжи продуцируют в среду фенилэтиловый спирт в зависимости от содержания фенилаланина, присутствующего в субстрате, но не более 20–25 мг/л.
Сульфгидрильные – SH-c оединения дрожжи могут выделять в среду в процессе брожения. В. Л. Кретовичем с соавторами показано, что наиболее активным продуцентом SH-соединений являются шампанские дрожжи; меньше их выделяют Sacch. carlsbergensis 776, наименее активно – пекарские дрожжи Sacch. cerevisiae 0–14. Результаты данной работы показывают, что выделение SH-соединений – физиологический процесс, связанный с обменом веществ клетки в процессе брожения и обусловленный особенностями данной расы дрожжей [89].
Выделение дрожжами сульфгидрильных соединений глютатиона и цйстеина, снижающих редокспотенциал (Eh),– важный показатель технологического процесса, поскольку развитие вина, начиная с выдержки и кончая созреванием и старением, связано в основном с течением окислительно-восстановительных реакций [161].
Изменение редокспотенциала в ходе брожения виноградного сусла зависит от скорости размножения дрожжей, накопления биомассы. Eh-потенциал начинает снижаться в момент размножения дрожжей, когда происходит максимальное потребление ими растворенного кислорода (табл. 16). При брожении сульфитированного сусла редокспотенциал уменьшается значительно интенсивнее [156].
Таблица 16
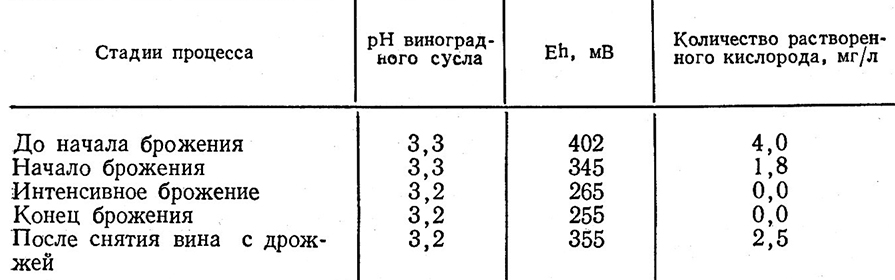
SH-соединения относятся к редуктонам – веществам с высокой восстанавливающей способностью. Редуктоны вина – это восстанавливающие вещества винограда и продукты биохимических реакций, протекающих в процессе приготовления вина. Присутствие редуктонов придает вину определенную способность защищать в первую очередь ароматические компоненты от окисления. Содержание редуктонов на различных этапах приготовления виноматериалов изучалось А. В. Трофимченко и сотр. [196]. Установлено наличие их в свежеотжатом сусле, при этом неодинаковое количество в различных сортах винограда. Существенные изменения в содержании редуктонов происходят в процессе брожения: количество их значительно повышается к моменту бурного брожения, а к концу брожения несколько снижается. Дробная сульфитация при брожении способствовала повышению количества редуктонов до 47 мг/л по сравнению с 33 мг/л при сульфитации сусла на отстаивании.
Наши определения показали более высокое содержание редуктонов в винах, сброженных под давлением СО2 0,4 МПа (50– 56 мг/л), чем в винах, приготовленных по общепринятой технологии (17 мг/л).
В виноматериалах, полученных путем сбраживания виноградного сусла под давлением СО2, запас сульфгидрильных соединений значительно выше. В них содержалось (в мг/л): восстановленного глютатиона 98 и SH-соединений 245, а в виноматериалах, приготовленных в обычных условиях брожения, соответственно 6 и 113.
Термотолерантные расы винных дрожжей способны в большей степени обогащать виноматериалы редуктонами. Eh виноматериалов, приготовленных на термотолерантных расах дрожжей Судак VI-5 (т), Феодосия 1-19 (т), Берегово 1 (т), был на 40–60 мВ ниже по сравнению с контрольными образцами.
Сероводород обладает неприятным запахом и его присутствие в вине в количествах, превышающих порог вкусовой чувствительности (0,005 мг/л), нежелательно [326]. Образование сероводорода при брожении виноградного сусла зависит от расы дрожжей, температуры брожения и состава среды. При испытании 10 различных рас дрожжей на способность накапливать H2S при сбраживании виноградного сусла обнаружена способность накапливать SО2 в количестве до 116 мг/л и H2S–до 10 мг/л. Обсуждаются данные по влиянию состава питательной среды на образование H2S дрожжами и наследственность этого признака [249, 331].
Дрожжи могут превращать элементарную серу и SO2 в H2S; цистеин, аспарагиновая, глютаминовая кислоты, глицерин, гистидин, орнитон, серин, треонин активируют образование H2S. Накопление H2S в винах задерживалось лишь присутствием метионина, пантотеновой кислоты или витамина В6 [244, 331]. Количество образуемого H2S для каждой расы было наследственным.
Разработан электролитический способ мгновенного удаления летучих соединений серы из пива путем пропускания его через камеру с двумя медными электродами [326].
Исследуя биологическое происхождение H2S в вине, Ружие [318] не обнаруживала его в винах, приготовленных путем быстрого брожения при высоких температурах. Снижение концентрации H2S наблюдалось и при применении смешанных культур дрожжей, способных и неспособных восстанавливать сульфаты.
Продукты, образующиеся в процессе автолиза дрожжей
Автолиз – это разложение компонентов клетки [65] под действием своих же гидролитических ферментов. При автолизе происходит распад белков, углеводов, нуклеотидов, липидов и других веществ клетки и выход их составных частей в среду. Необходимым условием автолиза является смерть клеток при сохранении активности внутриклеточных ферментов [159].
В виноделии длительное время поддерживалось мнение, что выдержка виноматериалов на дрожжах или добавление в вино-материал специально приготовленных автолизатов дрожжей значительно улучшает качество виноматериалов за счет увеличения азотистых веществ, в основном аминокислот. Однако позже исследованиями В. Н. Нилова и Г. Г. Валуйко [40] было установлено, что азотистые вещества дрожжей не улучшают качества виноматериалов, и только концентрат, полученный настаиванием вина на дрожжах при температуре +8°С, улучшает качество, придавая виноматериалам слаженный и мягкий вкус и тонкие тона бутылочной выдержки в букете. При дальнейшей расшифровке таких концентратов В. И. Ниловым и Е. Н. Датунашвили [40] было показано, что при температуре 0–10°С и pH в пределах 3, автолиз клеток дрожжей практически не идет, нет прироста азотистых веществ, а проявляется активность ферментов. Поэтому ферментные концентраты, получаемые в результате контакта небольшого количества виноматериала с большой массой дрожжей, отличаются активностью комплекса ферментов, снижающих ОВ-потенциал, и повышенным содержанием в них витаминов группы В, в особенности тиамина, пиридоксина и пантотеновой кислоты [41, 130].
Витамины группы В являются биологически активными соединениями и в ничтожных количествах могут оказывать существенное влияние на биохимические процессы, происходящие при созревании вина и формировании его букета. Поэтому положительное влияние ферментных концентратов на качество вина может быть связано с повышенным содержанием в них витаминов.
Ферментные концентраты, приготовленные на дрожжах разных рас, различаются по содержанию витаминов группы В. В ферментных концентратах дрожжей Sacch. vini пантотеновой (1000–1400 мкг/л) и никотиновой (20000–25000 мкг/л) кислот было в 2 раза больше, чем в концентратах дрожжей Sacch. oviformis (пантотеновой – 500–600 мкг/л, никотиновой 10000– 10200 мкг/л). Органолептическая оценка образцов вин, приготовленных с введением ферментных концентратов дрожжей различных рас, показала различие в аромате и букете готового вина. Наиболее существенное воздействие на качество вина оказывал ферментный концентрат дрожжей расы Феодосия 1-19 [41].
Введение в вино пантотената кальция дало такого же характера сдвиги в букете, что и ферментный концентрат. Внесение пантотената кальция в предварительно прокипяченное вино эффекта не дало, в связи с чем можно сделать вывод, что действие пантотената связано с его участием в биохимических процессах.
С продуктами автолиза дрожжей связан эффект созревания шампанского, обогащение вина биологически активными веществами, развитие тонкого букета и продолжительность игры [9, 161, 289]. С. П. Авакянц и Ф. И. Шакарова [5], изучая автолитические процессы у дрожжей при шампанизации, установили, что состав продуктов автолиза клеток зависит от температурного режима, продолжительности процесса и состава вина. Обработка дрожжей теплом (40°С) приводит к обогащению вина азотистыми и фосфорными веществами, участвующими в создании букета продукта. Для обогащения вина ферментами эффективной является обработка вина с дрожжами холодом (–5°С) в течение 2–5 сут.
Этими сведениями, естественно, не исчерпывается механизм действия продуктов автолиза дрожжей на вино. Не могут не привлечь внимания материалы, свидетельствующие о неодинаковой способности различных рас дрожжей синтезировать витамины, в том числе и витамин С [95]. Такая особенность дрожжей может быть важным показателем в селекции культур для производства, поскольку аскорбиновая кислота снижает редокспотенциал [38].
На основе изучения автолитических процессов в клетках дрожжей разработаны рациональные методы использования полезных свойств дрожжей в практике виноделия – применение ферментных концентратов для повышения качества вин [40, 124].

