Главной функцией молокосвертывающих энзимов является расщепление в æ-казеине связи Фен105-Мет106, в результате чего от æ-казеина отщепляется макропептид, мицеллы казеина теряют стабильность, и молоко свертывается. Это происходит во время выработки сыра в сырной ванне. Часть молокосвертывающих энзимов уходит с сывороткой, часть остается в сыре; оставшиеся в сыре энзимы расщепляют казенны по другим связям и тем самым принимают активное участие в созревании сыров. Исключение составляют сыры с высокими температурами II нагревания и с плавлением сырной массы, во время выработки которых молокосвертывающие энзимы большей частью или полностью разрушаются. Таким образом, молокосвертывающие энзимы кроме свертывания молока непосредственно участвуют в формировании органолептических показателей сыра.
Количество реннина, остающееся в сыре, увеличивается с увеличением его дозы, вносимой в молоко, и кислотности сыворотки. Грибные энзимы задерживаются в сырах в меньших количествах, чем реннин. Повышение температуры II нагревания снижает активность остающегося в сырах молокосвертывающего энзима. Уцелевший во время выработки реннин сохраняет активность в течение всего периода созревания сыра.
Высокая общая протеолитическая активность молокосвертывающих энзимов по сравнению с реннетом оказывает отрицательное влияние на качество сыров, особенно с длительными сроками созревания. Сыры, вырабатываемые с кристаллическим химозином, имеют менее выраженный вкус и медленнее созревают по сравнению с сырами, вырабатываемыми из этого же молока и по этой же технологии, но с сычужным порошком (реннетом). Следовательно, протеолиз, обусловливаемый общей протеолитической активностью молокосвертывающих энзимов, в определенной степени необходим или полезен в получении сыров высокого качества.
Химозин в растворе атакует α- и β-казеин, хотя они не имеют связи Фен - Мет. Характер расщепления химозином казеинов показан в разд. 2.4.2. В сырах химозин и пепсин атакуют медленно или почти не атакуют β казеин, что может быть связано с низкой активностью воды или иммобилизованным состоянием β-казеина.
Химозин и свиной пепсин в сыре образуют при расщеплении а51-казеина asrI пептид, но этот пептид далее расщепляет только химозин и энзимы молочнокислых бактерий.
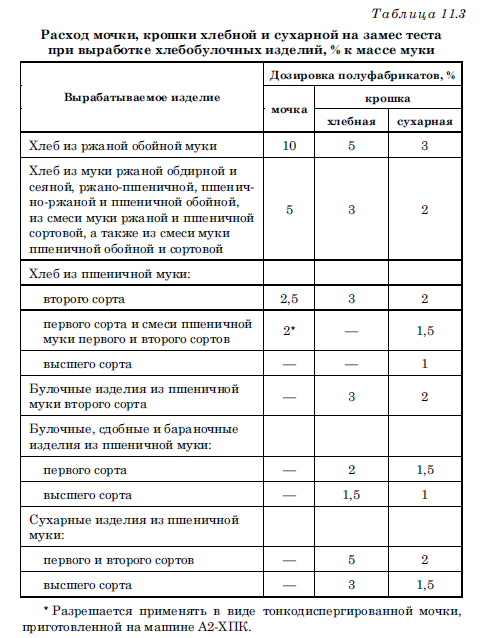
В сырах, вырабатываемых с химозином, последний ответственен за образование значительной части растворимого азота, пептидов большой молекулярной массы, но только небольшой части свободных аминокислот (табл. 11.3). При совместном действии реннина и закваски количество крупных и средних пептидов в сырах уменьшается, а количество мелких пептидов и аминокислот увеличивается, по сравнению с сырами, выработанными без закваски, что свидетельствует об активном расщеплении микрофлорой закваски пептидов, образуемых реннином. Ю. Свириденко и Г. Свириденко объясняют низкую активность молокосвертывающих энзимов при высвобождении свободных аминокислот из казеина стабилизацией пептидных связей связанными с казеином фосфатами.
В протеолизе участвуют не только химозин, но и другие молокосвертывающие энзимы. Пепсины и плесневые протеиназы обладают большей активностью по отношению к æ-, α- и β-казеинам. Продукты расщепления ими казеинов схожи, но не тождественны продуктам, образующимся под воздействием химозина. Исключением является энзим из End. parasitica, сильно отличающийся продуктами протеолиза от других молокосвертывающих энзимов. Чем сильнее молокосвертывающие энзимы отличаются от химозина, тем больше вероятность возникновения пороков.
Гидролиз α- и β-казеинов молокосвертывающими энзимами идет с гораздо более низкой скоростью, чем æ-казеина, но благодаря длительности созревания и участию протеолитических энзимов микрофлоры закваски к концу созревания as1-казеин и часть β-казеина бывают расщеплены. Пептиды, получающиеся в результате гидролиза казеинов молокосвертывающими энзимами, более доступны, чем исходный казеин, для протеолитических энзимов микрофлоры заквасок, которые играют главную роль в созревании твердых сыров.
Потери молочного жира с сывороткой выше, а плотность сгустка и качество сыра Чеддер ниже при использовании для свертывания молока пепсина вместо химозина. Исследования влияния сычужного фермента (СФ), энзима Мейто (М) и Реннилазы (Р) на химический состав сыра Чеддер показали, что самое высокое содержание влаги было в сырах, выработанных со смесью 1:1 М и Р, самое низкое - со смесью Р и СФ; М один или в смеси повышал содержание влаги и титруемую кислотность сыров; сыры с плесневыми протеиназами имели более высокое содержание летучих жирных кислот и быстрее созревали. Creamer et al. считают, что самые большие различия между сырами, вырабатываемыми с химозином и Реннилазой, касаются низкомолекулярных пептидов.
От вида молокосвертывающих энзимов зависит выход сыра, что обусловлено их различной протеолитической активностью. Так, были выработаны из одного и того же молока сыры со следующими комбинациями молокосвертывающих энзимов: 1 - сычужный порошок; 2 - рекомбинантный химозин (химозин, полученный методами генной инженерии); 3 - смесь 1:1 сычужного порошка и говяжьего пепсина; 4 - протеаза из Mucor miehei; 5 - протеаза из Мисог pusillus\ 6 - протеиназа из Endothia parasitica. Выход сыра был примерно равен в вариантах 1, 2 и 3, в остальных вариантах он был более низким. Выход Чеддера, выработанного на энзиме фирмы Хансена Ha-La (смесь химозина и пепсина, получаемая из телят), был на 0,39%, выше, чем выход сыра, выработанного с энзимом Мейто.
В промышленных препаратах молокосвертывающих энзимов имеются примеси липаз. При одинаковой молокосвертывающей активности скорость гидролиза оливкового масла при 37° С и pH 6,4 составила в нмоль · (мин-1 • мл'1) для сычужного порошка, говяжьего и свиного пепсинов, энзима Мейто примерно 2,2; для Реннилазы - 0,65; Фромазы - 0,88 и куриного пепсина - 2,78. Сопутствующие молокосвертывающим энзимам липазы были активны в широком диапазоне pH с оптимумом 5,5-7,0. Роль их в созревании сыров мало изучена.
В Италии для производства сыров вида Проволоне, острый вкус которых во многом обусловлен высоким содержанием масляной кислоты, готовят специальные сычужные пасты путем забоя телят, козлят или ягнят сразу после скармливания им молока, выдержке желудка со свернутым молоком в течение 60 дней и растиранием желудка с содержимым. Во время кормления эстеразы поджелудочной железы поступают одновременно с молоком в желудок. При выдержке в желудке наблюдается значительный рост микрофлоры. В зрелых желудках содержится смесь эстераз поджелудочной железы, желудочных протеиназ и липаз желудка, протеиназ и липаз микрофлоры. Получаемая паста обладает молокосвертывающей и липолитической активностью и позволяет вырабатывать сыры со специфическим вкусом; в сыре Проволоне после 370 сут созревания при использовании обычного реннета содержание масляной кислоты составило 0,71, при использовании сычужной пасты из козлят - 3,2 мг/г (Long & Harper, 1956).
Вид молокосвертывающих энзимов не оказал влияния на развитие микрофлоры закваски, лактобацилл и энтерококков в сыре Чеддер.
Степень участия молокосвертывающих энзимов в созревании сыров зависит от их количества, остающегося в сырной массе. Опыты с сыром Моцарелла с разным количеством реннета, остающимся в сыре (от 0,20 до 0,46 ед/г), показали, что прочность на разрыв сыра по мере его хранения при 10 °С снижалась, а содержание небелкового и водорастворимого азота повышалось пропорционально количеству оставшегося в сыре молокосвертывающего энзима.

