Полученные экстракты представляют собой маслянистую жидкость темного цвета, плохо растворимую в воде. Путем подбора была определена концентрация масла (1:10), в которой экстракты растворялись полностью.
Органолептические и физические свойства
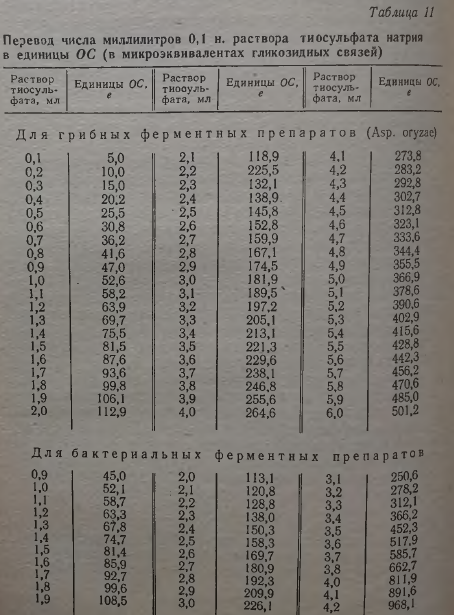
Полученные из различного сырья С02-экстракты коптильных препаратов обладали определенными органолептическими и физическими свойствами (табл. 11).
Пороговые концентрации определяли путем разбавления экстракта в порядке уменьшающейся концентрации. Подготовленные для определения пробирки должны содержать растворы с возрастающей концентрацией от нуля до концентраций, значительно превосходящих порог чувствительности. Наименьшие концентрации анализируемых веществ, в которых дегустатор в состоянии установить наличие запаха, фиксируются как индекс ощущения аромата (табл. 12).
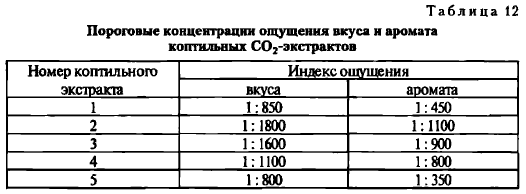
Наибольшие пороговые концентрации вкуса и аромата присущи экстракту, полученному из пиролизной древесины и шрота пряностей, т. е. он содержит наибольшее количество ароматообразующих компонентов.
Химический состав
Изучение химического состава экстрактов проводили методом газожидкостной хроматографии, основанной на способности различных веществ по-разному адсорбироваться на сорбентах. Для анализа использовали хроматограф «Сигма-1» фирмы «Перкин— Эльмерь со стеклянной капиллярной колонкой 25 м с жидкой фазой карбовакс 20 М, скорость газоносителя (гелий) — 40 см3/мин. Режим анализа: температура t = 70°С, продолжительность τ = 1 мин. После перепрограммирования: температура τ1 = 180°С, продолжительность T2 = 15 мин; t2 = 220°С, т2 = 10 мин. По времени удерживания классифицировали вещества, по площади пика определяли количество составных компонентов коптильных экстрактов. Результаты сравнительного анализа коптильных экстрактов представлены в табл. 13.

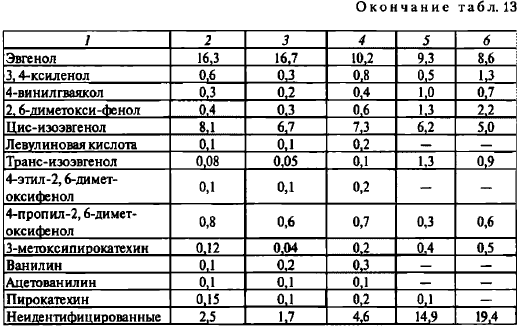
Из табл. 13 видно, что в коптильном С02-экстракте из отходов коптильного производства количество неидентифицированных продуктов колеблется от 14,9 до 19,4. Это, вероятно, связано с экстракцией жидким диоксидом углерода находящихся в отходах ацетилглицеринов, которые не идентифицировались использованным хроматографом. В эфирорастворимой фракции коптильных экстрактов 60—70 % составляют типичные для коптильных агентов фенолы: гваякол, метилгваякол, фенол, крезолы, эвгенол, изоэвгенол и др. Присутствуют также терпены, кислоты, карбонильные соединения.
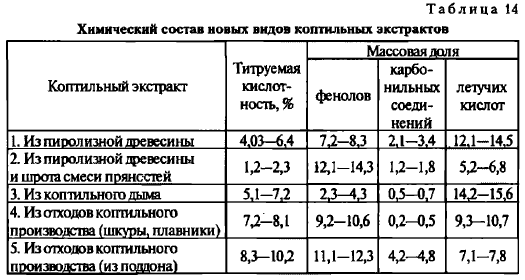
Химический состав коптильных экстрактов в количественных соотношениях представлен в табл. 14.
Наибольшее количество фенолов содержится в экстракте из смеси пиролизной древесины и шрота пряностей, что и определяет его аромат, поэтому для ароматизации консервов мы предлагаем этот экстракт.
Гидрофильно-липофильный баланс
С02-экстракты компонентов коптильного дыма, полученные нами по различным технологическим схемам, содержат фенольные вещества, которые способны тормозить окислительные процессы и подавлять жизнедеятельность микроорганизмов.
К фенольным веществам относят химические соединения, имеющие фенильный радикал (С6Н5-), к которому присоединены одна, две, три гидроксильные группировки (-ОН), кислотные (-СООН), аминные (-NH2), эфирные (-C-0-C-, -О-С=О), алкильные радикалы (-СН3, -С2Н5 и др.) и т. д.
Фенильный и другие радикалы молекул обладают неполярными свойствами и способны взаимодействовать с неполярными веществами. Функциональные группы (-СООН, -ОН, -NH2), содержащие в своем составе сильные электроотрицательные элементы (кислород, азот), способные смещать в свою сторону электронные облака, проявляют полярные свойства и взаимодействуют с полярными поверхностями. Таким образом, фенольйые соединения являются поверхностно-активными веществами, обладающими дифильными свойствами.
В растворах фенольные вещества могут диссоциировать, при этом могут образовываться анионы (R-COO-) или катионы (RNH3+), обладающие поверхностно-активными свойствами. Многие фенольные вещества не диссоциируют в водных растворах.
Фенольные вещества можно отнести к анионактивным, катионактивным и неионогенным поверхностно-активным веществам.
Важной характеристикой поверхностно-активных веществ, имеющей решающее значение для поверхностных и объемных свойств, является соотношение двух противоположных групп молекул — гидрофильной и гидрофобной (липофильной), так называемый гидрофильно-липофильный баланс (ГЛБ).
Для расчета ГЛБ использована теория Дэвиса, позволяющая с энергетических позиций количественно оценить и выразить в виде условных группировок чисел степень взаимодействия с водой отдельных групп, из которых состоит молекула поверхностно-активного вещества. ГЛБ рассчитывали по формуле:
![]()
Результаты произведенных нами расчетов представлены в табл. 15.

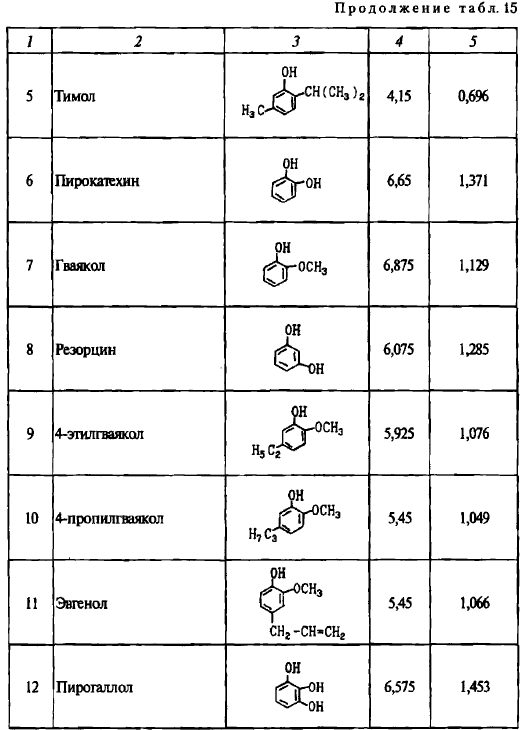
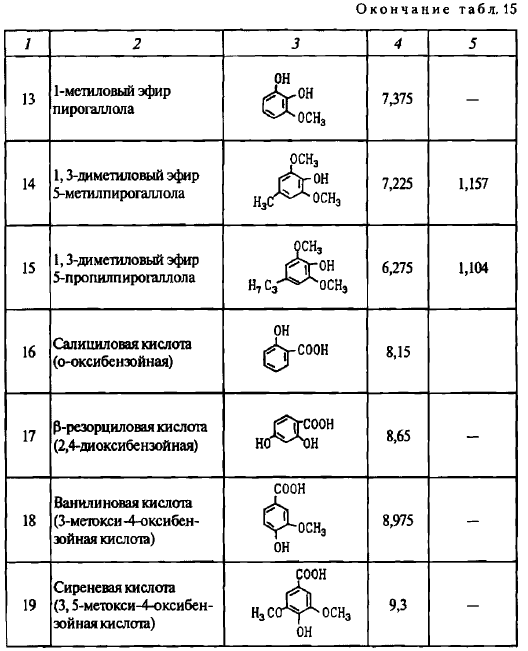
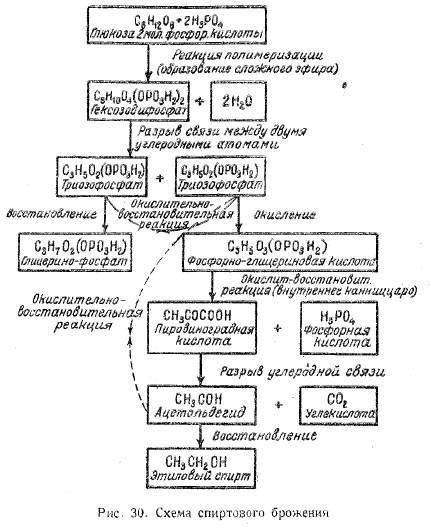
Подсчет ГЛБ фенольных веществ коптильных экстрактов показывает, что чем больше неполярных группировок в молекуле, тем ниже его значение (меньше 6). Такие молекулы можно отнести к эмульгаторам второго рода, стабилизирующим эмульсии типа «вода в масле» (рис. 30).
Попав в биологический объект с большим содержанием воды, фенольные вещества будут диспергировать воду, находящуюся рядом с жировыми частицами. Количество свободной воды, служащей переносчиком питательных веществ, уменьшится. Это может привести к гибели микроорганизмов, находящихся в пищевых продуктах.
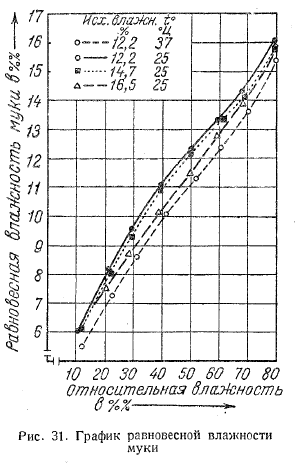
Наличие ионов калия и натрия в молекулах фенольных веществ увеличивает ГЛБ их на 17—19 единиц. Фенольные вещества начинают больше проявлять гидрофильные свойства, т. е. способность коллоидно растворяться, образуя почти прозрачные термодинамически равновесные растворы (рис. 31). Причем солюбилизирующая способность ПАВ возрастает с увеличением длины радикала.
Присутствие ионов натрия и калия в обрабатываемом коптильными экстрактами пищевом продукте переводит фенольные вещества из категории эмульгаторов второго рода в категорию эмульгаторов первого рода, стабилизирующих эмульсии типа «масло в воде» (рис. 32).
В данном случае диспергироваться будет «масло» (жир), находящееся в пищевом продукте. Появление эмульсии типа «масло в воде» придает любому продукту своеобразные вкусовые качества, а наличие в качестве стабилизатора такой эмульсии фенольного вещества придает продукту вкус копчености. При добавлении прянокоптильных экстрактов появляется аромат пряно-копченой продукции.
С другой стороны, такая стабилизация масла приведет к снижению количества кислорода, проникающего к поверхности масла, процессы окисления замедлятся. Кроме того, фенольные вещества являются прекрасными ловушками радикалов, появляющихся при окислительно-восстановительных реакциях. Наличие «ловушек» на поверхности масла также будет способствовать снижению скорости окисления жиров.
Токсичность коптильных экстрактов
Применение коптильных экстрактов является, в сущности, химическим методом обработки пищевых продуктов. Поэтому закономерен вопрос: не происходит ли при такой обработке накапливание химических веществ, наличие которых в пищевом продукте может оказаться нежелательным или даже вредным? Ранее сказано о положительной роли копчения как фактора, способствующего лучшей устойчивости продуктов при хранении и предупреждающего быструю окислительную и микробиальную порчу, что косвенно связано с пищевой ценностью продуктов.
Одной из групп коптильных компонентов, которую следует отнести к веществам, нежелательным в пищевых продуктах, являются многоядерные (полициклические) ароматические углеводороды, некоторые из них, например 3, 4-бензпирен, обладают канцерогенными свойствами.
Коптильные экстракты, способ изготовления которых предусматривает исключение полициклических углеводородов из их состава, не содержат 3,4-бензпирена. Отсутствие 3,4-бензпирена в коптильном экстракте, установленное таким тонким методом определения, как газохроматографический анализ, является практически достаточным условием для того, чтобы считать экстракты свободными от проканцерогенных веществ.
Антиокислительные свойства
В процессе технологической обработки продуктов питания кислород воздуха пагубно действует на его составные части: белки, липиды, углеводы и т. д.
Помимо обычного молекулярного кислорода, находящегося в триплетном состоянии (302), существует 6 его активных производных: атомарный кислород — О, озон — О3, синглетный кислород — 1О2, супероксидный радикал — 02*, гидроксильный радикал — НО* и пергидроксил — Н02*.
Наиболее высокой химической активностью отличается гидроксильный радикал НО*, который в течение 7 • 10-10 с вступает в реакцию с белками, нуклеиновыми кислотами, липидами, разрушая клеточные структуры и способствуя образованию продуктов свободнорадикального окисления — перекисей, альдегидов, кетонов.
Для защиты от образования свободных радикалов используют антиоксиданты.
К антиоксидантам относятся вещества различной химической природы: фенолы, полифенолы, пирокатехины, пирогаллол, рутин, кверцетин, витамины Е, С, Р, А, стероидные гормоны, фосфолипиды и серосодержащие соединения. В число антиоксидантов входят вода и двуокись углерода. Их относят к классу так называемых «тушителей».
Коптильный дым и конденсат дыма представляют собой очень сложную смесь различных классов органических соединений, причем даже в одной группе однотипных веществ может содержаться большое количество соединений, отличающихся не только молекулярными массами, но и химическими свойствами. Указанные особенности заставляют предпринимать необходимые предосторожности при хранении конденсатов дыма или их фракций, держа их до анализа при отрицательных температурах (-15...-20°С).
Возникновение антиоксидантных свойств коптильных компонентов связано с реакциями взаимодействия активных компонентов дыма с активными компонентами продукта.
При изучении окислительной порчи жиросодержащих продуктов наиболее важным является определение начала этого процесса.
Среди химических методов исследователи широко используют определение перекисного и кислотного чисел.
Перекиси образуются в жире раньше других продуктов окисления. Перекисное число характеризует стойкость жира против окисления, а в процессе хранения дает возможность улавливать начальный процесс окисления, не определяемый органолептической пробой.
Образцы рафинированного подсолнечного масла, использованного для обжаривания рыбы, массой 100 г каждый с добавками С02-экстрактов, выдерживали в течение 30 дней при комнатной температуре в открытых стеклянных стаканах. Площадь зеркала в каждом стакане составляла 12,5 см2. Все образцы в равной степени подвергались действию внешних факторов. Отбор масла для анализа проводили через каждые 10 дней. Исходное рафинированное подсолнечное масло имело перекисное число, равное 1,6 % 12. В табл. 16 представлены данные по изменению перекисного числа рафинированного подсолнечного масла при добавлении к нему 0,5 % С02-экстрактов.
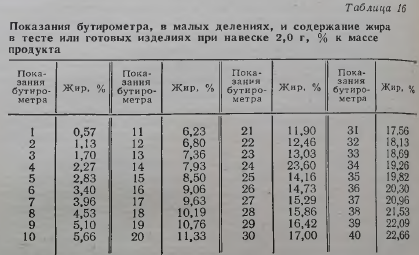
Таким образом, на основании проведенных экспериментов можно сделать вывод, что коптильный С02-экстракт и С02-экстракт почек гвоздики и перца черного содержат вещества, ингибирующие окисление растительных масел, используемых в производстве рыбных консервов при обжаривании рыбы. Ингибирующее действие этих добавок наблюдали и при хранении в течение 30 сут. Антиокислительная способность С02-экстрактов, полученных из кориандра, корицы, аирного корня и перца красного, по отношению к термоокисленному растительному маслу не обнаружена.
Установлена четкая связь между концентрацией перекисных соединений и интегральными кривыми хемилюминесценции света. Впервые вопрос о механизме свечения при окислении липидов в модельных системах подробно исследовался в большой серии работ Б. Н. Тарусова и А. Н. Журавлева.
В ходе самоокисления жирных кислот или жиров наблюдается свечение, которое связывают с образованием возбужденных альдегидов или кетонов, возникающих при рекомбинации перекисных радикалов:
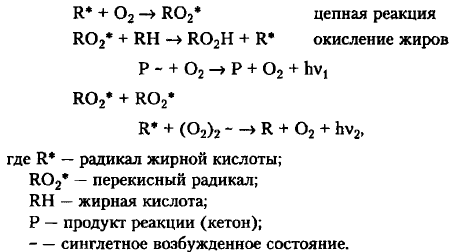
При добавлении одних антиоксидантов (адреналин, лецитин) наблюдается вспышка свечения. Добавление других антиоксидантов (β-ионола, α-нафтола) подавляет свечение, что объясняется связыванием перекисных радикалов. Очевидно, протекают реакции типа:

В КубГТУ и АГТУ изучено ингибирующее действие С02- экстрактов пряностей и коптильного С02-экстракта.
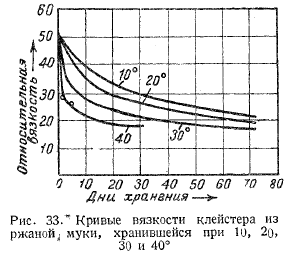
Устойчивость к окислению рафинированного масла, используемого для обжаривания рыбы, и антиокислительную эффективность добавок определяли с помощью установки для регистрации инстенсивности сверхслабого свечения ССС, сопровождающего окислительные процессы в липидах. Детектором установки являлся фотоэлектронный умножитель ФЭУ-39. Установка работала в режиме счетчика квантов. Образцы масла для исследования брали в виде 0,2 мл раствора масла в хлороформе. Кинетическую кривую ССС получали в результате суммирования импульсов фототока интегратором скорости счета и записи результатов на ленте автоматического самопишущего потенциометра ЭПП-09м. Об устойчивости растительных масел к окислению судили по кинетическим кривым термохемилюминесценции (ТХЛ), полученным методом измерения ССС при 85°С (рис. 33).
Графики показывают, что регенерированное после обжаривания в нем рыбы подсолнечное масло (кривая 2) в 5,5 раза менее стойко к окислению, чем исходное (кривая 1). Нерегенерированное подсолнечное масло после обжаривания в нем рыбы (кривая 3) устойчиво к окислению в 10 раз меньше свежего и в 2 раза — регенерированного. Несмотря на то, что по своим качественным показателям и составу регенерированное подсолнечное масло приближается к исходному, отсутствие в нем природных ингибиторов, по-видимому, снижает его устойчивость к окислению.
Установлено влияние добавок С02-экстрактов пряностей и коптильного С02-экстракта, полученного методом конденсации коптильного дыма в жидкой двуокиси углерода. Антиокислительную активность С02-экстрактов определяли по изменению величины вспышки свечения, наблюдаемой после введения их в количестве 5 % в нерегенерированное (рабочее) подсолнечное масло, в котором обжаривалась рыба (П. ч. = 0,4 % 12, К. ч. = 3,5 мг КОН на 1 г жира). Для сравнения ингибирующего действия те же С02-экстракты в количестве 3 % вводили в регенерированное подсолнечное масло. Результаты эксперимента представлены на графике (рис. 34).
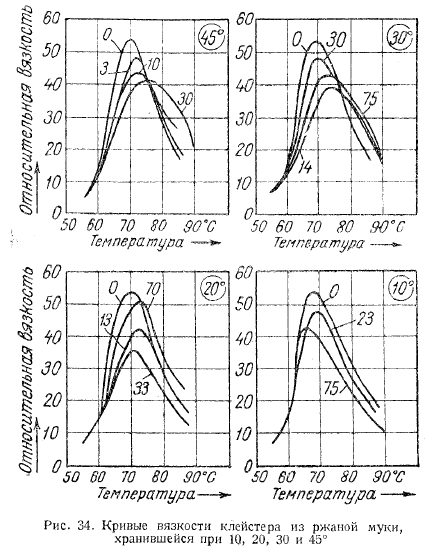
Согласно представленным графикам, тушение вспышки свечения наблюдалось при введении коптильного С02-экстракта и С02- экстракта гвоздики как в нерегенерированное (окисленное) подсолнечное масло (кривые 8, 6), так и в регенерированное (кривые 2, 3). Добавление С02-экстракта кориандра в обоих случаях оказалось менее эффективным (кривые 7, 4).
Определение эффективности действия ингибирующих окисление добавок проводили также кинетическим методом «активного кислорода», используя специальную установку для окисления масла. Воздух продували через слой масла (расход воздуха — 50 см3/мин) при температуре 140'С, периодически определяя пе- рекисное число (рис. 35). О стойкости к окислению судили по продолжительности индукционного периода, определяемого по достижении значения П. ч. - 0,5 % 12.
На графике (рис. 35) видно, что добавление 3 % С02-экстракта аирного корня и перца красного к регенерированному маслу (кривые 2, 3) практически не тормозило процессы окисления. Добавление 3 % С02-экстрактов корицы, гвоздики, перца черного и коптильного С02-экстракта (соответственно кривые 4, 5, 6, 7) к регенерированному подсолнечному маслу способствовало торможению окисления. При одном и том же значении П. ч. (0,5 % 12) индукционный период окисления регенерированного подсолнечного масла с С02-экстрактом перца черного (кривая 6) был в 1,6 раза продолжительнее, чем этот же показатель у регенерированного подсолнечного масла без добавки (кривая 1) и составлял 3,48 ч; у регенерированного подсолнечного масла с С02-экстрактами гвоздики и корицы был 3,34 и 3,18 ч соответственно. Индукционный период окисления регенерированного подсолнечного масла с коптильным С02-экстрактом составил 3,65 ч. Однако у подсолнечного масла, взятого в качестве контроля (кривая 8), этот период составил несколько больший отрезок времени — 4 ч и был больше в 1,77 раза, чем тот же показатель у регенерированного подсолнечного масла. Таким образом, регенерированное подсолнечное масло с добавкой С02-экстракта перца черного и коптильного С02- экстракта (кривая 7) по устойчивости к окислению приближается к свежему рафинированному маслу. Различие в эффективности антиокислителей обусловлено, вероятно, разным содержанием соединений фенольной природы в ингибирующих добавках (табл. 17).

Бактерицидность
Для первичной бактерицидной характеристики коптильных экстрактов приемлемы методы, используемые в работах с антибиотическими жидкостями. Обычно применяют метод дисков и метод последовательных разведений. В качестве тест-культур выбирают санитарно-показательные микроорганизмы и микроорганизмы, наиболее часто встречающиеся в рыбоовощной продукции. Диапазоны зон торможения представлены в табл. 18.
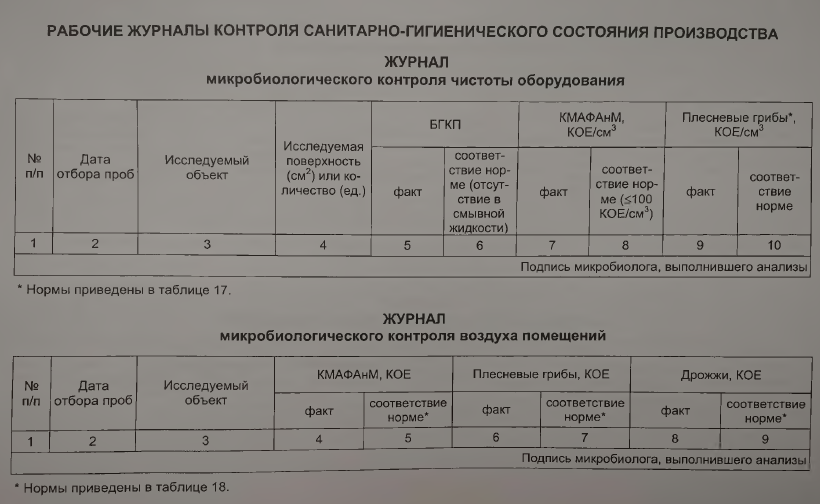
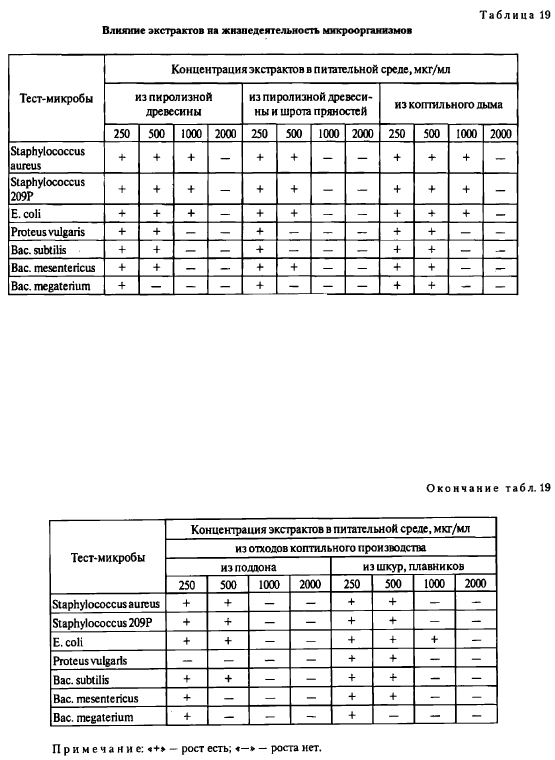
Влияние различных концентраций коптильных С02-экстрактов на жизнедеятельность микроорганизмов определяли методом последовательных разведений. Результаты анализов представлены в табл. 19.
Анализируя эти данные, можно сказать, что наиболее чувствительны к действию коптильных веществ протей и спорообразующие микроорганизмы. Весьма устойчивы, хотя и в различной степени, кишечная палочка, стафилококк. Вас. subtilis и Вас. megentericus оказались более устойчивыми к действию фенолов, чем Вас. mesentericus. Наиболее выраженными бактерицидными свойствами обладают коптильные экстракты, полученные экстрагированием пиролизной древесины и шрота смеси пряностей, так как они содержат наибольшее количество фенолов.
Существует ряд объяснений механизма бактерицидного действия фенольных соединений. Одни авторы считают, что фенолы понижают поверхностное натяжение на границе раствора бактерицида и бактериальной клетки, адсорбируются на поверхности клетки, вызывая изменение физического состояния коллоидов в ней, что и приводит к гибели микроорганизмов. Другие связывают бактерицидные свойства фенолов с их взаимодействием с бактериальными белками, воздействием на окислительно-восстановительную систему клеток, способностью к растворению клетки. А. Сатору пришел к заключению, что бактерицидный эффект выражается в подавлении жизнедеятельности клеток микроорганизмов химическими веществами и в проникновении их в клетку. Бактерициды, относящиеся к классу кислот, эфиров и соединений фенолов, воздействуют, проникая в плотную часть клетки, тогда как соединения, имеющие хиноидные группы, оказывают влияние на микроорганизмы в основном в зависимости от проницаемости клеток. Проникновение различных консервантов обусловливается адсорбционной способностью поверхности клеточной оболочки микроорганизмов, а эффект бактерицидности — химической природой бактериальных ингибиторов. Концентрации таких веществ, как фенолы, кислоты, сложные эфиры, достигают определенного равновесия, тогда как содержание других веществ постепенно уменьшается вследствие реакции с составными частями субстрата, в котором находятся микробы.
При увеличении алкильных боковых цепей в фенольном ядре увеличивается и бактерицидная сила. Отмечены и другие закономерности. Например, фенолы, содержащие разветвленные боковые цепи или две алкильные группы с одинаковым число атомов углерода, обычно менее бактерицидны по сравнению с фенолами, имеющими n-алкильные группы или одну из них.
Химизм антисептического действия кислот зависит, помимо природы микроорганизмов, проявляющих различную степень резистентности к кислотам, от способности к диссоциации, от природы аниона и сочетания этих факторов.
Карбонильные составляющие коптильного дыма, так же как и спирты, мало участвуют в бактерицидном действии копчения. Нейтральные соединения и органические основания обладают бактерицидным эффектом, а углеводы, наоборот, стимулируют рост микрофлоры.

