Для выбора наиболее эффективного стабилизатора необходимо иметь достаточно адекватные методы оценки действия их в пиве. Необходимо также установить такой аналитический показатель, который бы коррелировал с коллоидной стойкостью пива и позволял вскоре после розлива предсказывать, как долго данное пиво будет оставаться прозрачным, особенно- при хранении в условиях пониженной температуры.
Большинство методов основано на определении количества веществ — потенциальных образователей мути,, т. е. в основном полипептидов и полифенолов. Поскольку роль белков (полипептидов) в процессе образования мути была установлена раньше, чем роль полифенолов, определению количества именно этих компонентов посвящено наибольшее число методов.
Методы определения высокомолекулярных белков (полипептидов). Методы определения полипептидов в пиве весьма разнообразны. Ниже приводятся наиболее распространенные из них.
Определение коагулируемого белка [107]. В этом методе определяются высокомолекулярные полипептиды, свертывающиеся при нагревании. Количество коагулируемых азотистых веществ зависит от продолжительности и характера кипячения, поэтому должны строго соблюдаться определенные условия проведения анализа. Для кипячения можно использовать поваренную соль (40 г соли на 1 л воды), но соль неудобна тем, что она кристаллизуется на стенках бани. Лучше применять глицериновую баню, температура которой поддерживается на одном уровне (108° С), или проводить кипячение на плитке с асбестовой сеткой. '
По Де Клерку [107] в колбу Кьельдаля на 500—' 800 мл вносят 100 мл сусла или пива, освобожденного' от углекислоты, и кипятят 3 ч с обратным холодильником. Фильтруют содержимое колбы через фильтр диаметром 11 или 12,5 см и промывают колбу и фильтр четырехкратно (по 20 мл) горячей кипяченой водой. При этом свернувшиеся белки остаются на стенках колбы. Вносят в колбу фильтр с осадком и сжигают по Кьельдалю. Сжигают отдельно такой же фильтр и содержание азота в нем вычитают из значения его в главном опыте.
Однако не будет принципиальной ошибкой, если сжигать не осадок, а фильтрат после отделения скоагулированного белка, учтя разведение за счет промывания фильтра. В этом случае можно брать 50 мл сусла и пива, а объем фильтрата довести до 100 мл.
Определение коагулируемого азота часто дает полезную информацию о предполагаемой стойкости пива. Считают, что с уверенностью говорить о хорошей стойкости пива можно только в том случае, если количество коагулируемого азота в нем не более 0,5 мг/100 мл.
Определение предела осаждения сульфатом аммония [33, 107]. Методика проведения этого несложного определения хорошо известна. По Гартонгу анализ выполняется следующим образом. Берут ряд пробирок с 10 мл пива, в которые добавляют насыщенный раствор сульфата аммония в повышающихся количествах: 0,5; 0,6; 0,7 мл и т. д., перемешивают и через 15 мин рассматривают в проходящем свете. Объем сульфата аммония, который требуется для того, чтобы вызвать в пиве опалесценцию, характеризует предел осаждения. Результаты выражают в мл на 10 мл пива (иногда, в частности в СССР, предел осаждения выражают в мл на 100 мл пива). Обычно значения предела осаждения лежат между 0,5 и 2,5 мл/10 мл. Стойкое пиво дает значения 1,5 мл и более на 10 мл.
Необходимо отметить, что визуальное установление появления мути может быть источником ошибок. Нарцисс и Рёттгер [165] показали, что только самое первое легкое помутнение обусловливают вещества с молекулярной массой>60 ООО, если же добавлять сульфат аммония до несколько более сильного помутнения, то в этом случае осаждаются уже вещества меньшей молекулярной массы. Необходимо учитывать также, что вещества полисахаридной природы, имеющие достаточно высокую молекулярную массу, также выпадают в осадок при добавлении к пиву сульфата аммония.
Вариант более объективного, инструментального определения помутнения, возникающего от добавления сульфата аммония, предложен Симмондсом [218] и заключается в следующем. 200 мл пива, отмеренные цилиндром, вносят в бутылку из бесцветного стекла вместимостью 300 мл и добавляют к нему 50 мл (при 27° С) насыщенного раствора сульфата аммония. Бутылку плотно закрывают, тщательно встряхивают и помещают в водяную баню температурой 30° С. Через 30 мин измеряют мутность в чувствительном нефелометре (например, в мутномере фирмы «Радиометр»).
Однако и для этого варианта метода остаются в силе соображения о возможности возникновения помутнения, вызванного веществами полисахаридной природы.
Басаржова и др. [85] разработали объективные методы определения веществ, высаливающихся насыщенным раствором сульфата аммония, с помощью различного типа нефелометров. Предварительно по формазиновым суспензиям известной мутности (от 0,5 до 12 ед. ЕВС) строят калибровочные кривые. Один из вариантов метода заключается в следующем. В ряд пробирок вносят по 10 мл пива, освобожденного от СО2, и добавляют туда же в повышающихся количествах насыщенный раствор сульфата аммония. В контроле к ряду пробирок с 10 мл пива добавляют такое же количество воды. Измеряют мутность на ФЭКН при длине волны 570 нм. Измерение проводят через 15 мин после добавления сульфата аммония, причем в кювету раствор переносят за 2 мин до истечения 15 мин для того, чтобы раствор в кювете устоялся. Измерение делают против контроля.
Насыщенный раствор сульфата аммония готовят так, чтобы при температуре 20° С в 100 г раствора находилось 43 г безводного сульфата аммония, а после отстаивания раствора в течение 48 ч на дне колбы оставались нерастворившиеся кристаллики сульфата аммония. Если при приготовлении раствор оказывается мутным, его надо после 3—4 дней отстаивания тщательно профильтровать.
Авторы указывают следующее соотношение между результатами анализа и стойкостью пива:
пиво нестабилизированное показывало мутность 2 ед. ЕВС при добавлении 0,5—1,25 мл раствора сульфата аммония;
пиво, стабилизированное низкими дозами стабилизирующих средств и имевшее стойкость 3—4 мес, давало мутность 2 ед. ЕВС при добавлении 2,75 мл раствора сульфата аммония;
пиво со стойкостью до 6 мес. показывало мутность 2 ед. ЕВС при добавлении 3 мл раствора сульфата аммония;
пиво со стойкостью до 8 мес, сильно стабилизированное, давало мутность 2 ед. ЕВС при добавлении 3,5 мл раствора.
Однако далеко не всегда удается установить такую тесную корреляцию между показателями «сульфатного теста» и стойкостью пива.
Осаждение полипептидов пива пикриновой кислотой (реакция Эсбаха). Реактив Эсбаха готовится следующим образом: 12,5 г пикриновой кислоты растворяют в кипящей дистиллированной воде, добавляют 25 мл ледяной уксусной кислоты и объем доводят до 100 мл. Отмечают количество реактива (в миллилитрах), достаточное для возникновения помутнения в пиве. Расчет ведется в миллилитрах реактива на 10 мл пива. Этот реактив осаждает не только высокомолекулярные белки, но и среднемолекулярные полипептиды (молекулярная масса 4600).
Фракционирование азотистых веществ сусла и пива по Лундину и Шрёдерхай- му [107]. Этот метод позволяет разделить азотистые вещества сусла и пива на 3 фракции: фракция А — высокомолекулярные полипептиды, осаждаемые определенным количеством танина; фракция В — полипептиды средней молекулярной массы, осаждаемые фосфомолибденовой кислотой; фракция С — низкомолекулярные азотистые вещества (аминокислоты и пептиды), остающиеся в фильтрате после удаления осадка, образованного фосфомолибденовой кислотой. На коллоидную стойкость влияют вещества фракции А, более стойкое пиво содержит небольшое количество этих веществ.
Фракционирование по Лундину требует большой затраты времени и труда.
Определение высокомолекулярных белков с помощью краски Амидошварц 10 В. Клоппер [142] разработал метод определения высокомолекулярных белков (полипептидов) в сусле и пиве по связыванию ими краски Амидошварц 10В. Метод основан на том принципе, что высокомолекулярные азотсодержащие вещества образуют с красителегл нерастворимые соединения. Величина снижения оптической плотности раствора Амидошварца пропорциональна количеству высокомолекулярных полипептидов.
Определение проводится следующим образом. 5 мл сусла или пива вносят в центрифужную пробирку, добавляют 20 мл раствора красителя (примерно 440 мг/л, точная дозировка устанавливается по экстинкции раствора, содержащего 10 мг/л, которая должна быть 0,568 при 590 нм в кювете 10 мм). После перемешивания оставляют на 30 с, затем центрифугируют 10 мин при 3000 об/мин. 5 мл надосадочной жидкости переносят в 50 мл мерную колбу, доводят до метки и перемешивают. В контроле 5 мл воды смешивают с 20 мл раствора Амидошварца и разводят в соотношении 1 : 10. При длине волны 590 нм в кювете 10 мм определяют оптическую плотность контроля и сравнивают с опытным раствором. Была найдена хорошая корреляция (7=0,815) полученных значений с фракцией А по Лундину.
Все методы определения высокомолекулярных полипептидов пива могут использоваться для оценки действия того или иного стабилизатора, но они не дают «сколько-нибудь значительной корреляций с фактической коллоидной стойкостью пива.
Очень показательны в этом отношении результаты, полученные Греем и др. [71] еще в 1953 г. (табл. 73).
Таблица 73
Результаты анализов на содержание в пиве высокомолекулярных полипептидов и стойкость пива

* Мутность измерялась после 10 нед хранения при 30° С и суточного выдерживания при 0° С.
Данные табл. 73 показывают, что в пиве, .обработанном бентонитом, значительно снижено содержание веществ, осаждаемых сульфатом аммония и пикриновой кислотой, однако заметное улучшение стойкости получено только с очень большой дозой этого стабилизатора. Наоборот, в пиве, обработанном ферментным препаратом, количество этих веществ уменьшено незначительно, однако стойкость пива очень высокая. Авторы работы считают, что полученные результаты указывают на селективность и специфичность действия ферментов.
В настоящее время установлено, что появление коллоидного помутнения обусловлено не всей совокупностью высокомолекулярных полипептидов пива, а только какой-то частью их. Полагают, что это те полипептиды, которые имеют наибольшее сродство с полифенолами.
Определение белков, чувствительных к танину. Начало такого рода исследованиям было положено Финком и Вилднером [114]. Первая часть их работы касалась осаждения белков сусла и пива танином: как ведут себя различные белки сусла и пива при добавлении танина, осаждаются ли более или менее равномерно все группы белковых веществ или есть какие-то группы, вступающие в реакцию с танином в большей степени. К пробам сусла или пива добавляли раствор танина различной концентрации и оставляли на определенное время. Образующийся осадок или муть отфильтровывали и определяли азот в осадке и все формы азота в фильтрате. Исходили из концентрации танина, которая применяется на практике для стабилизации пива, — 10 г/гл.
В табл. 74 приведены данные по количеству осаждаемых различными концентрациями танина азотистых веществ сусла и пива. Отношение сусла или пива к раствору танина было 9:1.
Таблица 74
Осаждение различных азотистых веществ сусла танином
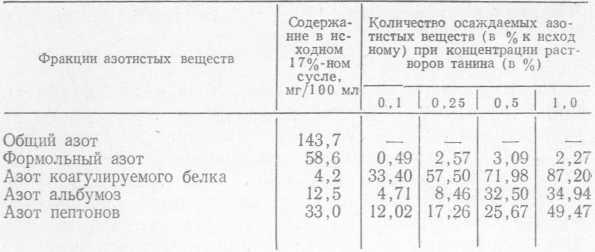
С повышением концентрации раствора танина количество осаждаемых азотистых веществ во всех фракциях увеличивается. Наибольшее участие в образовании осадка с танином в сладком сусле принимает фракция коагулируемого белка, которая уменьшается на 87% при обработке 1%-ным раствором танина, затем пептоны и альбумозы. В пиве, как показывают данные табл. 75, соотношение было иное.
Осаждение танином различных азотистых веществ пива
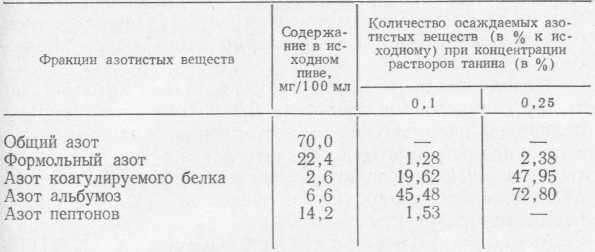
В пиве в реакцию с танином вступает преимущественно фракция альбумоз, которая уменьшается на 73% при обработке 0,25%-ным раствором танина, затем коагулируемый белок, уменьшающийся при такой обработке почти наполовину.
В результате исследований авторы предложили новый аналитический метод более глубокой характеристики белков пива — определение количества белка, осаждаемого танином. Под термином «таниновое число», предложенным этими авторами, понимается процент общего азота, осаждаемого 0,1%-ным (таниновое число I) или 0,2%-ным (таниновое число II) растворами танина в определенных условиях. Авторы считают, что таниновое число характеризует содержание в пиве белковых веществ, влияющих на его стойкость, и может быть одним из показателей пригодности пива для пастеризации. Исследовали влияние разных факторов на характер образующегося осадка.
Окончательная пропись метода была следующей. К 180 мл освобожденного от СО2 пива добавляют 20 мл 0,2%-ного раствора танина и ставят при температуре 10—12° С.
Через 1 ч фильтруют через двойной складчатый фильтр до прозрачности (обычно достаточно 2 раза). По 50 мл фильтрата сжигают по Кьельдалю.
Шапон предложил метод оценки количества белка, чувствительного к танину, путем добавления к пиву 0,1% галлотанина и нефелометрирования образующегося помутнения [159].
Посада и др. [190] разработали такой метод: в бутылку с пивом вместимостью 0,2 л добавляют определенное количество свежеприготовленного раствора гал- лотаниновой кислоты из расчета 5 г на 1 л пива и бутылку 1,5 ч встряхивают. Разница в нефелометрических показаниях до обработки и после нее характеризует галлотаниновую муть.
Метод Томпсона и Форварда [233]. К 180 мл пива, находящегося в кювете с длиной грани 55 мм при 20° С, добавляют при постоянном перемешивании свежеприготовленный раствор галлотаниновой кислоты концентрацией 100 мг/л. Скорость добавления 4,5 мл/ч. Когда концентрация галлотаниновой кислоты достигнет 5 мг/л, измеряют мутность в нефелометре Хелма. Из полученных результатов вычитают начальную мутность и получают значение галлотаниновой мути пива. Расчеты показывают, что на 180 мл пива надо добавить 0,4 мг галлотаниновой кислоты, т. е. 9 мл раствора в течение 2 ч.
Авторы считают, что этот метод может быть полезен в установлении небольших различий во фракции полипептидов, чувствительных к танину, которые трудно определить какими-либо другими методами.
Метод ВНИИПБПа. Во ВНИИПБПе разработан простой и быстрый метод определения количества высокомолекулярных полипептидов, способных реагировать с танином [62]. При разработке метода исходили из соотношений ингредиентов, принятых в методе Лундина при определении фракции А.
В мерную колбу на 50 мл вносят 2,5 мл пива, освобожденного от углекислоты, добавляют примерно 25— 30 мл дистиллированной воды, затем 5 мл 10%-ного раствора H2SO4 и 5 мл 1,6%-ного раствора танина. Доводят объем до метки дистиллированной водой и переливают содержимое в колбу вместимостью 250—300 мл. Через час, тщательно перемешав суспензию танино-по- липептидного осадка, ее нефелометрируют на ФЭКН. При проведении анализа необходимо следить за тем, чтобы температура растворов и посуды была около 20° С (±2). С помощью этого метода была прослежена динамика изменения количества высокомолекулярных полипептидов пива под влиянием различных ферментных препаратов и изучено действие разных стабилизирующих средств.
В настоящее время результаты, получаемые по этому методу, могут быть выражены прямо в величине фракции А по Лундину. Формула пересчета, рассчитанная Калашниковой с помощью ЭВМ по 192 определениям, имеет вид:
у = — 0,0450,0276х,
где (/ — таниновый показатель, опт. плотн.;
х — фракция А, мг/100 мл.
Методы определения содержания в пиве полифенолов. До настоящего времени нет достаточно адекватного метода определения в сусле и пиве полифенолов, участвующих в образовании коллоидного помутнения. Это связано с тем, что при определении, например, только антоцианогенов остаются неохваченными многие вещества, также участвующие в помутнении. При определении же всей совокупности полифенолов получают малозначимую информацию, поскольку многие полифенолы не имеют отношения к помутнению.
Ниже приведены некоторые из методов определения полифенолов, наиболее широко используемых зарубеж- ними исследователями и наиболее приемлемых для практического осуществления.
Метод Овэйдеса, Рубина и Бреннера [176]. Этот метод основан на экстракции дубильных веществ этилацетатом и измерении светопоглощения на спектрофотометре. Предварительно строятся калибровочные кривые для дубильных веществ хмеля и солода.
Дубильные вещества солода получают следующим образом. Приготовляют конгрессное сусло, 300 мл его упаривают примерно до 100 мл и 1 н. раствором НС1 устанавливают pH 2,0. Проводится трехкратная экстракция дубильных веществ 100 мл этилацетата. Из этилацетатного раствора вода удаляется безводным сульфатом натрия. Этилацетат выпаривают на водяной бане и сухой остаток переводят в метанол, объем которого доводят до 50 мл. В части раствора гравиметрически определяют содержание дубильных веществ. С различными разведениями этого раствора строят калибровочную кривую. Максимум экстинкции лежит между 265—275 нм.
Определение дубильных веществ в пиве проводят в следующем порядке. В 50 мл градуированный цилиндр вносят 5 мл пива, освобожденного от СО2, и 5 мл н. НС1. Объем доводят до 25 мл, затем добавляют изооктан до 50 мл. Смесь сильно встряхивают 30 с, затем переносят в делительную воронку и оставляют до хорошего разделения фаз. Водный раствор отделяется (примерно 22—23 мл), а изооктановый слой выбрасывается. Из водного раствора 10 мл вносят в делительную воронку и экстрагируют 50 мл этилацетата в течение 10 с. После хорошего разделения фаз водную фазу сливают и выбрасывают. К этилацетатному экстракту добавляют безводный сульфат натрия для удаления следов влаги. Раствор декантируют в 100 мл колбу. Этилацетат полностью удаляют на водяной бане. Колба остается еще на 30 мин на водяной бане для полного удаления следов этилацетата. Остаток растворяют метанолом, причем производят 3 последовательные экстракции примерно по 3 мл метанола, метаноловые экстракты переносят в мерную колбу на 10 мл, в которой уже содержится 0.5 мл н. НС1. Доводят объем метанолом до 10 мл. Экстинкция этого раствора измеряется против контроля — 0,5 мл н. НС1 + 9,5 мл метанола.
Пфеффер [181], проверяя этот метод, нашел, что этилацетат экстрагирует и другие вещества, кроме дубильных, что завышает результаты гравиметрического определения при построении калибровочной кривой. Он установил наличие в этилацетатных экстрактах белка (до 14% в экстрактах из пива), что объясняется экстракцией белково-полифенольных комплексов. Максимумы поглощения дубильных веществ пива лежат около 263—280 нм, причем они выражены слабее, чем у раствора танина и катехина (у танина — при 276 нм, у катехина— при 278 нм).
Согава [219] считает этот метод достаточно простым, чувствительным и воспроизводимым. Он полагает, что, поскольку этилацетат сам по себе имеет большую адсорбцию при 270 нм, лучше проводить определение при 283 нм, так как при этой длине волны этилацетат совершенно прозрачен. Была рассчитана удельная адсорбция танина е[^=69,9 и полифенолов пива = 21,7. Пользуясь этими данными, рассчитывали содержание полифенолов по кривой, построенной по растворам танина.
Метод Стоуна и Грэя [по 181]. Этот метод является модификацией метода Де Клерка и др. [107], которым еще и сейчас пользуются в некоторых исследовательских и производственных лабораториях. Метод основан на колориметрическом определении интенсивности красного окрашивания, которое дают полифенолы с солями трехвалентного железа в щелочной среде. Определение велось в визуальном компараторе и количество полифенолов определялось по стандартному раствору танина.
К пробам сусла или пива добавляют раствор гуммиарабика для предотвращения образования мути. Так как оптимум окраски лежит при pH 9, pH пробы пива устанавливается на эту величину разведенным аммиаком. Расчет ведется по растворам танина известной концентрации.
В 25 мл мерную колбу вносят 10 мл раствора гуммиарабика (12,5 г гуммиарабика центрифугируют в 90 мл Н2О), 10 мл испытуемой пробы и встряхивают. Добавляют 0,5 мл реактива, содержащего 2,5 г лимоннокислого железо-аммония в 100 мл воды и 0,01%-ный раствор фенилртутного ацетата, и перемешивают. Добавляют 5 мл разведенного NH3 (1:2) и встряхивают. Отмечают время, доводят водой до 25 мл и точно через 5 мин фотометрируют.
Пфеффер проводил определение на спектрофотометре при 530 нм. Всего на каждое определение делается 4 измерения: А — проба с железным реагентом; В —проба без железного реагента; С—вода с железным реагентом; D — вода без железного реагента. Содержание дубильных веществ (в мг) находят по формуле: (А—В) — (C — D)F. Коэффициент F берется по кривой, построенной по растворам танина.
Пфеффер отмечает, что если при определении дубильных веществ пользоваться коэффициентом, полученным по кривой для танина, то получаются заниженные результаты. Это объясняется тем, что различные дубильные вещества дают различную окраску, причем танин дает с железом значительно более интенсивную окраску, чем дубильные вещества хмеля и особенно пива. Антоцианогены дают примерно такую же по интенсивности окраску, как и танин, катехин — значительно слабее. Если на растворе танина А = 0,294, то на растворе катехина F=0,893.
Метод Гарриса и Рикеттса [128]. Определяемые по этому методу антоцианогены включают все вещества, которые при нагревании с кислотой образуют красные пигменты — антоцианидины. Антоцианогены полностью адсорбируются на нейлоне, и адсорбат растворяется в смеси бутанол—НС1 и нагревается. Антоцианогены переводятся в окрашенные антоцианидины. По интенсивности возникающей окраски определяют содержание антоцианогенов.
Определение проводят в следующем порядке. 10 мл пива без СО2 встряхивают 40 мин с 0,5 г нейлона. Встряхивание не должно продолжаться дольше, так как интенсивность образования окраски снижается. Нейлон отфильтровывают, отмывают водой от пива и растворяют в 15 мл смеси «-бутанол — НС1 (5:1). Реакционная смесь нагревается до 105° С, причем каждые 3 мин встряхивается до тех пор, пока не образуется прозрачный раствор красного цвета. После этого температура выдерживается еще 30 мин. После охлаждения прозрачный пурпурно-красный раствор доводится смесью бутанол — НС1 до 25 мл, интенсивность окраски измеряется на спектрофотометре при 550 нм. Из-. полученного значения вычитается значение, полученное в контрольном опыте, в котором вместо пива берется вода:. Если экстинкция выше 0,550, пиво надо развести. При адсорбции на нейлоне наблюдаются потери, которые- могут быть объяснены полимеризацией и образованием хинонов. Калибровочная кривая строится по определенным количествам лейкоцианидина, добавляемого к пиву.. Калибровочная линия не прямая.
Интенсивность образующейся окраски зависит от- наличия катализаторов (железо, медь) и от образования коричневого пигмента при нагревании с HCI, поэтому концентрация НС1 должна быть по возможности низкой. Влияние железа исключается добавлением к раствору бутанол — НС1 определенного количества железа (10 мг/л).
Метод Штайнера и Штокера [225] (в модификации Пфеффера). Этот метод также основывается: на превращении антоцианогенов в антоцианидины посредством обработки минеральной кислотой. Но в этом методе не производится адсорбция антоцианогенов, антоцианогены определяются прямо в пиве. Пиво содержит довольно много веществ, которые при обработке смесью бутанол — НС1 образуют коричневые пигменты. Поскольку было установлено участие этих веществ в холодном помутнении, определение их является положительным моментом.
Смесь 5 мл пива, 2 мл концентрированной НС1, содержащей 0,001% железа, 10 мл бутанола, нагревают 30 мин на кипящей водяной бане и после охлаждения доводят бутанолом объем ее до 25 мл. Измерение производится при 550 нм. Метод может быть применен: только для светлого пива.
Метод Макфарлана [155]. В этом методе вместо нейлона в качестве адсорбента применяется порошок PVP (Поликлар АТ). Адсорбированные вещества растворяются в растворе п-метил-2-пирролидона и НС1, содержащем сульфат железа, и посредством нагревания переводятся в антоцианидины.
154 мг FeSO4-7H2O растворяют в 100 мл концентрированной НС1. К Ю мл этого раствора добавляют 70 мл концентрированной НС1 и водой доводят до 100 мл. Две части свежеперегнанного п-метил-2-пирро- лидона смешивают с 1 частью раствора FeSO4 —HCI. Получаемый раствор содержит 10 мг Fe/л и может храниться 1 мес. 100 мг PVP вносят в градуированную 15 мл центрифужную пробирку. Добавляют 5 или 10 мл лива без СО2 (в зависимости от ожидаемого количества антоцианогенов — больше или меньше 50 мг/л). Пробирку закрывают увлажненной резиновой пробкой и встряхивают в течение 30 мин, перед удалением пробки содержимое пробирки для оседания пены несколько мщ- нут центрифугируют. Надосадочную жидкость сливают и остаток PVP промывают водой. К осадку добавляют 10 мл растворителя, перемешивают стеклянной палочкой, которую затем промывают бутанолом. Нагревают лробирку 30 мин в кипящей водяной бане. После охлаждения доводят объем смеси бутанолом до 15 мл и сильно перемешивают стеклянной палочкой. Центрифугируют 10 мин при 2500 об/мин. Надосадочную прозрачную жидкость красно-фиолетового цвета измеряют при 550 нм. Калибровочная линия по методу Макфарлана, которая строится по растворам цианидина, представляет собой прямую. При этом отмечается пропорциональность между количеством взятого на анализ пива и экстинкцией. Так как калибровочная по этому методу идет значительно круче, количество антоцианогенов, рассчитанное по методу Гарриса и Рикеттса, примерно в 1,5 раза выше, чем по методу Макфарлана.
Метод Франкен-Люикс [116]. Этот метод основывается на реакции между катехином и молибденовой кислотой, при которой возникает красное окрашивание. Поскольку антоцианогены также определяются этим методом, то анализ дает сведения о содержании важнейших полифенольных веществ, участвующих в образовании мути (т. е. о таниногенах).
Для анализа 10 мл пива вносят в колбу, добавляют 1 мл 1,5 М фосфатного буфера (pH 7,2), 1 мл 1%-ного раствора сульфата натрия, 1 мл 2%-ного раствора молибдата натрия и 1 мл воды и все тщательно перемешивают. Измерения осуществляют в течение 10 мин при 400 нм.
Пфеффер несколько модифицировал метод, а именно: вместо 1 мл 1,5 М фосфатного буфера использовал .2 мл 0,75 М буфера и воду уже не добавлял.
Этот метод очень прост и достаточно точен. Тем не менее должны быть проведены глубокие исследования в направлении изучения специфики окраски в результате реакции с различными веществами полифенольной природы. В частности, необходимо установить, зависит ли интенсивность образующейся окраски от степени полимеризации полифенолов.
Во ВНИИПБПе было проверено влияние мелано- идинов на определение таниногенов методом Франкен- Люикс. Были испытаны растворы меланоидинов, выделенных Тихомировой и Беленькой из пива, а также растворы модельных меланоидинов, полученных из глицина и глюкозы. Проверка показала, что ни те, ни другие меланоидины не влияют на определение.
Методы Еруманиса [137]. Еруманис разработал и предложил аналитическому комитету ЕВС два варианта метода определения общего количества полифенолов, основанного на реакции этих веществ с лимоннокислым железо-аммонием (III) в щелочной среде.
По 1-му варианту метода реагенты готовят следующим образом:
- В миксер вносят 10 г чистой натриевой соли КМЦ (карбоксиметилцеллюлозы), 2 г ЕДТА (этилендиаминтетрацетат, динатриевая соль) и примерно 500 мл дистиллированной воды. Все тщательно перемешивают до растворения всех комочков. Переносят количественно в литровую мерную колбу и доводят объем дистиллированной водой до метки. Нерастворенные частички удаляют центрифугированием.
- Для приготовления железного реагента 2,5 г коричневого цитрата железо-аммония (III) растворяют в 100 мл 0,1%-ного раствора уксуснокислой ртути.
- Аммиак (концентрированный) разводят 2 объемами дистиллированной воды.
Для приготовления контрольного образца в бюретку вносят 10 мл дистиллированной воды, открывают кран и дают части воды стечь для удаления воздуха из крана. Кран закрывают, когда в бюретке останется 3—4 мл Н2О. Вводят в бюретку слой ваты примерно высотой 5 мм и осторожно выравнивают ее стеклянной палочкой. Затем также вводят слой стеклянной ваты (5 мм). Отвешивают 120 мг Поликлара АТ и смывают его медленно дистиллированной водой в бюретку. После того как вода сойдет из бюретки, колонку осторожно промывают водой (примерно 8 мл), затем осторожно по стенке бюретки наливают 10 мл дегазированного пива, открывают кран и дают пиву стекать в мерную колбу на 25 мл. Промывают колонку трижды по 1,5 мл дистиллированной воды. В мерную колбу с пивом добавляют 8 мл реагента 1, встряхивают, добавляют 0,5 мл железного реагента 2, перемешивают и добавляют 0,5 мл реагента 3. После перемешивания доводят объем смеси дистиллированной водой до метки, снова перемешивают и измеряют оптическую плотность при 525 нм против дистиллированной воды.
Одновременно с контролем в мерную колбу на 25 мл вносят пипеткой 10 мл пива и добавляют те же реагенты и в той же последовательности, что и в контроле. Через 10 мин измеряют оптическуйэ плотность при 525 нм против дистиллированной воды в 10 мл кювете.
Разница между оптической плотностью в главном опыте и в контрольном после умножения на коэффициент 630 дает содержание полифенолов в 1 л пива (в мг). Коэффициент получен из калибровочных кривых, построенных по полифенолам солода, хмеля и пива.
По 2-му варианту метода (более простому) пиво освобождают от СО2. Мутное пиво или сусло осветляют центрифугированием.
10 мл пива и 8 мл реагента 1 (КМЦ) вносят пипетками в одну мерную колбу на 25 мл, тщательно перемешивают, добавляют 0,5 мл железного реагента 2, перемешивают, добавляют 0,5 мл реагента 3 и снова перемешивают. Доводят объем водой до метки и перемешивают. Через 10 мин измеряют оптическую плотность в 10 мл кювете при 600 нм против дистиллированной воды.
Контроль I —в мерную колбу на 25 мл вносят 10 мл пива и 8 мл реагента 1, добавляют 0,5 мл реагента 3, доводят до метки и через 10 мин измеряют оптическую плотность так же, как и в главном опыте.
Контроль II — вместо пива берут 10 мл дистиллированной воды, остальное проводят все так же, как и в контроле I.
Содержание полифенолов (в мг/л) находят по формуле:
[Л —(В + С)] 820,
аде А,—оптическая плотность раствора в главной* опыте;”
В—то же, в контроле I;
С — тоже, в контроле II.
Еруманис установил, что на определение полифенолов влияют меланоидины, редуцирующие сахара, цистеин и аскорбиновая кислота. В варианте 2 эти вещества не принимаются во внимание, в варианте 1 влияние этих веществ исключено. Однако аналитический комитет ЕВС принял именно второй вариант для широкой проверки и апробации.
Для определения антоцианогенов Еруманис рекомендует метод Макфарлана с небольшими модификациями. Он отмечает, что при определении антоцианогенов с помощью цветной реакции с кислотой при нагревании интенсивность окраски снижается в том случае, если антоцианогены полимеризованы. Следовательно, интенсивность окраски пропорциональна не количеству антоцианогенов, а в значительной степени их полимеризации. В то же время определение общего количества полифенолов по реакции с железом не зависит от степени полимеризации полифенолов: были получены идентичные значения при определении простых и конденсированных полифенолов. Отсюда следует, что отношение общего количества полифенолов к количеству антоцианогенов, определенному нагреванием в кислой среде, будет тем больше, чем более полимеризованы антоцианогены. Еруманис предложил обозначать это отношение как индекс полимеризации, причем он отмечает, что определение только одних антоцианогенов бесцельно. Определение только тогда имеет смысл, когда одновременно производится определение общих полифенолов.
Эти соображения Еруманиса могут быть применимы только в случае определения антоцианогенов методами, основанными на нагревании их в кислой среде (т. е. методами Гарриса и Рикеттса, Макфарлана и др.). Если же антоцианогены определяются другими методами, для которых не установлена зависимость от степени полимеризации, соотношение значений общих полифенолов и антоцианогенов указывает только на долю антоцианогенов (и катехинов) в общем количестве полифенолов. В этом случае лучше определять процентное содержание антоцианогенов от общего количества полифенолов.
По нашему мнению, вряд ли правильно трактовать изменение в количестве антоцианогенов только с точки зрения их полимеризации. Это изменение может отражать различие в качественном составе полифенольных веществ.
Басаржова и Черна [84] сравнили несколько методов определения полифенолов и показали, что наименьшее количество полифенолов дает 1-й вариант метода Еру- маниса, как более точный и специфичный. На данные других методов влияют, очевидно, вещества неполи- фенольной природы, присутствующие в сусле и пиве. Но 2-му варианту метода Еруманиса в сусле определяется на 11—25%, а в пиве на 32% больше полифенолов, чем по 1-му варианту. Содержание антоцианогенов, определяемое методом Гарриса и Рикеттса, составляет 23—26% от полифенолов, определенных по 2-му варианту метода Еруманиса.
Метод Дадика [105]. Существенным моментом нового метода определения в пиве таниногенов — катехинов и антоцианогенов — является то, что в нем учитывается различие в абсорбции при двух длинах волн (455 и 545 нм) окрашенных продуктов, образующихся из катехинов и антоцианогенов при нагревании со спиртовым раствором НС1. Лейкоцианидин при нагревании со смесью пропанол (бутанол) — НС1 (5:1) образует пигмент с наибольшим максимумом при 545 нм и небольшим максимумом при 455 нм. d ( + )-Катехин, обработанный таким же образом, дает пигмент с наибольшим максимумом при 455 нм и небольшим максимумом при 545 нм. С помощью этого метода было определено количество таниногенов в 6 фракциях, полученных десорбированием адсорбата из 100 мл пива на Нейлоне-66. Суммарное количество таниногенов составило 150 мг/л, причем преобладали производные катехина.
Метод Нг и Мосека [172]. Метод основан на осаждении полифенолов уксуснокислым свинцом в кислой и щелочной среде. Предварительно таким же способом выделяют полифенолы пива и используют их для построения калибровочной кривой после анализа образующегося осадка на полипептиды, полисахариды и минеральные вещества. Количество полифенолов рассчитывали по разнице между массой осадка и содержанием в нем указанных выше веществ.
Точно отмеренные 100 мл пива выливают в 400 мл ацетона при энергичном перемешивании, центрифугируют и надосадочную жидкость концентрируют в ва- куум-испарителе при 35° С примерно до 60 мл. Добавляют к полученному концентрату 5 мл насыщенного водного раствора уксуснокислого свинца, центрифугируют и полученный осадок обозначают как кислый. Доводят pH надосадочной жидкости до 8,5 концентрированным NaOH, центрифугируют и надосадочную жидкость выбрасывают, осадок обозначают как щелочной.
Добавляют к кислому осадку примерно 40 мл промытой смолы Dowex 50 Н+, осторожно перемешивают и выливают в 100 мл этилацетата, 10 мин перемешивают и центрифугируют. Повторяют то же самое с порцией 50 мл этилацетата, собирают и объединяют фильтраты. Упаривают фильтраты в ротационном испарителе до сухой массы при 35° С и растворяют в 10 мл метанола. Полученную фракцию называют кислой.
Добавляют к щелочному осадку примерно 80 мл сухой смолы Dowex 50 Н+ и приготовляют щелочную фракцию так, как описано приготовление кислой фракции.
Для проведения цветной реакции выбран окрашивающий реагент, который имеет наименьшее взаимодействие с белками и углеводами, — 4-аминоантипирин.
В мерную колбу на 10 мл вносят 0,5 мл кислой или щелочной фракции, добавляют 1 мл 15%-ного NH4OH, 0,5 мл 2%-ного водного раствора 4-аминоантипирина и 0,5 мл 2%-ного водного раствора КзРе(СМ)6. Объем доводят водой до 10 мл. Сосуд хорошо встряхивают и оставляют стоять 45 мин. Приготовляют контроль таким же образом, но без образца фракций. Оптическую плотность определяют при 550 нм. Расчет ведут по калибровочной кривой.
Было найдено, что количество полифенолов в кислой фракции колебалось от 10,4 до 20,3 мг/100 мл пива, в щелочной — от 34,3 до 42,0 мг. Отмечалась значительная разница в окраске: кислая фракция давала коричневую окраску, щелочная — красную. Эта окраска соответствовала стандартам — катехину и сиреневой кислоте соответственно. Следовательно, полифенолы в двух фракциях существенно различны: в кислой содержатся й основном флавоноидные вещества, в щелочной — феноловые кислоты.
Полученные этим методом значения трудно сравнивать с величинами, определяемыми другими методами, поскольку в большинстве методов не учитываются вещества, содержащиеся в щелочной фракции. В трех образцах канадского пива этим методом было найдено 678, 786 и 593 мг/л полифенолов, что значительно выше обычно указываемых в литературе.
Методы, основанные на определении интенсивности помутнения пива на холоде. Несмотря на большое число методов определения полипептидов и полифенолов в пиве, необходимых для оценки действия стабилизаторов, ни один из них не дает отчетливой корреляции с фактической коллоидной стойкостью пива. По мнению многих исследователей, наиболее адекватные результаты дают методы, основанные на измерении холодного помутнения.
Часто с этой целью используют простой метод: пиво в бутылке или разлитое высоким столбиком в пробирки, плотно закрытые резиновыми пробками, помещают в воду со льдом, а сосуд с водой ставят в холодильник. Точно через 24 ч измеряют помутнение пива с помощью мутномера, если определение проводится на бутылочном пиве, или на ФЭКН, быстро определяют мутность пива в пробирках. В последнем случае трудно избежать ошибки, связанной с возможным небольшим нагреванием пива при определении. Но для быстрой сравнительной оценки склонности различных образцов пива к помутнению на холоде этот простой метод вполне применим. Нефелометрические показания ФЭКН могут быть прокалиброваны или по формазиновому стандарту, или по большому числу параллельных определений на мутномере и ФЭКН.
Свежеразлитое пиво не всегда дает заметное образование мути после 24-часовой выдержки при 0° С. Это объясняется тем, что растворимость имеющихся в пиве полипептидно-полифенольных комплексов еще велика, поскольку в этих комплексах участвуют малополимери- зованные, достаточно простые полифенолы.
Шапон [97, 159] предложил способ, которым можно выявить склонность пива к образованию мути уже на ранних стадиях его хранения. К пробам пива добавляютот 1 до 6%' этилового спирта и помещают их в специальный рефрижераторный нефелометр при температуре —8° С. Через 40 мин проводят измерение. Шапон считает, что эта проба приводит к осаждению существующих в пиве комплексов, концентрация которых еще недостаточна для образования мути при 0° С. Он полагает также, что такая проба может быть характеристикой пива с точки зрения возможной стойкости. Разные образцы пива дают различное помутнение при добавлении спирта и охлаждении до —8° С (рис. 40), причем более пологая кривая свидетельствует о высокой стабильности пива.
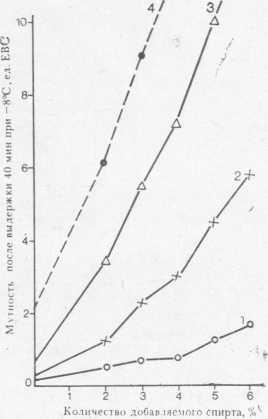
Рис. 40. Интенсивность помутнения различных образцов (1—4) охлажденного пива при добавлении этилового спирта.
Французские исследователи [159] собрали данные по 10 заводам за год и рассчитали коэффициент корреляции между двумя параметрами: мутностью пива через 6 мес и показателем в тесте «спирт — холод» по Шапону. Коэффициент корреляции (г— 4-0,655) оказался высокозначимым. На рис. 41, взятом из работы этих авторов, показаны кривые помутнения нескольких образцов одного и того же пива, подвергнутого различной стабилизирующей обработке.
Недостатки метода Шапона состоят в том, что для его осуществления требуется специальное, довольно сложное оборудование; в нем не находит отражения процесс изменения полифенолов, происходящий при длительном хранении или при тепловом воздействии (пастеризация).
Попытки учесть последнее обстоятельство делаются в так называемых ускоренных тестах, или тестах на ускорение старения пива. Эти тесты заключаются в выдержке пива при высокой (40—60° С) и низкой (0°С) температурах. При разработке этих способов исходят из той предпосылки, что выдержка пива при высокой температуре должна значительно усилить те процессы (главным образом окислительную и катализируемую кислой средой конденсацию полифенолов), которые медленно протекают в пиве при хранении в условиях комнатной температуры.
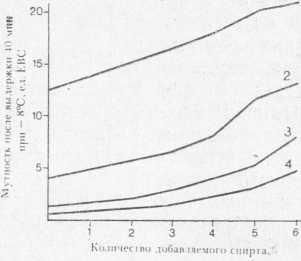
Рис. 41. Влияние этилового спирта на помутнение охлажденного до —8° С пива:
1 — необработанного; 2 — обработанного танином; 3 — протеолитическим ферментом; 4 — обоими стабилизирующими средствами.
Наиболее широко используются два варианта проведения ускоренного теста. В первом чередуется выдержка бутылочного пива в течение 24 ч при 40 или 60° С и при 0°С. После холодной выдержки измеряют мутность с помощью соответствующего нефелометра. Наиболее часто для этой цели применяют Haze Meter. Такое чередование нагревания — охлаждения продолжают до тех пор, пока мутность пива не станет равна 2 ед. ЕВС. Результаты проверки выражают числом циклов нагревания.
Второй вариант ускоренного теста, официально принятый комитетом ЕВС в 1963 г., состоит в том, что 5 или 6 бутылок с пивом помещают при 40° С (нестаби- лизированное пиво) или при 60°С (стабилизированное пиво) на 7 сут, после чего переносят их на 24 ч при О3 С и измеряют возникающее помутнение на Haze Meter. В этом случае результаты проверки выражаются прямо в единицах мутности ЕВС. Стойкое пиво должно при таком анализе давать мутность не более 2 ед. ЕВС.
Сокращенно этот анализ обозначают так: (7/1— 40° С/0°С).
Использование различной температуры для опытного (стабилизированного) и контрольного пива встречает возражение со стороны многих исследователей, причем большинство считают более приемлемой температуре 40° С.
Эти тесты дают весьма ценную информацию. Молль и др. [159] рассчитали коэффициент корреляции между прозрачностью пива через 6 мес (у) и результатами теста 7/1—40°С/0°С (х).
Уравнение регрессии имело вид: t/=0,82 + 0,29x.
Коэффициент корреляции (г=+0,695) был высокозначимым.
Пересчет данных ускоренных тестов на фактическую стойкость пива сопряжен с большими трудностями. Например, при пересчете числа циклов по первому варианту ускоренного теста предлагаются различные коэффициенты, которые позволяют пересчитать число циклов в дни стойкости. Шильд и др. предлагают коэффициент 22. Так, если пиво выдерживает 8 циклов, то оно будет прозрачным (+/2 ед. ЕВС мутности) 176 дней, т. е. почти 6 мес.
Польские исследователи [221] предлагают следующую формулу для пересчета числа циклов в дни стойкости:
Х=[(2 — a)l(b-a) + K\Z,
где X —действительная стойкость пива, дни;
а и b — мутность пива соответственно при предпоследнем и последнем определениях, ед. ЕВС;
К — число «теплых суток» до предпоследнего определения мутности пива.
Более или менее точные результаты получаются в том случае, если каждый завод предварительно установит для своего пива коэффициент Z в этой формуле. Для исследованных образцов пива с 6-месячным гарантийным сроком стойкости, стабилизированных разными препаратами, значение Z колебалось в пределах 6,1—20,1 и в среднем составляло 11,2.
Недостатком ускоренных тестов ЕВС является то, что определение в них производится довольно длительно — по второму, официальному, способу — за 8 дней. Чехословацкие исследователи [82] разработали более быстрый метод «шока», пользуясь которым можно получить представление о коллоидной стойкости пива уже через 33 ч. Способ заключается в том, что не менее 3 бутылок пива помещают при 0° С на 6 ч, затем после быстрого подогревания примерно до 40° С оставляют бутылки при 66° С на 16 ч, охлаждают до 20° С и снова помещают при 0° С на 6 ч, после чего измеряют мутность.
Во ВНИИПБПе разработан и применяется [64] вариант лабораторного метода «ускоренного теста», который заключается в том, что пиво, разлитое высоким столбиком, почти под пробку, в пробирки, закрытые резиновыми пробками, помещают на 2 сут при температуре 40° С, затем на сутки при 0° С, после чего на ФЭК.Н измеряют возникающее помутнение. Сокращенно анализ обозначается как 2/1—40°С/0°С.
Помимо длительности «ускоренных тестов», многие ученые считают их вообще не правомерными, поскольку, как отмечает Шапон, при 40 и 60° С могут ускоряться не только те реакции, которые медленно протекают при комнатной температуре, но могут возникать новые, несвойственные обычным условиям хранения реакции. Тем не менее эти методы в настоящее время дают наиболее адекватную информацию о состоянии коллоидных систем пива и о склонности его к помутнению.
Химические способы определения коллоидной стойкости пива. Метод Штайнера [224]. К 0,5 л пива добавляют 1 мл 40%-ного формальдегида, оставляют стоять 4 ч при 20° С, затем 3 ч при 0°С, после чего измеряют мутность, выражая ее в единицах ЕВС.
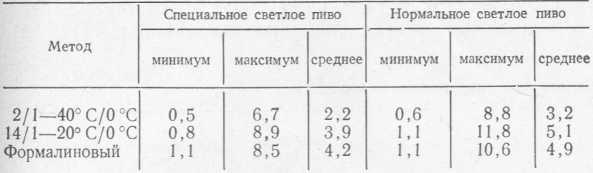
Данные этого метода сравнивали с данными двух гестов: 1) пиво выдерживали 2 сут при 40° С, затем на 24 ч помещали при 0°С; 2) пиво выдерживали 14 сут при 20° С, после чего также на сутки помещали при 0°С. В табл. 76 приведены результаты, полученные примерно по 100 образцам пива в каждом тесте на двух сортах пива.
Коэффициенты корреляции между данными формалинового метода, с одной стороны, и данными методов 2/1—40°С/0°С и 14/1—20°С/0°С, с другой, оказались высокозначимыми и равнялись для специального пива + 0,639 и +0,720, для нормального пива +0,686 и + 0,761 соответственно. Расчеты показывают, что быстрый формалиновый метод позволяет за 7 ч с высокой степенью вероятности оценить поведение пива после суточного охлаждения спустя 2 нед хранения. К сожалению, отсутствуют данные о корреляционной зависимости между данными этого метода и коллоидной стойкостью пива после более длительного срока его хранения.
Сравнение методов
Цинхониновый метод Томсона и Форварда [233]. Метод основан на свойстве полимеризованных полифенолов образовывать нерастворимые комплексы с алкалоидами. С помощью перекиси водорода и пероксидазы производят быстрое окисление, полифенолов пива и после добавления раствора сульфата цинхонина измеряют на нефелометре образующуюся муть. Таким образом в методе учитываются легкоокис- ляемые полифенолы.
К 40 мл пива добавляют 160 мл воды и измеряют мутность (Я]) в кювете 55 мм в нефелометре Хелма. К другим 40 мл пива добавляют по каплям с постоянным перемешиванием 1 мл Н2О2 (0,2 М, приготовляется перед использованием). Через 1 мин после добавления перекиси вносят по каплям 0,4 мл свежеприготовленного раствора пероксидазы хрена (0,04%) и оставляют на 30 мин. Затем добавляют 160 мл насыщенного раствора сульфата цинхонина (1,7%, профильтрованный через стеклянный фильтр), тщательно перемешивают и через 1 ч измеряют мутность (Я2). Количество окисляемых полифенолов равно разности Я2 и Я] и выражается в единицах Хелма.
Количество полифенолов в пиве, способных к взаимодействию с сульфатом цинхонина, можно определить таким же образом, исключив стадию окисления. Температура мало влияет на определение. Этим методом анализировали два типа пива — светлое и темное, стабилизированное и нестабилизированное (табл. 77).
Таблица 7
Анализ пива цинхониновым, методом

Значительное улучшение стойкости сопровождается сильным снижением количества окисляемых полифенолов и уменьшением содержания антоцианогенов. Была установлена обратно пропорциональная зависимость между цинхониновой мутью (количеством окисляемых полифенолов) и стойкостью пива (рис. 42).
Недостаток метода в том, что сульфат цинхонина — труднодоступное вещество.
Методы оценки окислительно-восстановительных свойств пива. Окислительно-восстановительные свойства пива отражают состояние его окисленности и имеют непосредственное отношение к стойкости.
Количество редуцирующих веществ, обусловливающих окислительно-восстановительные свойства пива, определяют по скорости обесцвечивания (восстановления) пивом определенного количества индикатора 2,6-ди- хлорфенолиндофенолята натрия: чем больше в пиве редуцирующих веществ, тем быстрее обесцвечивается добавленный индикатор. Если же пиво подвергалось окислительным воздействиям, в результате которых часть редуцирующих веществ оказалась окисленной, обесцвечивание индикатора происходит медленнее.
Таким образом, скорость восстановления индикатора является мерой концентрации и природы восстанавливающих веществ в данном образце пива. Для измерения степени окисленности пива и характеристики его восстанавливающей способности предложен ряд методов, основанных на восстановлении этого индикатора.
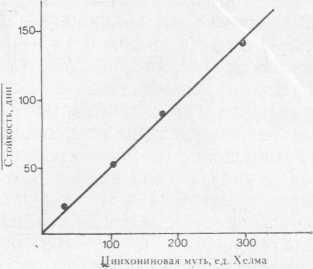
Рис. 42. Соотношение между стойкостью и цинхониновой мутью
Методом ITT (Indicator Time Test) устанавливают время (в секундах), которое требуется для полного обесцвечивания некоторого количества раствора индикатора, добавленного к определенному объему пива [13]. Чем больше величина ITT, т. е. чем медленнее обесцвечивается индикатор, тем сильнее окислено пиво и тем меньше в нем веществ, обладающих сильной восстанавливающей способностью. На определение не влияет присутствие растворенного кислорода, однако при сильной аэрации пива значение ITT изменится (увеличится). В присутствии аскорбиновой кислоты измерять ITT невозможно — индикатор обесцвечивается мгновенно.
Клоппер предложил другой метод определения окислительно-восстановительного состояния пива под названием «метод редокститрации». В этом методе определяют количество обесцвеченного индикатора за определенное время (20 с). Результаты выражают в микро- грамм-эквивалентах (микровалях) веществ, обладающих сильной редуцирующей способностью.
Некоторые исследователи применяют такой вариант метода, в котором прослеживается динамика восстановления индикатора. В методе Де Клерка с сотрудниками
[107] и Главачека [133] отмечается количество восстановленного (обесцвеченного) индикатора (в процентах или микрограммах) за 15 с, 5 мин и 15 мин. По мнению исследователей, обесцвечивание за эти отрезки времени производится разными веществами, обладающими различной восстанавливающей способностью (см. с. 107).
Беленькая и Тихомирова [9] предложили еще один вариант метода определения окислительно-восстановительного состояния пива. Метод является модификацией! метода Штайнера, в котором с помощью спектрофотометра определяется процент обесцвечивания 2.6-дихлор- фенолиндофенолята натрия в течение определенного) времени после прибавления красителя к пиву.
В предлагаемом методе учтено влияние pH пива на- цвет индикатора. Готовят буферные растворы с pH! 3,5 —6,5 и к 10 мл каждого раствора добавляют 0,25 мл 0,005 М раствора красителя. Измеряют на ФЭК оптическую плотность этих растворов — Do— (светофильтр 6, кювета 10 мм) против воды. Строят калибровочную кривую значений Do от величины pH (калибровочная имеет вид прямой линии).
К 10 мл исследуемого образца пива прибавляют 0,25 мл 0,005 М раствора красителя. Через 60 с после добавления растворов измеряют оптическую плотность в тех же условиях — Dx. Для сравнения используют сусло (пиво), к которому не прибавляют красителя. Затем измеряют pH пива и по калибровочной кривой находят величину Do. Рассчитывают процентное обесцвечивание красителя (ПОК), которое является величиной, пропорциональной содержанию в пиве быстро восстанавливающих веществ (редуктонов).
Во ВНИИПБПе несколько видоизменили этот метод и прослеживали динамику восстановления (обесцвечивания) красителя на протяжении 10 мин, снимая показатели оптической плотности опытного образца через каждую минуту. На рис. 43 приведена динамика изменения ПОК в двух образцах пива, выдержанных после розлива 2 сут при температуре 25 или 40° С. Снижение величины ПОК в последнем образце пива свидетельствует о прошедших в нем окислительных процессах.
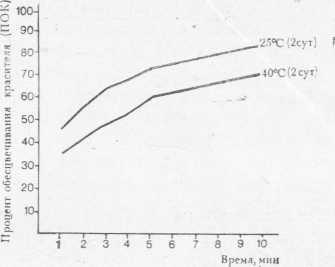
Рис. 43. Динамика восстановления индикатора в зависимости от температуры хранения пива.
Методы определения окислительно-восстановительных свойств пива несложны и легко выполнимы в любой заводской лаборатории. С их помощью можно получить данные о степени окисленности пива для принятия соответствующих технологических решений с целью уменьшения контакта с воздухом. Методы непосредственного определения содержания воздуха в пиве на различных стадиях его изготовления более сложны и трудно выполнимы в заводских лабораториях.
Из обширного перечня методов для практического использования в заводских' лабораториях могут быть в настоящее время рекомендованы следующие: 1) измерение мутности в мутномерах (с. 220); 2) определение количества высокомолекулярных полипептидов, способных реагировать с танином (метод ВНИИПБПа) (с. 235); 3) определение таниногенов по Франкен-Люикс (с. 240); 4) определение полифенолов по Еруманису (с. 241); 5) определение интенсивности помутнения пива на холоде (с. 246); 6) ускоренные тесты на холодную муть (с. 247); 7) определение окислительно-восстановительного состояния пива по Беленькой и Тихомировой (с. 254). 4
Для более полного микробиологического контроля рекомендуется использовать питательные среды, прописи которых приведены на с. 221—226.

