Известно применение в качестве улучшителей некоторых химических соединений, из них наиболее эффективными и распространенными являются улучшители окислительного действия.
Улучшители окислительного действия
Из улучшителей окислительного действия следует назвать броматы, йодаты, персульфаты, пербораты, перкарбонаты, аскорбиновую и дегидроаскорбиновую кислоты, пропионаты и ванадаты.
Наиболее распространено использование броматов, йодатов и персульфатов. Наиболее широкое применение находит бро- мат калия (КВгОз), употребляемый обычно в количестве 0,001 — 0,003% от веса муки. Несколько реже применяется йодат калия (KJ03) в количестве 0,0004—0,0008% от веса муки. В некоторых случаях применяется персульфат аммония (NН4)2S2О8 в количестве 0,01—0,02% от веса муки. Указанные выше дозировки бромата и йодата, остающиеся в пределах тысячных и десятитысячных долей процента от веса муки, говорят о том, что это очень эффективные и сильно действующие улучшители.
Несмотря на то, что применение персульфата аммония было предложено в 1911 г., а бромата калия — в 1914 г. и с тех пор эти препараты широко использовались в разных странах, до 1935 г. было известно только то, что эти улучшители резко увеличивают объем хлеба, особенно при работе на муке из мягких пшениц со слабой клейковиной. Наблюдалось также, что мякиш хлеба делался несколько более светлым, а корка несколько более румяной, и что при чрезмерном увеличении дозы этих улучшителей хлеб получался плотный, уменьшенного объема. Этим и исчерпывалось все, что было достоверно известно о действии этих окислительных улучшителей.
Попытки истолкования химизма действия этих улучшителей обычно приводили к ссылкам на влияние их на коллоидные свойства теста. Указывалось также, что окислительные улучшители действуют стимулирующе на дрожжи и на вызываемое ими брожение. Некоторые, даже основанные на экспериментах, работы не дали удовлетворительного объяснения действию окислительных улучшителей. В одной из таких работ видели-основную причину эффективности этих улучшителей в действии их на фосфатиды муки, а во второй —склонялись уже к коллоидно-химическому их действию в качестве электролитов, а не окислителей. Мы не останавливаемся на некоторых еще менее обоснованных предположениях, вроде предположения о влиянии кислорода улучшителей на дыхание протоплазмы и т. п.
Датский исследователь Йоргенсен внес известную ясность в понимание природы действия йодатов и броматов (а также персульфатов). В августе 1935 г. Йоргенсен сообщил о результатах своих работ, убедительно доказывающих, что ни броматы, ни йодаты не действуют на газообразующую способность теста (персульфат аммония, применяемый в количестве 25 г на 100 кг муки, несколько стимулировал газообразование, но, как было доказано Йоргенсеном, за счет содержания в нем аммония, а не за счет окисляющего действия персульфата).
Взаимно контролирующими методами Йоргенсен доказал, что объяснение природы действия йодатов, броматов, персульфатов и перборатов лежит в действии этих окислителей, парализующем (тормозящем) протеолитические ферменты муки. Йоргенсен сделал предположение, что всякое вещество, инактивирующее протеолитические энзимы муки, должно быть улучшителем хлебопекарных свойств муки, аналогичным по своему действию хотя бы бромату калия.
В качестве примера такого вещества он привел аскорбиновую кислоту (витамин С), которая была известна не как хлебопекарный улучшитель, но как парализатор действия растительных протеиназ. Проверка ее свойств в качестве хлебопекарного улучшителя полностью оправдала ожидания Йоргенсена и лишний раз подтвердила принципиальную правильность его гипотезы о природе действия броматов и других аналогичных им окислителей.
Со времени упомянутой работы Йоргенсена можно считать общепринятым, что окислительные улучшители не стимулируют газообразование в тесте, а благоприятно действуют на его белково-протеиназный комплекс. Рядом последующих работ разных авторов установлено, что тормозящее протеолиз действие этих улучшителей связано с их окислительным действием, с вызываемым ими сдвигом окислительно-восстановительного потенциала теста в окислительном направлении.
Работы нескольких исследователей, проведенные в 1935 г., показали, что окислительно-восстановительный потенциал муки гН колеблется в довольно узких пределах (от 15 до 19). Существенно также то, что окислительно-восстановительный потенциал муки не отличается большой устойчивостью, что его легко изменить добавками очень незначительного количества веществ окислительного или восстановительного действия. В бродяшем тесте гН изменяется в сторону восстановительных свойств, усиливающихся по мере брожения теста. Опыты показали, что тесто из муки со значением гН, равным 18—19, после 3—4 час. брожения приобретало резко выраженные восстановительные свойства, и гН приблизительно был равен 15.
Восстановительные свойства теста настолько заметны, что добавляя к бродящему тесту сублимированную серу, можно явственно ощущать запах сероводорода, получающегося в результате восстановления серы.
Начиная с работы Йоргенсена, опубликованной в 1935 г., подавляющее большинство исследователей связывает окислительно-восстановительные процессы в тесте с его протеолизом — с влиянием окислительно-восстановительных процессов на соединения, содержащие сульфгидрильную группу — SH. В составе биологических систем большую роль играют соединения типа R—SH (где R — условно обозначаемый радикал). Эти соединения способны к окислительно-восстановительным превращениям по схеме:
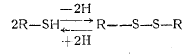
Окисление ведет к образованию дисульфидного соединения, а -восстановление—к образованию -соединения со -свободной тиоловой (сульфгидрильной) группой. Из соединений этого типа можно указать на широко распространенный в растительном мире глютатион, имеющий формулу:
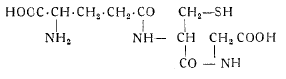
Глютатион представляет собой трипептид, содержащий остатки глютаминовой кислоты, цистеина, включающего группу — SH, и глицина.
При окислении две частицы глютатиона дают соединение с дисульфидной связью, имеющее следующую формулу:
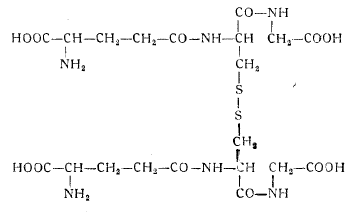
Обычно глютатион в восстановленном состоянии обозначают как G—SH, а в окисленном состоянии как G—S—S—G. Этими обозначениями мы будем пользоваться в нашем дальнейшем изложении. Глютатион в относительно больших количествах содержится в хлебопекарных дрожжах. В зерне пшеницы он содержится преимущественно в зародыше. Активную группу в глютатионе составляет остаток цистеина, содержащий группу — SH.
Цистеин имеет формулу:
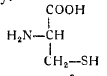
и представляет собой α амино β—тиопропионовую кислоту.
При окислении две молекулы цистеина образуют цистин, имеющий формулу:
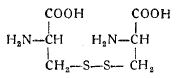
Отметим кстати, что цистеин входит в небольших количествах в состав глиадина и глютелина пшеницы.
Существенным является также установленное работами Берзина и других исследователей наличие группы — SH и в составе самого пэпаина и, повидимому, в протеиназе пшеницы.
Соединения, содержащие сульфгидрильную группу, играют исключительно важную роль в действии растительных протеиназ типа папаиназ, к которым принадлежит и протеиназа пшеницы.
В восстановленном виде соединения, содержащие группу—SH, активируют протеолиз. В главе III мы приводим примеры активирующего протеолиз действия цистеина и глютатиона дрожжевой воды. В окисленном состоянии, в виде дисульфидного соединения, они не действуют уже активирующе на протеолиз, вызываемый растительными протеиназами типа папаина. Больше того, вполне вероятно, что в окисленном состоянии дисульфидные соединения, сдвигая гН в окислительную сторону, могут изменять направленность действия протеиназ даже в сторону синтеза.
Об этом позволяют говорить работы Благовещенского и Юргенсон и Благовещенского, показавших, что применение окислительной системы (перекись водорода плюс пероксидаза) не только не прекращало протеолитического распада белкового вещества, но и вызывало синтез белкового вещества, устанавливаемый по приросту азота, осаждаемого трихлоруксусной кислотой.
В этом отношении показательно также, что добавление к бродящему тесту окисленного глютатиона (G—S—S—G) не только не вызывало ухудшения его физических свойств, но имело результатом заметное улучшение их. Искусственно сдвигая гН теста с 16 до 27, т. е. в зону сильного окислительного действия, можно в результате вызвать заметное улучшение физических евойств теста.
Таким образом, можно считать установленным, что действие броматов, йодатов, персульфатов и других аналогичных им улучшителей связано с их окислительным действием в тесте, с переводом сульфгидрильных групп, активирующих протеолиз, в неактивную окисленную дисульфидную форму. Дискуссионным остается вопрос о том, не сопровождаются ли процессы активирования протеолиза соединениями, содержащими — SH, а процессы инактивирования этих соединений окислительными улучшителями — прямым воздействием и тех и других на белковые вещества муки в тесте. Отдельные авторы приходят, например, к заключению, что эти добавки оказывают непосредственное действие на серосодержащие звенья белковых молекул муки.
Необходимо иметь в виду, что броматы и йодаты требуют различных оптимальных условий для своего действия в качестве окислительных улучшителей, и поэтому броматы эффективно действуют только в достаточно кислой среде, более кислой, чем это необходимо для йодатов.
Это положение экспериментально подтверждено в одной из работ, показавшей, что йодаты проявляют свое окислительное действие более легко и быстро и в менее кислой среде, чем броматы. То, что для действия броматов требуется кислая среда, было установлено работой Проскурякова и Бундель и другими исследователями.
Интересные данные о ходе восстановления КВгО3 в процессе приготовления теста и выпечки приведены в табл. 86.

Около половины всего бромата восстанавливается во время замеса, очень немного расходуется в период брожения, остаток полностью восстанавливается во время выпечки. Форсированное восстановление бромата происходит, очевидно, в результате действия температуры. Интенсивное окисление глютатиона броматом калия наблюдается в интервале между 50—90°.
В некоторых работах, проведенных за последние годы, отмечается, что эффект улучшающего действия бромата находится в зависимости от длительности и интенсивности механической обработки теста, в процессе его замеса, обминки, прокатки и разделки.
При изучении влияния добавок к тесту протеиназы, глютатиона и бромата, при замесе и повторном промесе в атмосфере воздуха, кислорода и азота были получены следующие результаты (рис. 119). Если к тесту из муки, дающей нормальный хлеб 1 добавить некоторое количество протеиназы или глютатиона, то будет получен хлеб 2, худшего качества и меньшего объёма вследствие ухудшения физических свойств теста в результате усиленного протеолиза. Если к такому тесту добавить бромата или произвести замес его в атмосфере кислорода, что приведет к окислению — SH групп и торможению протеолиза, мы получим нормальный хлеб 3. Если к такому тесту добавить слишком много бромата, то хлеб 4 получится плотный, малого объема и с недостаточной пористостью, как из чрезмерно сильной муки. Повторный промес такого теста с излишним количеством бромата после его брожения механически ослабляет клейковину в тесте и приводит опять к возможности получения нормального хлеба 5. Однако, если повторный промес теста будет чрезмерно длительным, то, по мнению авторов, тесто, оставшееся чрезмерно долго в соприкосновении с кислородом воздуха, опять даст хлеб 6 пониженного объема. Длительный повторный промес теста после его брожения в атмосфере азота дает нормальный хлеб.
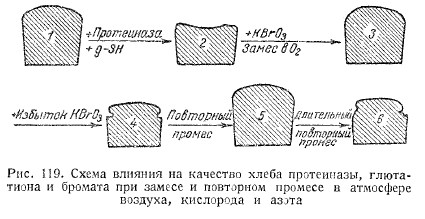
Предположения о том, что в атмосфере азота длительность механической обработки не играет роли, и о том, что плохой хлеб G получается при слишком продолжительном промесе теста с передозировкой бромата вследствие того, что при промесе он в течение большого промежутка времени остается в соприкосновении с кислородом воздуха, хотя и вытекают из результатов проведенной работы, вызывают все же сомнение.
В производственной практике применяют более длительный замес при работе на сильной муке и, по возможности, сокращенный замес при слабой муке, опасаясь в этом случае чрезмерного механического ослабления и без того слабой клейковины. Правильность такой практики подтверждают и результаты опытов, показавших, что чем больше дозировка бромата, тем большее механическое воздействие на тесто необходимо для получения хлеба наилучшего объема и качества.
Реакция разных образцов муки на добавление бромата. Отдельные авторы предлагают использовать экстенсограф для выявления, в какой мере исследуемая мука реагирует на добавление бромата калия.
В качестве показателя было предложено принять окси-число муки, определяемое по формуле:
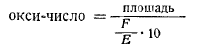
По величине окси-числа разбивают все образцы муки на группы соответственно табл. 87.


