Сорбция в двух изложенных ранее модификациях – ионный обмен и адсорбция микропористыми сорбентами – предполагает высокую селективность сорбентов или отсутствие в обрабатываемом растворе веществ, имеющих близкие характеристики по селективности. Между тем в биологических растворах часто оказывается смесь близких по природе веществ, имеющих в то же время различную биологическую активность. Сорбенты при этом адсорбируют всю эту смесь, да и при десорбции в конечном счете все эти вещества выделяются вместе, хотя и очищенными от других загрязняющих веществ. Возникает задача разделения этих близких по природе веществ.
Эту задачу выполняет процесс хроматографии. Хроматография известна больше в измерительной технике, где с ее помощью решают задачу количественного определения вещества, находящегося в сложной смеси близких по составу веществ (например, углеводороды нефти или углеводы в сложных природных смесях Сахаров). Между тем в технологии на тех же принципах основан процесс, который более точно называют препаративная хроматография. По существу, это специфический способ десорбции сорбированной любым способом смеси веществ, чаще всего на микропористых сорбентах.
Как уже было сказано, при обычной схеме десорбция не очень- то различает разные вещества близкого состава и молекулярной массы, которые при десорбции выделяются вместе. Хроматография позволяет это сделать.
При хроматографии поток элюента, выходящий из слоя сорбента, не собирается весь в одну емкость, а фракционируется по времени пропускания элюента через колонку.
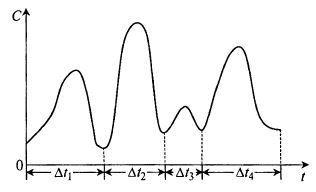
Дело в том, что десорбция разных по молекулярной массе или, точнее, разных по сродству к сорбенту веществ протекает с разной скоростью. Поэтому сначала в поток перейдут вещества с меньшей молекулярной массой и менее связанные с сорбентом, а затем все более и более трудно десорбируемые. Если измерять концентрацию вещества в потоке элюента во времени, то можно наблюдать ряд пиков различной высоты, разделенных участками низкой концентрации (рис. 16.5).
Рис. 16.5. График изменения во времени концентрации десорбируемого вещества в элюате:
С – концентрация вещества в элюате; t– время от начала десорбции (элюирования);
Δt1, Δt2, Δt3, Δt4 – интервалы времени для сбора различных фракций элюата, содержащих различные вещества
В измерительных приборах (хроматографах) высота и площадь пиков являются основой для определения концентрации вещества. В препаративной хроматографии поток элюента, собираемый за различные промежутки времени (Δt1, Δt2, ….Δtn), является основой для разделения смеси веществ на более однородные по составу растворы.
Так можно разделять разные белки, разные аминокислоты или разные сахара. За основу разделения берется время выхода, отсюда и название метода («хромато» – время).
Рассмотренный пример можно назвать адсорбционной хроматографией, он основан на поверхностном связывании растворенного компонента. Аналогично этому существует ионообменная хроматография, где сначала связываются, а затем с разной скоростью десорбируются ионы растворенных компонентов.
Интересной разновидностью хроматографии в биотехнологии является так называемая «аффинная хроматография». В ней для сорбции и десорбции используют биоспецифичное вещество, которое подходит к соответствующей выделяемой молекуле, как ключ к замку. Это могут быть ферменты или иммуносорбенты. Сначала практически полностью происходит связывание специфичного вещества, а потом путем изменения элюента оно выделяется с довольно четким фронтом.
Так можно разделять и ферменты, если в качестве сорбента использовать закрепленный на носителе «лиганд» – вещество, подобное субстрату, на который фермент действует. Разное сродство ферментов к субстрату может являться основой для их разделения по скорости образования и распада фермент-субстратного комплекса:
E1 + S ↔ E1S; E2 + S ↔ E2S; E3 + S ↔ E3S. (16.9)
Преимущества хроматографии:
- высокая селективность;
- возможность разделения веществ с близкими свойствами;
- мягкие условия проведения процесса.
Недостатки:
- более низкая скорость десорбции, необходимая для улавливания разных «пиков» выделения веществ;
- обычно более разбавленные растворы;
- более сложное аппаратурное оформление процесса.