Важность и разнообразие микробных продуктов
После исследований Пастера по спиртовому, масляному и молочному брожению главным достижением промышленной микробиологии можно считать открытие Вейцманном ацетонобутанолового брожения, относящееся к периоду первой мировой войны. Биосинтез пенициллинов методами ферментации в 1940-х гг. знаменовал собой начало эры современной промышленной микробиологии. Среди соединений, продуцируемых микроорганизмами, отметим следующие:

Для промышленност выбор между биосинтезом и химическим синтезом вещества определяется экономическими факторами. Вот почему такую важность и еет цена сырья. При микробном брожении сырьем обычно; являются полисахариды (крахмал, целлюлоза) или побочные продукты пищевой промышленности (меласса, молочная сыворотка и пр.). При химическом синтезе сырьем служит нефть или ее производные. Следует также принимать во внимание эффективность процеесса: количество субстрата, превращаемого в конечный продукт, длительность синтеза, стоимость отделения продукта от культуральной среды или от искусственных реагентов синтеза. Необходимо учитывать стоимость уничтожения отходов или побочных продуктов производственного процесса, равно как и стоимость их возможного использования.
Микроорганизмов, синтезирующих продукты или осуществляющих реакции, полезные для человека, несколько сотен видов (из более чем 100 000 видов, известных в природе). Их относят к четырем группам: бактерии, актиномицеты (филаментозные бактерии, обитающие в почве), дрожжи и плесени. Из 500 известных видов дрожжей первым люди научились использовать Saccharomyces cerevisiae, этот вид наиболее интенсивно культивируется. Многочисленные штаммы S. cerevisiae находят применение в пивоварении, виноделии, производстве японской рисовой водки (сакэ) и других алкогольных напитков, а также в хлебопечении. К дрожжам, сбраживающим лактозу, относится Kluyveromyces fragilis, который используют для получения спирта из сыворотки. Saccharomycopsis lipolytica деградирует углеводороды и употребляется для получения белковой биомассы. Все три ида принадлежат к классу аскомицетов. Другие полезные виды относятся к классу дейтеромицетов (несовершенны грибов), так как они размножаются не половым путем, а почкованием. Candida utilis растет в сульфитных сточных водах (отходы бумажной промышленности). Trichosporon cutaneum, окисляющий многочисленные органические соединения, включая некоторые токсичные (например, фенол), играет важную роль в системах аэробной переработа ки стоков. Phaffia rhodozyma синтезирует астаксантин-: каротиноид, который придает мякоти форели и лосося, выращиваемых на фермах, характерный оранжевый или розовый цвет.
Промышленные дрожжи обычно не размножаются половым путем, не образуют спор и полиплоидны. Последним объясняется их сила и способность адаптироваться к изменениям среды культивирования (в норме ядро клетки S. cerevisiae содержит 17 или 34 хромосомы, т. е. клетки гаплоидны или диплондны).
Плесени вызывают многочисленные превращения в твердых средах, которые происходят перед брожением, их наличием объясняется гидролиз рисового крахмала при производстве сакэ и гидролиз соевых бобов, риса и солода при получении пищи, употребляемой в азиатских странах (мисо, чуи и темпех). Плесени также продуцируют ферменты, используемые в промышленности (амилазы, протеазы, пектиназы), органические кислоты (лимонную, молочную), антибиотики. Их применяют в производстве сыров·(например, камамбера и рокфора).
Полезные бактерии относятся к эубактериям. Уксуснокислые бактерии, представленные родами Gluconobacter и Acetobacter, это грамотрицательные бактерии, превращающие этанол в уксусную кислоту, а уксусную кислоту в углекислый газ и воду. Род Bacillus относится к грамположительным бактериям, которые способны образовывать эндоспоры и имеют перитрихиальное жгутикование. В. subtilis строгий аэроб, а В. thuringiensis может жить и в анаэробных условиях. Анаэробные, образующие споры бактерии представлены родом Clostridium; С. acetobutylicum сбраживает сахара в ацетон, этанол, изопропанол и n-бутанол (ацетонобутаноловое брожение), другие виды могут также сбраживать крахмал, пектин и различные азотсодержащие соединения. К молочнокислым бактериям относятся представители родов Lactobacillus, Leuconostoc и Streptococcus, которые не образуют спор, грамположительны и не чувствительны к кислороду. Гетероферментатнвные молочнокислые бактерии рода Leuconostoc превращают утлеводы в молочную кислоту, этанол и уклекислый газ; гомоферментативные молочнокислые бактерии рода Streptococcus продуцируют только молочную кислоту, а брожение, осуществляемое представителями рода Lactobacillus, позволяет получить наряду с молочной кислотой ряд разнообразных продуктов. К бактериям рода Corynebacterium, неподвижные грамположительные клетки которых не образуют эндоспор, отньсятся патогенные (С. diphtheriae, С. tuberculosis) и непатогенные почвенные виды, имеющие промышленное значение. С. glutamicum служит источником лизина и улучшающих вкус 5'-нуклеотидов. Коринебактерии хотя и считаются факультативными анаэробами, но лучше всего растут аэробно. Они синтезируют каталазу, которая разлагает перекись водорода на воду и кислород.
Истинные актиномицеты-строго аэробные бактерии; они грамположительны и не образуют спор. Наиболее представительный в этой группе-род Streptomyces, отдельные виды которого продуцируют широко применяемые антибиотики. При росте на твердых средах актиномицеты образуют очень тонкий мицелий с воздушными гифами, которые дифференцируются в цепочки конидиоспор. Каждая конидиоспора способна образовать микроколонию. Антибиотики продуцирует и другой род актиномицетов, Micromonospora, колонии которого лишены воздушных гиф и образуют конидиоспоры непосредственно на мицелии.
К продуктам микробного брожения и метаболизма относятся первичные метаболиты, ферменты, капсульные полисахариды и сама клеточная биомасса (так назьшаемые белки одноклеточных организмов).
Производство первичных метаболитов
Первичные метаболиты-это низкомолекулярные соединения (молекулярная масса менее 1500 дальтон), необходимые для роста микробов; одни из них являются строительными блоками макромолекул, другие участвуют в синтезе коферментов. Среди наиболее важных для промьшшенности метаболитов можно выделить· аминокислоты, органические кислоты, пуриновые и пиримидиновые нуклеотиды, растворители и витамины. Микробные клетки, как и клетки других живых существ, не производят избытка первичных метаболитов, что бьшо бы расточительно и умевыпало способность к выживанию. Имеются, однако, микробные штаммы с нарушениями регуляции синтеза этих метаболитов, которые и служат исходными wтаммами для промьшшенных процессов.
В самом деле, многие аминокислоты и нуклеотиды производятся в процессе ферментаций, осуществляемых ауксотрофами (т. е. микробами, нуждающимися для воспроизведения в факторах роста), в метаболических путях которых нарушены процессы регуляции синтеза ферментов. Штаммы Brevibacterium flavum и Corynebacterium glutamicum превращают более трети сахаров, содержащихся в культуральной среде, в лизин; так получается не менее 75 г лизина на 1 л среды. Лизин-конечный продукт разветвленного метаболического пути, который также ведет к синтезу метионина и треонина. Лизин. и треонин регулируют этот путь, взаимодействуя с его первым ферментом аспартаткиназой; накопление обеих аминокислот ингибирует активность этого фермента. Первый mп мутаций в гене, кодирующем гомосериндегидрогеназу, нарушает активность этого фермента и блокирует синтез треонина и метионина; в результате удаляется один из ингибиторов этого фермента (треонин). Затем такой ауксотрофный мутант выращивают в среде, содержащей достаточно треонина и метионина для поддержания роста, однако имеющегося треонина мало для прекращения биосинтеза лизина, который продолжается с нормальной скоростью, что приводит к его накоплению. Мутации второго типа изменяют аспартаткиназу таким образом, что она перестает взаимодействовать с лизином и более не чувствительна к ингибированию по принципу обратной связи этой аминокислотой; последняя накапливается в мутантных клетках и затем в культуральной среде. Мутации второго типа могут быть отобраны, так как они пр щают клеткам устойчивость к соединению, называемому АЕС, которое настолько сходно с лизином, что имитирует его регуляторную функцию и полностью блокирует аспартаткиназу. В присутствии АЕС клетки дикого типа погибают (так как они не способны синтезировать лизин), а мутантные штаммы выживают.
Из 20 аминокислот, составляющих белки, восемь не могут синтезироваться в организме человека; эти незаменимые аминокислоты должны содержаться в. пище. Особенно важны метионин и лизин. Метионин производится синтетически, тогда как 80% лизина-биосинтетически (в 1980 г. путем ферментации было произведено 40 000 т лизина). Интерес к микробиологическому синтезу аминокислот объясняется также тем. что этот процесс приводит к получению биологически активных изомеров (L-аминокислот), в то время как при химическом синтезе получаются равные количества обоих изомеров. Поскольку их трудно разделить, половина продукции оказывается биологически бесполезной.
Глутаминовая кислота, которая в виде натриевой соли применяется в качестве специи, синтезируется исключительно культурами Corynebacterium glutamicum и Brevibacterium flavum (произведено 360 000 тв 1980 г.). В США в 1980 г. в пищевой промышленности нашло употребление 30 000 т продукта, причем треть была импортирована из Южной Кореи и Японии, где в это время производилосъ100 000 т глутамата (эджайномото) и 20 000 т лизина. Субстратом для этих видов ферментации служит глюкоза, однако в конце 1960-х гг. использовали n-парафины, что объяснялось их избытком и дешевизной. Еще одним потенциальным субстратом, не столь дорогим, как глюкоза, является уксусная кислота.
Когда Corynebacterium glutamicum растет в среде с меньшей, чем оптимальная, концентрацией биотина, нарушается синтез мембранных фосфолипидов, в результате глутамат натрия проходит через мембрану и накапливается в среде. То же происходит при добавлении к кулътуральной среде пенициллина: этот антибиотик подавляет синтез клеточной стенки и тем самым способствует выделению аминокислот.
Промышленное производство аминокислот, особенно лизина и метионина, будет развиваться не только для питания людей, но и для получения добавок в комбикорм· скота. Компания «Евролизин» в Амьене (Франция) ассигновала 27 млн. долл., чтобы добиться удвоения производства лизина. Растет также спрос на глицин, аланин и цистеин: первые две аминокислоты используются как приправы, а третья-для создания пористой структуры хлеба. Повышение спроса объясняется также использованием определенных аминокислот для лечения заболеваний желудка и печени.
Важнейшей промышленной органической кислотой является уксусная кислота. Она используется при производстве резины, пластмасс, ацетатных волокон, фармацевтических препаратов, инсектицидов и т. д. В Японии уксусная кислота применяется как субстрат при ферментации для производства аминокислот. В США в 1980 г. производилось свыше 1,4 млн. т этой кислоты (не считая уксуса); рыночная стоимость составляла 500 млн. долл. Окисление этанола в уксусную кислоту посредством уксуснокислых бактерий экономически выгодно лишь при получении уксуса. Общепринятый химический синтез основан на карбонилировании метанола. Проводились исследования по сбраживанию целлюлозы в уксусную кислоту под действием термофильных бактерий. Кроме того, отметим, что Clostridium aceticum и Acetobacter woodii способны превращать в уксусную кислоту углекислый газ и водород. Однако развитие связанных с этим производственных процессов зависит от дальнейшего изучения упомянутых бактерий. Лимонную кислоту получают из мелассы при помощи Aspergillus niger (рис. 8). В 1980 г. мировое производство лимонной кислоты составляло 175 000 т; ее рыночная стоимость составляла 259 млн. долл. Ферментативное производство может стать экономически более выгодным, если в качестве субстрата использовать целлюлозу. Целлюлозу в принципе можно разложить под действием штаммов А. niger, в которые будут перенесены гены целлюлаз.
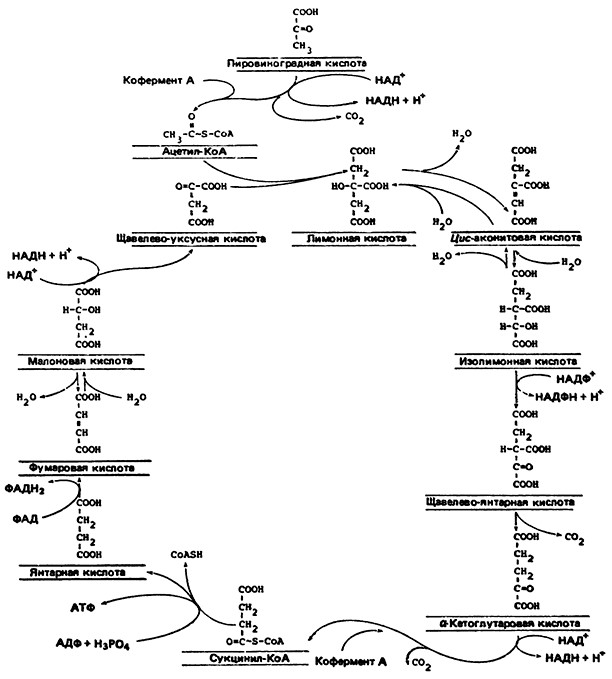
Рис. 8. Цикл трикарбоновых кислот, или цикл Кребса.
Пировиноградная кислота, которая получается при анаэробном гликолизе или в результате разрушения
других метаболитов, в аэробных условиях в клетках микробов, растений и животных разлагается в ходе
цикла трикарбоновых кислот. В последнем участвуют трикарбоновые кислоты (лимонная, цисаконитовая,
изолимонная и щавелевоуксусная). Молекула пировиноградной кислоты декарбоксилuруется и дегидрируется;
в результате получается углекислый газ и водород (т. е. протоны и электроны); водород при помощи
переносчиков электронов переносится к кислороду с образованием воды. Цикл трикарбоновых кислот
основной механизм производства энергии в клетке; энергия запасается в виде АТФ (аденозинтрифосфорной кислоты).
В производстве лимонной кислоты определенными штаммами микробов, растущих на углеводах,
используются те же ферментативные реакции, в ходе которых пировиноградная кислота
и щавелевоуксусная кислота превращаются в лимонную кислоту. Но лимонная кислота не вступает
в цикл Кребса, а накапливается.
Молочная кислота-первая из органических кислот, которую начали производить путем брожения. Она находит широкое применение в качестве окислителя в пищевой промышленности, как протрава в текстильной промышленности, а также в гальваностегии и производстве пластмасс. По данным 1980 г., в США и Европе ежегодно производилось 40 000 т молочной кислоты на общую сумму 56 млн. долл. Практически вся производимая в США молочная кислота синтезируется химическим путем, тогда как в Европе половину общего количества получают при сбраживании глюкозы Lactobacillus delbrueckii.
Ключевым фактором при нескольких видах брожения является нехватка определенных металлов. Так, производство лимонной кислоты при помощи Aspergillus niger происходит при нехватке железа и марганца, для продуцирования фумаровой кислоты Rhizopus negricans нужна нехватка цинка.
Воздействуя на регуляцию метаболизма и прибегая к генетическим манипуляциям, можно значительно повысить производство отдельных витаминов: например, Ashbya gossypii производит рибофлавина в 20 000 раз больше, чем необходимо для роста, а Pseudomonas denitrificans способен производить в 50 000 раз больше, чем необходимо, витамина В12.
Получение алкогольных напитков при помощи различных штаммов микроорганизмов основано на спиртовом брожении, в процессе которого сбраживаемый сахар исходного субстрата (крахмала или фруктового сока) превращается в этанол и дополнительные продукты. Такой тип брожения, приводящий к производству первичного метаболита, может быть непосредственно использован для крупномасштабного производства этанола вместо алкогольных напитков; в данном случае этанол можно использовать как промышленное сырье или топливо. Это справедливо и для других спиртов, таких, как глицерин, который можно получить в одном из вариантов ·спиртового .брожения (рис. 9), или n-бутанол, являющийся конечным продуктом ацетонобутанолового брожения.
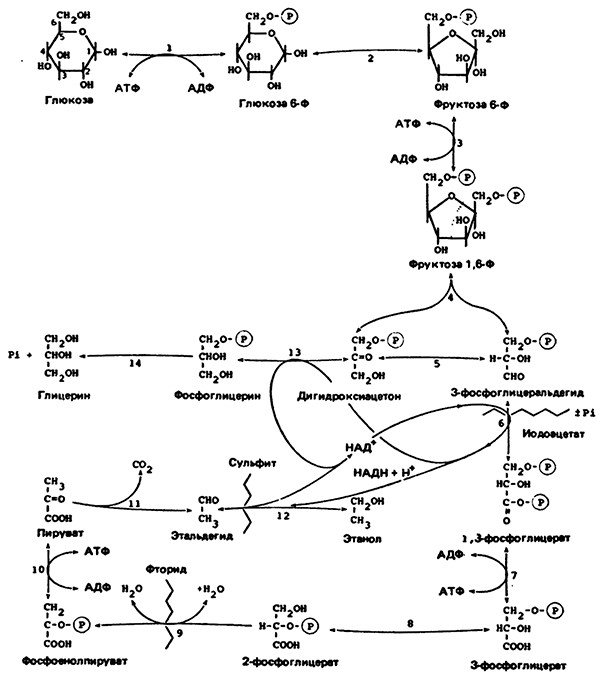
Рис. 9. Анаэробный гликолиз и спиртовое брожение.
Молекула глюкозы распадается на две молекулы триозофосфата β-фосфоглицеральдегид)
и затем превращается в две молекулы пирувата. В анаэробных условиях в дрожжевых клетках
пируват превращается в ацетальдегид, который восстанавливается в этанол. В процессе брожения
получается также небольшое количество глицерина, который образуется за счет восстановления
одного из триозофосфатов (дигидроксиацетона).
Реакции катализируются следующими фермщтами:
1 - глюкокиназой; 2 - фосфогексоизомеразой; З - фруктозо-6-фосфаткиназой; 4 - альдолазой;
5 - триозофосфатизомеразой; 6 - триозофосфатдегидрогеназой; 7 - трансфосфорилазой;
8 - фосфоглицеромутазой; 9 - енолазой; 10 - пируваткиназой; 11 - карбоксилазой;
12 - алкогольдегидрогеназой; 1З - глицерофосфатдегидрогеназой; 14 - Фосфатазой.
Как показали археологические раскопки, уже 6000 лет назад процессы брожения в экстрактах зерен хлебных злаков бъmи подлинным искусством; 5000 лет назад началось развитие виноделия. Пиво варят из ячменного солода (в меньшей степени для этого пользуются другими злаками, например просом и сорго). Соложение индуцирует в семенах ферменты, которые либо в процессе соложения, либо позднее катализируют гидролиз крахмала. В дальнейшем ячменный солод размельчают и смешивают с водой при температуре не выше 67° С; в течение нескольких часов цепи крахмала разрываются, и происходит частичный протеолиз. Водный экстракт, называемый солодовым суслом, кипятят вместе с хмелем. В процессе кипячения прекращается ферментативная активность, осаждаются белки из сусла и экстрагируются вкусовые компоненты хмеля. Затем в сусло засевают штамм Saccharomyces cerevisiae, который сбраживает сахара в спирт и углекислый газ (в процессе брожения дрожжевая биомасса увеличивается в пять раз). Ряд других соединений, придающих пиву его особенный вкус, образуются в незначительных количествах. Среди них амиловый, изоамиловый и фенилэтиловый спирты, концентрация которых составляет около нескольких миллиграммов на 1 л, уксусная и масляная кислоты, а также эфиры. По окончании брожения дрожжи отделяют от пива, которое после необходимого периода созревания фильтруют и пастеризуют. Большинство видов легкого пива получают при помощи дрожжей, которые оседают на дно ферментера. Такие дрожжи низового брожения были в 1880 г. выведены в чистую культуру датским ботаником Хансеном, работавшим в Карлсбергском институте в Копенгагене (отсюда название Saccharomyces carlsbergensis). Дрожжи верхового брожения, не оседающие в процессе ферментац и, являются штаммами S. cerevisiae и используются для получения разновидностей пива с повышенной концентрацией спирта. В 1980 г. мировое производство пива составило 700 млн. гл (гектолитров) в год.
Виноделие в большинстве регионов остается мелкомасштабным процессом, в котором традиционные навыки и способы культивирования способствуют приготовлению вина с особыми свойствами. Модернизация процесса спиртового брожения заключается в отборе более эффективных штаммов S. cerevisiae, которые добавляют к виноградному соку, в регулировании температуры брожения в диапазоне 7-14° С, а также в попытках достигнуть непрерывного брожения для получения ординарных вин.
Производство сакэ, или рисовой водки (в Японии в 1980 г. произведено 17 млн. гл), похоже скорее на пивоварение, чем на виноделие, поскольку сбраживаемым углеводом является крахмал. Последний превращается в сбраживаемые сахара под действием Aspergillus oryzae, споры которого смешивают с размолотым и сваренным на пару рисом и инкубируют пять-шесть дней при 35° С. Полученный продукт смешивают с распаренным рисом и засевают штаммом S. cetevisiae (мото). Брожение продолжается не менее трех недель. Приготовление сакэ сложный и труднорегулируемый процесс, требующий освоения различных способов брожения (в полутвердом и затопленном состоянии) и последовательного регулирования микробных популяций: сначала плесени (Aspergillus oryzae), затем бактерий (Lactobacillus и Leuconostoc spp.) и наконец дрожжей (S. cerevisiae). Концентрация спирта перед выходом в торговую сеть доводится обычно до 16% по объему, однако к концу брожения сакэ содержит не менее 20% спирта. Устойчивость дрожжевых штаммов к таким концентрациям спирта, возможно, связана с гетерогенным характером брожения. В Японии проводятся активные исследования по селекции устойчивых к спирту и температуре штаммов дрожжей с целью усовершенствовать экономическую конкурентоспособность ферментационного производства спирта.
В отличие от пивоварения для производства спиртов из зерна не нужно кипятить сусло, поэтому хотя брожение продолжается дольше, зато спирта производится больше. Характер последующей перегонки зависит от вида алкогольных напитков. Например, шотландское ячменное виски перегоняют в небольших перегонных кубах, тогда как для большинства других видов виски процесс перегонки проводят в постоянно действующих агрегатах. Для многих алкогольных напитков ферментируемая жидкость помещается в перегонные кубы вместе с щюжжами; последние наряду с компонентами, экстрагированными из деревянных бочонков, в которых выдерживаются спиртные напитки, придают вкус конечному продукту.
Одним из лимитирующих факторов в ферментационном производстве этанола являются неспособность микроорганизмов переносить высокие концентрации спирта и вызываемая этим остановка процесса брожения по достижении относительно высокого уровня концентрации спирта. Мы пока мало знаем о факторах, влияющих на устойчивость микробов к спирту, однако, по-видимому, она связана с ненасыщенными жирными кислотами клеточной мембраны; жирные кислоты могут сделать мембрану более проницаемой для спирта, что приведет к уменьшению его концентрации внутри клетки.
В связи с ростом цен на нефть ферментационное производство спирта приобретает особое значение. Со временем производство таким путем спирта в качестве топлива станет основной целью национальных программ, учитывающих следующие технические и экономические Факторы: возможность выращивать «продуцирующие спирт» растения на больших площадях, использование избыточного зерна, совершенствование платежного баланса, ухудшающегося из-за тяжелых нефтяных программ, а также технологический прогресс в связи с созданием машин, в которых спирт выступает заменителем топлива.
N-бутанол (n означает «нормальный», т. е. молекула представляет собой прямую цепь атомов углерода и не разветвлена) используется при производстве пластификаторов, гидравлических тормозов, карбамидной смолы, экстрагирующих веществ и добавок к бензину. Он производится почти исключительно химическим путем. Однако еще в 1912 г. Вейцманн, работавший тогда в Манчестерском университете, обнаружил, что Clostridium acetobutylicum и C.saccharoacetobutylicum сбраживают крахмал и сахарозу соответственно в n-бутанол и ацетон. Вейцманн для получения синтетического каучука синтезировал бутадиен из n-бутанола. Во время первой мировой войны существовал большой спрос на ацетон, так как этот растворитель использовался при производстве бездымного пороха. После войны нужда в ацетоне стала гораздо меньше, зато возросла потребность в n-бутаноле. В 1940-1950-х гг. ферментационное производство n-бутанола сократилось в связи с тем, что цена на нефтехимическое сырье упала ниже цен на кукурузу и мелассу. Тем не менее в ЮАР, где источником энергии служит уголь, n-бутанол по-прежнему производится из мелассы. По окончании процесса ферментации бактерии отделяют и используют в качестве корма для скота. Вполне возможно, что широкомасштабное возобновление ферментационного производства n-бутанола окажет существенную помощь в решении нефтяной проблемы.
Как и в случае этанола, лимитирующим фактором при ацетонобутаноловом брожении является токсичность n-бутанола для бактерий. Первые промышленные штаммы С. acetobutylicum сбраживали от силы 3,8% крахмала; при этом выход спирта составлял 1,2%. Поиск мутантных штаммов с повышенной толерантностью к n-бутанолу не увенчался сколько-нибудь заметным успехом, однако в лабораторных испытаниях удалось достигнуть устойчивости бактерий к 2,85% спирта при условии добавления в культуральную среду активированного древесного угля.

