Включенные в Подгруппу 4 семь родов сходны друг с другом не более чем с представителями других подгрупп Группы 5. Они помещены в одну подгруппу для удобства. Фенотипические признаки, позволяющие дифференцировать роды Подгруппы 4 друг от друга и от Подгрупп 1–3, приведены в табл. 5.1.
Дифференциация родов, включенных в Подгруппу 4: См. табл. 5.1.
Род Calymmatobactehum
Плеоморфные палочки, шириной 0,5–1,5 мкм и длиной 1,0–2,0 мкм» с закругленными концами, одиночные или в скоплениях. Характерны единичные или биполярные участки конденсации хроматина в клетках. Имеют капсулы. Грамотрицательные. Неподвижные. При окраске экссудата из инфицированных тканей по Райту или Гимза видны как характерные внутриклеточные организмы в цитоплазме больших мононуклеарных фагоцитов. Высокотребовательны в отношении питательной среды; могут расти in vivo в желточном мешке куриных яиц с зародышем или in vitro в специальных средах с яичным желтком, но культивирование редко бывает успешным, и ни один из штаммов не хранится в коллекциях культур. Оптимальная температура 37°С. Патогенны для человека: вызывают донованоз. Диагноз ставится по клиническим признакам и данным микроскопии (Dienst, Brownell, In: Bergey's Manual of Systematic Bacteriology, vol. 1, p. 585– 587, 1984; Albritton et al., Manual Clin. Microbiol., 4th ed., p. 869-873, 1985).
Типовой (и единственный) вид: Calymmatobacterium granulomatis.
Отличия рода Calymmatobacterium от других родов: Простейшим способом идентификации С. granulomatis служит исследование мазков пораженной ткани, окрашенных по Райту или Гимза. Характерный вид внутриклеточных организмов (рис. 5.1) специфичен для диагноза донованоз. Отличия от других родов приведены в табл. 5.1.
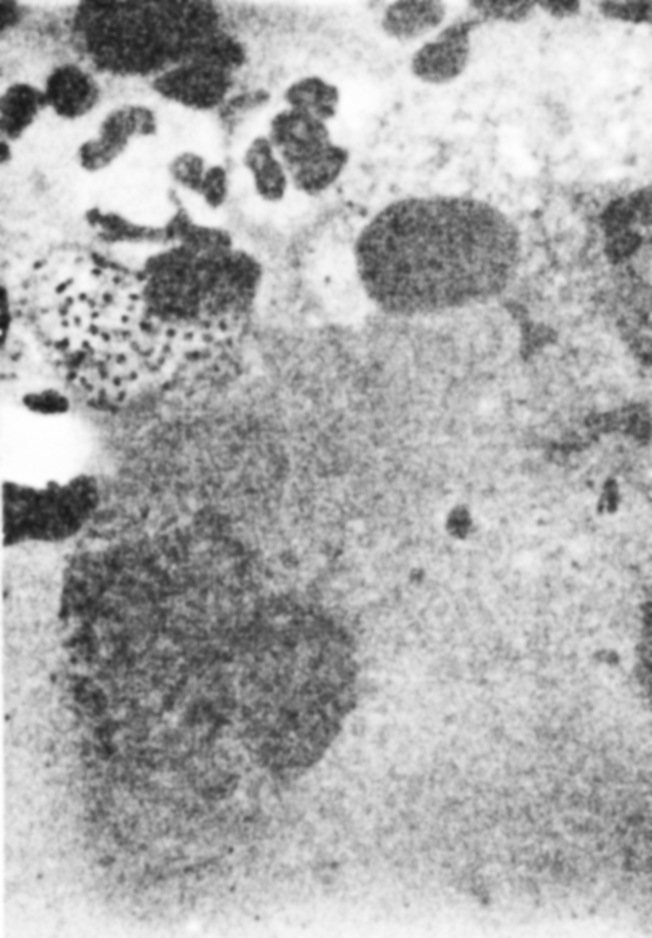
Рис. 5.1. Большие мононуклеарные фагоциты с клетками Calymmatobacterium granulomatis. Окраска по Райту (х 900). (С разрешения по R. В. Dienst, G. Н. Brownell, In: М. P. Starr et aL, (ed.) The Procaryotes: a Handbook on Habitats, Isolation and Identification of Bacteria, p 1410, 1981, Springer Verlag, New York.)
Род Cardiobacterium
Прямые палочки, 0,5–0,75 х 1–3 мкм, с закругленными концами. Иногда встречаются длинные нити. Плеоморфиые. Клетки одиночные, в парах, коротких цепочках или розетковидных скоплениях. Грамотрицательные, однако возможно сохранение кристаллического фиолетового в набухших концах или центральной часта клеток. Неподвижные. Факультативные анаэробы. Некоторые штаммы при выделении нуждаются в СО2. В аэробных условиях рост скудный. Рост в анаэробных условиях или в эксикаторе с зажженной свечой не зависит от повышенной влажности. Оптимальная температура в пределах 30–37°С. Колонии на кровяном агаре гладкие, выпуклые, матовые, через 48 ч роста 1–2 мм в диаметре, Хемоорганотрофы, метаболизм бродильного типа. Оксидазоположительные и кагалазоотрицательные. Образуют небольшие количества индола. Нитрат не восстанавливают. Из глюкозы, мальтозы, маннитола, маннозы, сахарозы, сорбитола и фруктозы образуют кислоту, но не газ (в течение 7 сут). Не растут на агаре Макконки. По уреазе и орнитиндекарбоксилазе отрицательные. Встречаются в микрофлоре носовой полости у человека. Патогенны для человека: вызывают эндокардит.
Типовой (и единственный) вид: Cardiobacterium hominis.
Отличия Cardiobacterium от других родов: Один или оба конца клеток часто утолщены и в этих областях в большей или меньшей степени удерживается кристаллический фиолетовый при окраске по Граму. Один из важных признаков для идентификации – образование индола, которое, однако, может быть слабым и недоступным для определения без концентрирования индола путем его экстракции ксиленом (Weaver, In: Bergey's Manual of Systematic Bacteriology, vol. 1, p. 583– 585, 1984). В тестах на гидролиз эскулина, разжижение желатины, образование H2S, гидролиз Твин-20 и Твин-40, а также сбраживание адонитола, арабинозы, галактозы, дульцитола, инозитола, ксилозы, лактозы, мелецитозы, мелибиозы, рамнозы, салицина, трегалозы, целлобиозы и эритритола результаты отрицательные.
Признаки, отличающие Cardiobacterium от других родов, приведены в табл. 5.1 и 5.56.
Таблица 5.56. Дифференциация Cardiobacterium hominis и фенотипически сходных родов и видов1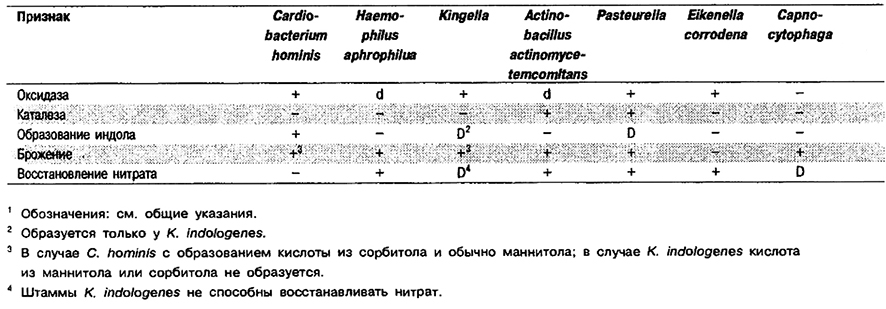
Род Chromobacterium
Палочки, 0,6–0,9 х 1,5–3,5 мкм, с закругленными концами, иногда слегка изогнутые; одиночные, иногда в парах, встречаются удлиненные формы или короткие цепочки. Капсул и покоящихся стадий не образуют. Грамотрицательные, часто окрашиваются полосами или биполярно и содержат липидные включения. Подвижные за счет единственного полярного жгутика и обычно 1–4 субполярных или латеральных жгутиков. Факультативные анаэробы. На плотных средах образуют маслянистые колонии фиолетового цвета; в жидких средах образуют фиолетовое кольцо по стенке сосуда у поверхности жидкости. На обычных средах растут при 25 однако по оптимальной температуре виды различаются. Хемоорганотрофы; метаболизм в основном бродильного типа. Образуют кислоту, но не газ из глюкозы, трегалозы, фруктозы и обычно маннозы, но не из дульцитола, инозитола, инулина, ксилозы, лактозы и маннитола. Как правило, оксидазоположительные (реактив Ковача), но считыванию результатов может мешать фиолетовый пигмент. Катал азоположительные. Индолотрицательные. Реакция Фогеса-Проскауэра отрицательная. Восстанавливают нитрат. Разжижают желатину. По лизин- и орнитиндекарбоксилазе, фенилаланиндезаминазе и гидролизу эскулина отрицательные. Исследованные организмы (только С. violaceum) не образуют кислоты из адонитола, мелецитозы, мелибиозы и рафинозы, дают отрицательную реакцию в тестах на О-нитрофенил-β-D-галактопиранозид, дезоксирибонуклеазу и расщепление пектата, способны к росту в присутствии KCN. Устойчивы к бензилпенициллину (10 мкг/мл) и вибрностатнческому агенту О/129. Почвенные и водные организмы. С. violaceum иногда вызывает тяжелые гнойные или септические инфекции у млекопитающих и человека.
Типовой вид: Chromobacterium violaceum.
Отличия Chromobacterium от других родов: Признаки, отличающие Chromobacterium от других родов Подгруппы 4, приведены в табл. 5.1. Некоторые виды, ранее отнесенные к Chromobacterium, теперь классифицированы в составе рода Janthi- nobacterium. Признаки, отличающие Chromobacterium от Janthinobacterium, приведены в табл. 5.57.
Таблица 5.57. Признаки» отличающие род Chromobacterium от рода Janthinobacterium1
Дифференциация видов рода Chromobacterium: См. табл. 5.58.
Таблица 5.58. Признаки видов рода Chromobacterium1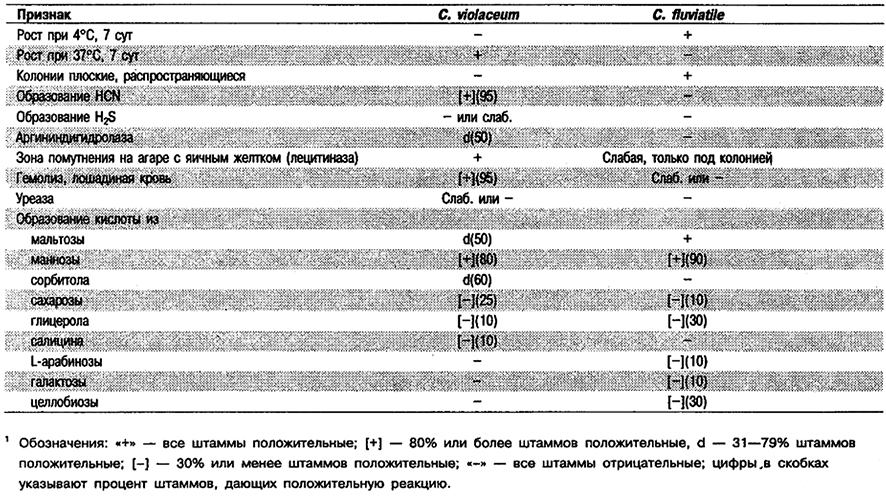
Род Eikenella
Прямые палочки, 0,3–0,4 х 1,5–4,0 мкм. Иногда образуют короткие нити. Неспорообразующие. Грамотрицательные. Неподвижные, не имеют жгутиков, однако на поверхности агара возможна подвижность рывками. Факультативные анаэробы. Оптимальная температура 35–37°С. Рост колоний может приводить к коррозии поверхности агара. Негемолитики; вокруг колоний на кровяном агаре может наблюдаться слабое позеленение. Оксидазоположительные (метод Ковача). Отрицательные по каталазе, уреазе, аргининдигидролазе и индолу. Положительные по лизиндекарбоксилазе. Восстанавливают нитрат до нитрита. Из глюкозы и других углеводов кислоты не образуют. Для роста в аэробных условиях обычно нуждаются в гемине. Встречаются в полости рта и кишечника у человека, могут вызывать оппортунистические инфекции.
Типовой (и единственный) вид: Eikenella corrodens.
Отличия Eikenella от других родов: Признаки, отличающие Eikenella от других родов Подгруппы 4, приведены в табл. 5.1. Дифференциация Eikenella от других родов и видов представлена в табл. 5.59.
Таблица 5.59. Отличия ВкелеИа от сходных организмов1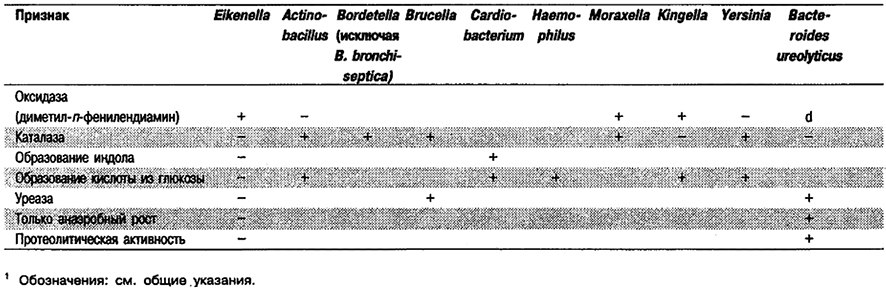
Признаки вида: Размеры колоний достигают через 24 ч роста 0,2–0,5 мм и через 48 ч 0,5–1,0 мм. Колонии выглядят растущими как бы в мелких углублениях на поверхности среды (рис. 5.2). Культуры в чашках Петри имеют запах хлорной извести, напоминающий также запах культур, характерный для видов Haemophilus и Pasteurella. В жидких средах рост, как правило, скудный; его стимулирует добавление холестерола (Henricksen, Int. J. Syst. Bacterid. 19: 165–166, 1969) или 3% сыворотки крови. Такой же эффект оказывает добавление 0,2% агара (Jackson et al., J. Med. Microbiol. 4: 171–184, 1971). Для роста свежевыделенных культур в аэробных, но не в анаэробных условиях необходим гемин (от 5 до 25 мкг/мл). Как аэробному, так и анаэробному росту свежевыделенных культур способствует повышенная концентрация (5–10%) СО2. Желатину не гидролизуют, результаты теста на орнитиндекарбоксил азу вариабельные.
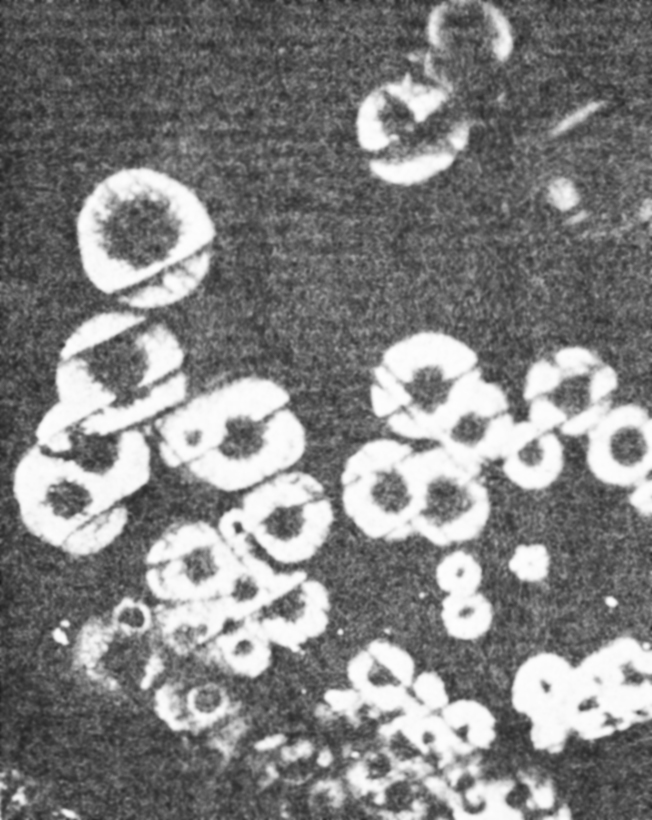
Рис. 5.2. Колонии БкепеНа corrodens на агаризованной среде с кровью барана, 48 ч инкубации. Диаметр колоний 0,5–1,0 мм. (С разрешения no Е. J. Bottone, J. Kittick, S. S. Schneierson, American Cliri. Pathol. 59; 560-566, 1973, American Society of Clinical Pathology.)
Род Gardnerella
Плеоморфные палочки, 0,5 х 1,5–2,5 мкм. Капсул и эндоспор не образуют. От грамотрнцательных до грамварнабельных. Неподвижные. Факультативные анаэробы. Требовательные к составу питательной среды, но не нуждаются в факторе X или факторе V. Каталазо- и оксидазоотрицательные. Хемоорганотрофы, метаболизм бродильного типа. Оптимальная температура для роста 35–37°С. Образуют кислоту, но не газ из глюкозы и других углеводов. Не восстанавливают нитрат. Гидролизуют гиппурат. Вызывают гемолиз крови человека, но не барана. Обнаружены в мочеполовых путях у человека, Считаются основными возбудителями бактериального «неспецифического» вагинита.
Типовой (и единственный) вид: Gardnerella vaginalis.
Отличия рода Gardnerella от других родов: Признаки, отличающие Gardnerella от других родов Подгруппы 4, приведены в табл. 5.1. Дифференциация Gardnerella от других родов представлена в табл. 5,60.
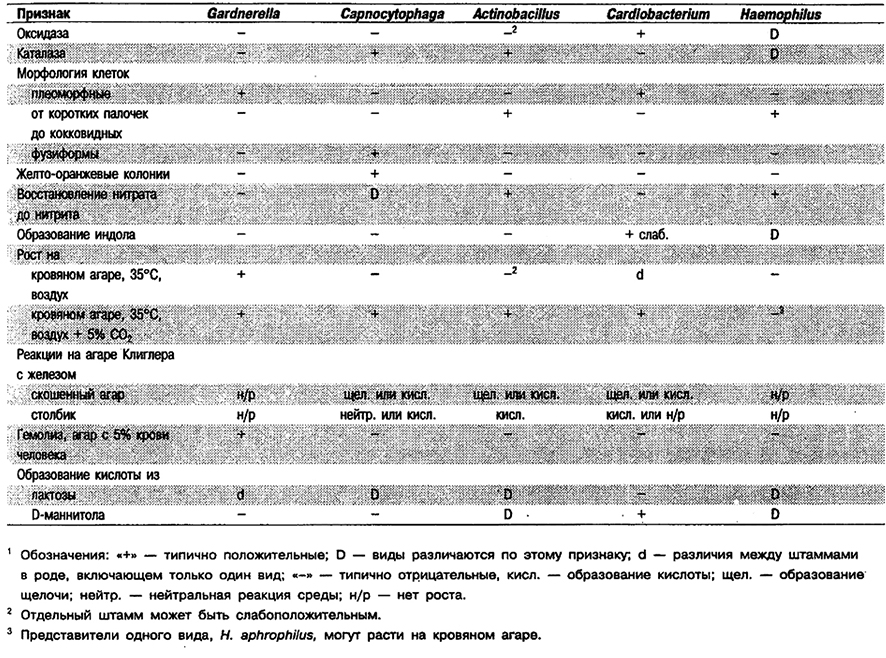
Таблица 5.60. Дифференцирующие признаки рода Gardnerella
и других морфологически и физиологически сходных родов1
Признаки вида: Слабый рост либо его отсутствие на МПА или наиболее употребительных селективных средах. На агаре Vaginalis через 48 ч инкубации в СО2-инкубаторе или в эксикаторе с зажженной свечой образуются колонии диаметром 0,5 мм. Для проведения тестов на образование кислоты из углеводов, оксидазу, каталазу, гемолиз, а также гидролиз гиппурата необходимо использовать специальные методики (Greenwood, Pickett, In: Bergey's Manual of Systematic Bacteriology, vol. 1, p. 587–591, 1984). Результаты тестов на аргининдигидролазу, гидролиз эскулина, гидролиз желатины, H2S, индол, лизинде карбоксилазу, фенилаланиндеэаминазу, орнитиндекарбоксилазу, гидролиз Твин-80, уреазу и ацетоин (реакция Фогеса-Проскауэра) отрицательные. Не образуют кислоты из арбутина, глицерола, инозитола, маннитола, мелибиозы, рафинозы, рамнозы, салицина и целлобиозы. Результаты тестов на липазу, О-нитрофенил-β-D-гадактопиранозид, образование кислоты из L-арабинозы, галактозы, инсулина, ксилозы, лактозы, маннозы, сахарозы и фруктозы вариабельные. Результаты тестов с метиловым красным, на ингибирование Н2О2, гидролиз крахмала и образование кислоты из декстрина, крахмала, мальтозы и рибозы положительные.
Род Streptobacillus
Палочки, 0,1–0,7 х 1–5 мкм, с закругленными или заостренными концами, одиночные либо в длинных волнистых цепочках или нитях длиной 10–150 мкм. Могут быть в значительной степени плеоморфными. У одиночных палочек возможно вздутие в центральной части; цепочки и нити могут иметь ряд вздутий, создающий вид бус. Грамотрицательные, Неподвижные, Факультативные анаэробы. Для роста нуждаются в сыворотке, асцитической жидкости или крови. Росту способствует высокая влажность среды или пониженное содержание агара (мягкий агар). В процессе культивирования возможно спонтанное превращение в L-фазный или переходный варианты. Оптимальная температура 35–37°С. Хемоорганотрофы. Глюкозу и другие углеводы сбраживают с образованием кислоты, но не газа. Каталазо- и оксидазоотрицательные. Индол не образуют. Нитрат до нитрита не восстанавливают. Присутствуют в глотке и носоглотке диких и лабораторных крыс. Вызывают у человека одну из форм болезни от укуса крыс.
Типовой (и единственный) вид: Slreptobacillus moniliformis.
Отличия Streptobacillus от других родов: Признаки, отличающие Streptobacillus от других родов, приведены в табл. 5.1 и 5.61.
Таблица 5.61. Отличие Slreptobacillus от других родов1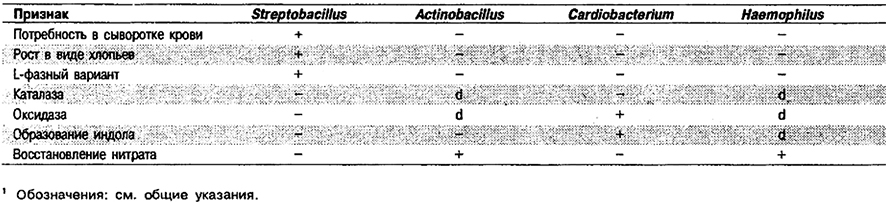
Признаки вида: Колонии на сывороточном агаре 1–2 мм в диаметре через 3 сут. Колонии, образованные L-фазным вариантом, гораздо мельче и имеют типичный вид «яичницы-глазуньи» с плотным центром, проникающим в агар. Колонии не производят гемолиз на агаре с кровью лошади или барана. Культуры, выращенные в жидкой среде с сывороткой, образуют белый хлопьевидный осадок или беловатые гранулы на дне и стенках пробирок; среда над осадком обычно прозрачная. Выделение из большинства очагов поражения представляет трудности из-за потребности организмов для роста в сыворотке крови и высокой влажности, а также из-за их медленного роста и вероятности преимущественного роста сопутствующих организмов. Период жизнеспособности культур короток. Пересевы следует делать сразу после обнаружения роста. Для пересева колоний L-фазного варианта нужно размазать по поверхности агаризованной среды небольшие агаровые блоки, взятые из участка интенсивного роста. Во все среды для биохимических тестов необходимо добавлять сыворотку, кровь или асцитическую жидкость. Биохимические реакции, особенно для L-фазного варианта, лучше проводить на пластинках агаризованной среды, содержащей в качестве добавок лошадиную сыворотку и субстраты и/или индикаторы, простерилизованные фильтрованием (Cohen et al., Appl. Microbiol. 16: 1655–1662, 1968), Все тесты должны включать незасеянные контрольные чашки Петри со средой, содержащей субстраты,. и засеянные контрольные чашки Петри со средой, к которой вместо субстратов добавлена дистиллированная вода. Результаты тестов на разжижение желатины, с метиловым красным, на фенилаланиндезаминазу, уреазу и ацетоин (Фогеса-Проскауэра) отрицательные, на гидролиз эскулина вариабельные, на аргининдигидролазу и образование H2S положительные. При сбраживании галактозы, гликогена, декстрина, инулина, крахмала, мальтозы, маннозы, салицина и фруктозы образуют кислоту. Не сбраживают адонитол, арабикозу, глицерол, дульцитол, инозитол, ксилозу, лактозу, маннитол, меле цитозу, мелибиозу, рафинозу, рамнозу, сорбитол, сахарозу, сорбозу, трегалозу и целлобиозу.
Род Zymomonas
Палочки, 1,0–1,4 х 2–6 мкм, с закругленными концами, обычно в парах. Грамотрицательные. Обычно неподвижные; если подвижные, имеют 1–4 полярных жгутика. Факультативные анаэробы; некоторые штаммы – облигатные анаэробы. Хемоорганотрофы; растут за счет использования глюкозы или фруктозы, сбраживая 1 моль сахара с образованием почти 2 моль этанола, 2 моль СО2 и некоторого количества молочной кислоты. Некоторые штаммы используют также сахарозу, но не другие источники углерода. Оптимальный диапазон температуры 25–30°С. Колонии на стандартной среде (D-глюкоза, 20 г, дрожжевой экстракт, 5 г на 1 л дистиллированной воды) блестящие, с ровным краем, от белых до кремовых, через 2 сут 1–2 мм в диаметре, с фруктовым запахом. Оксидазоотрицательные и каталазоположительные. Желатин азу не образуют. Нитрат не восстанавливают, индол не образуют. Для хорошего роста нуждаются в смеси аминокислот, но ни одна из аминокислот сама по себе не оказывает эффекта. Нуждаются в биотине и пантотенате. Встречаются как возбудители порчи в ниве, сндре и грушевом сидре, как возбудители брожения в соке агавы, пальмовом соке и соке сахарного тростника, а также на медоносных пчелах и в созревающем меде.
Типовой вид: Zymomonas mobilis.
Отличия рода Zymomonas от других родов: Фенотипические признаки Zymomonas хорошо выражены и его легко идентифицировать. Особый признак – количественное сбраживание глюкозы, фруктозы или сахарозы, но не других сахаров, с образованием эквимолярных количеств этанола и СО2. Признаки, отличающие Zymomonas от других родов, приведены в табл. 5.1 и 5.62.
Таблица 5.62. Дифференцирующие признаки рода Zymomonas и других родов1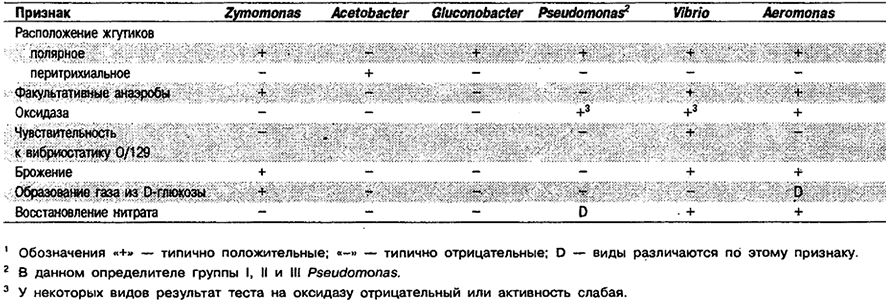
Признаки Zymomonas mobilis: Отсутствие спор и капсул. Отсутствие роста в МПБ или жидкой среде с 1% пептона. Для обогащения рекомендуется использовать среду Дэддса (см. Swings, De Ley, In: Bergey's Manual of Systematic Bacteriology, vol. 1, p. 576–580, 1984). Дают слабоположительную реакцию Фогеса-Проскауэра, вариабельные результаты в тестах на H2S, лизин- и орнитиндекарбоксилазу, аргининдигидролазу, уреазу. Не сбраживают или не используют в качестве источников углерода следующие вещества: адонитол, D-арабинозу, L-арабинозу, D-галактуронат, глицерол, крахмал, D-ксилозу, декстрин, дульцитол, DL-лактат, лактозу, DL-малат, мальтозу, D-маннитол, D-маннозу, пируват, рафинозу, L-рамнозу, D-рибозу, салицин, D-сорбитол, L-сорбозу, сукцинат, тартрат, трегалозу, целлобиозу, цитрат, эритритол и этанол. Для дифференциации Z mobilis subsp. mobilis от Z mobilis subsp, pomacii используют следующие признаки: наличие роста при 36°С (первый растет, второй нет) и размеры колоний после роста в течение 7 сут при 30°С в аэробных условиях (в первом случае 1,5 мм, во втором 1 мм).

